解题方法
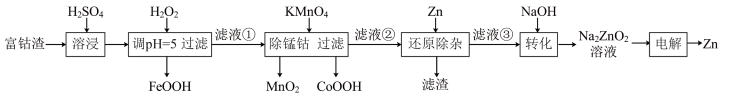
1 . 电解锌的生产过程中产生大量富钴渣,主要含金属Zn、Cd及CoO、MnO和FeO。采用以下工艺可利用富钴渣生产高纯锌_______ 。
(2)加入H2O2后生成FeOOH的化学方程式为_______ 。
(3)“滤液①”中含有的金属离子有Cd2+、Co2+、_______ 。
(4)“除锰钴”中,生成MnO2的离子方程式为_______ 。
(5)还原除杂的“滤渣”主要成分是_______ 。
(2)加入H2O2后生成FeOOH的化学方程式为
(3)“滤液①”中含有的金属离子有Cd2+、Co2+、
(4)“除锰钴”中,生成MnO2的离子方程式为
(5)还原除杂的“滤渣”主要成分是
您最近一年使用:0次
解题方法
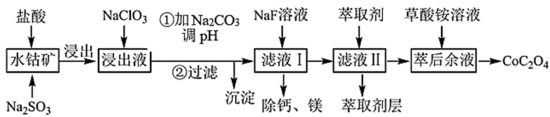
2 . 利用水钴矿(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等)制取草酸钴的工艺流程如下:
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)为增大水钴矿的浸取效率,可采取的措施为______ 。(任写一条)
(2)向浸出液中加入NaClO3对应的离子反应方程式为______ ,制取NaClO3可以将氯气通入到热的浓氢氧化钠溶液,该反应的离子方程式为______ ;实验需要制取21.3克NaClO3,需要的氯气由电解食盐水生成,若不考虑反应过程中的损失,则同时生成的氢气的体积为______ (标准状况)。
(3)向浸出液中加入碳酸钠后析出的沉淀是______ ,至少调节pH为______ 。
(4)滤液Ⅱ中加入萃取剂的目的是______ 。
(5)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液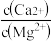 =
=______ 。
(6)取15gCoC2O4样品灼烧(CoC2O4=CoO+CO+CO2,假设杂质不参与变化),将分解产生的气体收集起来得到标况下体积为4.48L的气体,则CoC2O4的纯度为_______ 。
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)为增大水钴矿的浸取效率,可采取的措施为
(2)向浸出液中加入NaClO3对应的离子反应方程式为
(3)向浸出液中加入碳酸钠后析出的沉淀是
(4)滤液Ⅱ中加入萃取剂的目的是
(5)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10。当加入过量NaF后,所得滤液
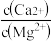 =
=(6)取15gCoC2O4样品灼烧(CoC2O4=CoO+CO+CO2,假设杂质不参与变化),将分解产生的气体收集起来得到标况下体积为4.48L的气体,则CoC2O4的纯度为
您最近一年使用:0次
解题方法
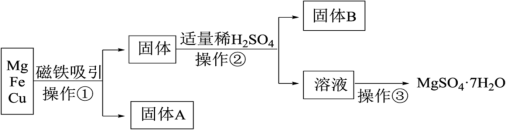
3 . 有Mg、Fe、Cu的混合粉末,分离得到MgSO4·7H2O过程如下:___________ 。
(2)操作②的名称是___________ ,需要用到的主要玻璃仪器有 ___________ 、玻璃棒,其中玻璃棒的作用是___________ 。
(3)操作②发生的离子反应方程式为___________ ,属于___________ 反应。(填基本反应类型)
(4)实验中可选用适量的下列试剂中的代替稀H2SO4___________ (填标号)。
A. CuSO4溶液 B.FeSO4溶液 C.稀盐酸
(5)操作③主要包含蒸发浓缩、___________ 、过滤、洗涤烘干等。
(2)操作②的名称是
(3)操作②发生的离子反应方程式为
(4)实验中可选用适量的下列试剂中的代替稀H2SO4
A. CuSO4溶液 B.FeSO4溶液 C.稀盐酸
(5)操作③主要包含蒸发浓缩、
您最近一年使用:0次
4 . 氯化钠是一种重要的食品添加剂与工业原料,自春秋时期,齐国管仲就提出了“官山海”政策,即对盐实行专卖。秦国商鞅变法,控制山泽之利,也实行食盐专卖。
(1)实验室现需要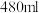

 溶液,配制时使用容量瓶的规格为
溶液,配制时使用容量瓶的规格为___________ ;下列操作会使所配溶液浓度偏低的是___________ (填标号)。
a.容量瓶洗涤干净后未放入加热烘箱干燥
b.定容、摇匀后发现液面下降,再加适量的蒸馏水
c.在定容时俯视容量瓶上的刻度线
d.初次转移溶液后,未洗涤烧杯和玻璃棒
(2)粗盐中常含有少量的 Ca2+、Mg2+、 等杂质离子,可采用如图的工序来纯化。
等杂质离子,可采用如图的工序来纯化。___________ 、___________ 的方法。
②试剂a中包含多种物质,按滴加顺序依次是NaOH、___________ 、___________ (填化学式)。要在实验室中完成“过滤”操作,需要的玻璃仪器包括烧杯、玻璃棒、___________ 。
③要检验产品中是否存在 ,需要进行的操作是
,需要进行的操作是___________ 。
④某工厂因工艺不佳,其最终的产品中混入了少量的FeCl3,已知FeCl3与 Na2EDTA可发生反应 (产品中其他物质不与Na2EDTA反应),若质量监督管理人员在实验中称取5.000 g产品,测试发现恰好能与20.00 ml 0.01 mol/L Na2EDTA溶液完全反应,则产品中FeCl3的质量分数是
(产品中其他物质不与Na2EDTA反应),若质量监督管理人员在实验中称取5.000 g产品,测试发现恰好能与20.00 ml 0.01 mol/L Na2EDTA溶液完全反应,则产品中FeCl3的质量分数是___________ (保留两位有效数字)。
(1)实验室现需要
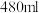

 溶液,配制时使用容量瓶的规格为
溶液,配制时使用容量瓶的规格为a.容量瓶洗涤干净后未放入加热烘箱干燥
b.定容、摇匀后发现液面下降,再加适量的蒸馏水
c.在定容时俯视容量瓶上的刻度线
d.初次转移溶液后,未洗涤烧杯和玻璃棒
(2)粗盐中常含有少量的 Ca2+、Mg2+、
 等杂质离子,可采用如图的工序来纯化。
等杂质离子,可采用如图的工序来纯化。
②试剂a中包含多种物质,按滴加顺序依次是NaOH、
③要检验产品中是否存在
 ,需要进行的操作是
,需要进行的操作是④某工厂因工艺不佳,其最终的产品中混入了少量的FeCl3,已知FeCl3与 Na2EDTA可发生反应
 (产品中其他物质不与Na2EDTA反应),若质量监督管理人员在实验中称取5.000 g产品,测试发现恰好能与20.00 ml 0.01 mol/L Na2EDTA溶液完全反应,则产品中FeCl3的质量分数是
(产品中其他物质不与Na2EDTA反应),若质量监督管理人员在实验中称取5.000 g产品,测试发现恰好能与20.00 ml 0.01 mol/L Na2EDTA溶液完全反应,则产品中FeCl3的质量分数是
您最近一年使用:0次
解题方法
5 . 氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业氧化锌[含有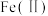 、
、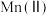 、
、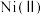 等杂质]的流程如下
等杂质]的流程如下


已知:①在本实验条件下,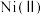 不能被氧化;高锰酸钾的还原产物是
不能被氧化;高锰酸钾的还原产物是 。
。
②不考虑操作过程中引起的质量损失。
回答下列问题:
(1)加稀硫酸酸浸时,常将工业 粉碎,其目的是
粉碎,其目的是_____ 。
(2)过滤时,主要用到的玻璃仪器有烧杯、玻璃棒和________ ,其中玻璃棒的作用为_________ 。
(3)②发生反应的离子方程式有 和
和________ 。
(4)若④中产物仅为 ,则发生反应的离子方程式为
,则发生反应的离子方程式为________ ;取干燥后的滤饼 ,煅烧后可得到产品(
,煅烧后可得到产品( )
) ,则
,则 等于
等于_____ (用含a、m的代数式表示)。
(5)④形成的沉淀要水洗,检验沉淀是否洗涤干净的操作和现象是________ 。
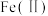 、
、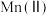 、
、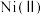 等杂质]的流程如下
等杂质]的流程如下

已知:①在本实验条件下,
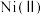 不能被氧化;高锰酸钾的还原产物是
不能被氧化;高锰酸钾的还原产物是 。
。②不考虑操作过程中引起的质量损失。
回答下列问题:
(1)加稀硫酸酸浸时,常将工业
 粉碎,其目的是
粉碎,其目的是(2)过滤时,主要用到的玻璃仪器有烧杯、玻璃棒和
(3)②发生反应的离子方程式有
 和
和(4)若④中产物仅为
 ,则发生反应的离子方程式为
,则发生反应的离子方程式为 ,煅烧后可得到产品(
,煅烧后可得到产品( )
) ,则
,则 等于
等于(5)④形成的沉淀要水洗,检验沉淀是否洗涤干净的操作和现象是
您最近一年使用:0次
解题方法
6 . 粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。某班同学在粗盐提纯实验中,为把少量可溶性杂质 、
、 一并除去,设计了如下方案:
一并除去,设计了如下方案:
(1)为了加快粗盐的溶解,可采取的措施有_______ (填一种即可)。
(2)写出步骤ⅳ中发生反应的化学方程式:_______ 。
(3)沉淀B的主要成分为_______ (填化学式);往沉淀B中加入足量稀盐酸,观察到的现象为_______ 。
(4)在步骤ⅵ中,___ (填“能”或“不能”)用稀硝酸代替稀盐酸进行该实验,理由为____ 。
(5)步骤ⅶ中操作b指的是_______ 。
(6)该方案实际得到的氯化钠比粗盐中含有的氯化钠要多,理由为_______ 。
 、
、 一并除去,设计了如下方案:
一并除去,设计了如下方案: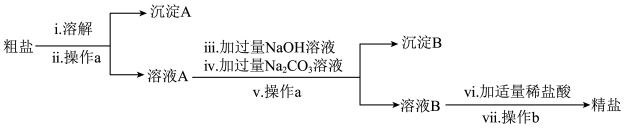
(1)为了加快粗盐的溶解,可采取的措施有
(2)写出步骤ⅳ中发生反应的化学方程式:
(3)沉淀B的主要成分为
(4)在步骤ⅵ中,
(5)步骤ⅶ中操作b指的是
(6)该方案实际得到的氯化钠比粗盐中含有的氯化钠要多,理由为
您最近一年使用:0次
解题方法
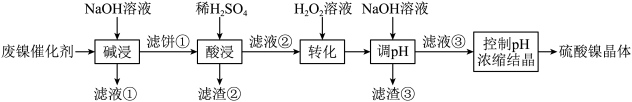
7 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体( ):
):
回答下列问题:
(1)“碱浸”中NaOH溶液可以有效地除去金属铝及其氧化物,写出NaOH溶液除去铝单质的离子方程式___________ 。
(2)“滤液②”中含有的金属离子有Fe2+和___________ ,检验Fe2+的试剂是铁氰化钾溶液,写出Fe2+和铁氰化钾溶液反应的离子方程式___________ 。
(3)利用上述表格数据,计算 的
的
___________ (写出计算结果)。如果“转化”后的溶液中 浓度为
浓度为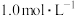 ,则“调pH”应控制的pH范围是
,则“调pH”应控制的pH范围是___________ 。
(4)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的 。写出该反应的离子方程式
。写出该反应的离子方程式___________ 。
 ):
):
| 金属离子 |  |  | Fe3+ |  |
开始沉淀时(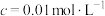 )的pH )的pH | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时( )的pH )的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中NaOH溶液可以有效地除去金属铝及其氧化物,写出NaOH溶液除去铝单质的离子方程式
(2)“滤液②”中含有的金属离子有Fe2+和
(3)利用上述表格数据,计算
 的
的
 浓度为
浓度为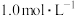 ,则“调pH”应控制的pH范围是
,则“调pH”应控制的pH范围是(4)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的
 。写出该反应的离子方程式
。写出该反应的离子方程式
您最近一年使用:0次
8 . 二氧化氯 是一种高效消毒灭菌剂。但稳定性较差,可将其用吸收法和电解法两种方法得到较稳定的
是一种高效消毒灭菌剂。但稳定性较差,可将其用吸收法和电解法两种方法得到较稳定的 加以保存。其工艺流程示意图如下图所示:
加以保存。其工艺流程示意图如下图所示:
ⅰ.纯 易分解爆炸,一般用稀有气体或空气稀释到
易分解爆炸,一般用稀有气体或空气稀释到 以下。
以下。
ⅱ.长期放置或高于 时
时 易分解生成
易分解生成 和
和 。
。
(1)步骤1中,生成 的离子方程式是
的离子方程式是_______ ,通入空气的作用是_______ 。
(2)方法1中,反应的离子方程式是_______ ,利用方法1制 时,温度不能超过
时,温度不能超过 ,可能的原因是
,可能的原因是_______ 。
(3)方法2中,利用下图所示装置制备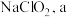 电极(左侧电极)处发生的电极反应式为
电极(左侧电极)处发生的电极反应式为______ ,b电极(右侧电极)处发生的电极反应式为_____ 。溶液中的溶质浓度:f处____ d处(填“>”、“<”或“=”)。 的溶解度曲线如下图所示,步骤3中从
的溶解度曲线如下图所示,步骤3中从 溶液中获得
溶液中获得 的操作是
的操作是_______ 。 使用时,加入稀盐酸即可迅速得到
使用时,加入稀盐酸即可迅速得到 ,写出反应的离子方程式:
,写出反应的离子方程式:_______ 。若加入盐酸浓度过大,则气体产物中 含量会增大,原因是
含量会增大,原因是_______ 。
 是一种高效消毒灭菌剂。但稳定性较差,可将其用吸收法和电解法两种方法得到较稳定的
是一种高效消毒灭菌剂。但稳定性较差,可将其用吸收法和电解法两种方法得到较稳定的 加以保存。其工艺流程示意图如下图所示:
加以保存。其工艺流程示意图如下图所示:
ⅰ.纯
 易分解爆炸,一般用稀有气体或空气稀释到
易分解爆炸,一般用稀有气体或空气稀释到 以下。
以下。ⅱ.长期放置或高于
 时
时 易分解生成
易分解生成 和
和 。
。(1)步骤1中,生成
 的离子方程式是
的离子方程式是(2)方法1中,反应的离子方程式是
 时,温度不能超过
时,温度不能超过 ,可能的原因是
,可能的原因是(3)方法2中,利用下图所示装置制备
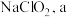 电极(左侧电极)处发生的电极反应式为
电极(左侧电极)处发生的电极反应式为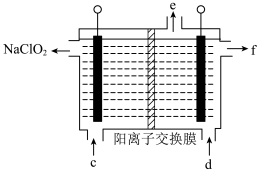
 的溶解度曲线如下图所示,步骤3中从
的溶解度曲线如下图所示,步骤3中从 溶液中获得
溶液中获得 的操作是
的操作是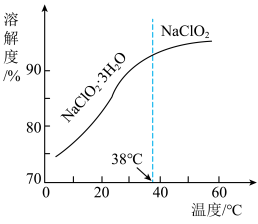
 使用时,加入稀盐酸即可迅速得到
使用时,加入稀盐酸即可迅速得到 ,写出反应的离子方程式:
,写出反应的离子方程式: 含量会增大,原因是
含量会增大,原因是
您最近一年使用:0次
解题方法
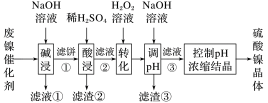
9 . 某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
回答下列问题:
(1)“碱浸”中NaOH的两个作用分别是______ 。为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式______ 。
(2)“滤液②”中含有的金属离子是______ 。
(3)若工艺流程改为先“调pH”后“转化”,即,“滤液③”中可能含有的杂质离子为______ 。
(4)如果“转化”后的溶液中Ni2+浓度为1.0mol·L-1,则“调pH”应控制的pH范围是______ 。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式______ 。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是______ 。

| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时 (c=0.01mol·L-1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时 (c=1.0×10-5mol·L-1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)“碱浸”中NaOH的两个作用分别是
(2)“滤液②”中含有的金属离子是
(3)若工艺流程改为先“调pH”后“转化”,即,“滤液③”中可能含有的杂质离子为
(4)如果“转化”后的溶液中Ni2+浓度为1.0mol·L-1,则“调pH”应控制的pH范围是
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
您最近一年使用:0次
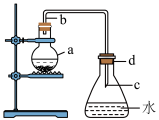
10 . 中学实验室用下图所示装置制取少量溴苯,请填写下列空白:___________ 的作用。
(2)反应过程中在导管c的下口附近可以观察到有白雾出现,这是由于反应生成的___________ 遇水蒸气而形成的。
(3)反应完毕后,向锥形瓶d中滴入AgNO3溶液,有___________ 生成。
(4)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有棕色不溶于水的液体,这是溶解了___________ 的粗产品溴苯。
(5)写出烧瓶a中发生反应的化学方程式:___________ 。
(6)提纯粗溴苯的方法是将含有溴的溴苯倒入氢氧化钠溶液中充分混合,发生的化学反应方程式是___________ ,待静置分层后,用___________ 分离出下层液体,即为溴苯。
(2)反应过程中在导管c的下口附近可以观察到有白雾出现,这是由于反应生成的
(3)反应完毕后,向锥形瓶d中滴入AgNO3溶液,有
(4)反应完毕后,将烧瓶a中的液体倒入盛有冷水的烧杯里,可以观察到烧杯底部有棕色不溶于水的液体,这是溶解了
(5)写出烧瓶a中发生反应的化学方程式:
(6)提纯粗溴苯的方法是将含有溴的溴苯倒入氢氧化钠溶液中充分混合,发生的化学反应方程式是
您最近一年使用:0次



