名校
1 . 实验室在酸性环境下用重铬酸钠氧化环己醇制备环己酮的流程如图所示:
下列说法不正确的是
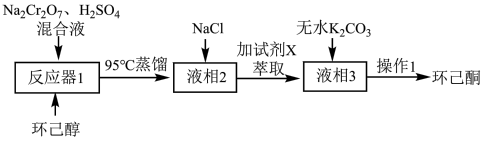
下列说法不正确的是
A.若将环己醇滴加入 和 和 的混合溶液中会降低环己酮的产率 的混合溶液中会降低环己酮的产率 |
| B.NaCl可降低产物在水中溶解度,便于后续萃取、分液 |
| C.“试剂X”可选用丙酮一次萃取“液相2”来提高产率 |
| D.“操作1”中可选用空气冷凝管 |
您最近一年使用:0次
名校
解题方法
2 . 工业上高炉炼铁产生的CO和CO2可以按如下流程脱除或利用。___________ 。
(2)煅烧产生的尾气可通过途径Ⅱ转化为CO2.。2分子氨和1分子CO2生产A,最终转化为尿素[CO(NH2)2];可通过途径Ⅲ转为b。
①下列说法正确的是___________ 。
A.黄铁(FeS2)可作为高炉炼铁的铁源
B.途径Ⅱ可通过实现反应转化MnO2+CO→CO2+Mn2O3
C.化合物A是一种盐
D.化合物B为CH3COONa
②尿素[CO(NH2)2]在较高温度下可以聚合成环状化合物三聚氰胺(C3H6N6),写出该反应的化学方程式___________ 。
(3)设计实验验证化合物A中含有N元素___________ ;写出实验过程中涉及的反应方程式___________ 。

已知: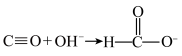 。请回答:
。请回答:
(2)煅烧产生的尾气可通过途径Ⅱ转化为CO2.。2分子氨和1分子CO2生产A,最终转化为尿素[CO(NH2)2];可通过途径Ⅲ转为b。
①下列说法正确的是
A.黄铁(FeS2)可作为高炉炼铁的铁源
B.途径Ⅱ可通过实现反应转化MnO2+CO→CO2+Mn2O3
C.化合物A是一种盐
D.化合物B为CH3COONa
②尿素[CO(NH2)2]在较高温度下可以聚合成环状化合物三聚氰胺(C3H6N6),写出该反应的化学方程式
(3)设计实验验证化合物A中含有N元素
您最近一年使用:0次
名校
解题方法
3 . 富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下。


A.酸浸时镁硼酸盐发生反应为 |
| B.向NaHCO3固体中滴加饱和硼酸溶液,有气泡产生 |
| C.加入MgO的目的是调节溶液的pH,使杂质离子转化为Fe(OH)3、Al(OH)3沉淀 |
| D.已知浓缩滤液时MgSO4和H3BO3接近饱和;将滤液浓缩蒸发结晶,得到硫酸镁晶体,趁热过滤,再将母液降温结晶,分离得到硼酸晶体 |
您最近一年使用:0次
4 . 化学实验离不开实验装置,下列说法不正确 的是

A.利用图1所示装置证明 极易溶于水 极易溶于水 |
| B.利用图2所示装置证明化学能可转化为电能 |
| C.利用图3所示装置蒸馏石油,所得煤油中可能混入柴油 |
| D.利用图4所示装置测定电石纯度(其它操作均正确),测定结果偏高 |
您最近一年使用:0次
名校
5 . 茴香油是淡黄色液体或晶体,难溶于水,易溶于有机溶剂,在水蒸气作用下易挥发,某茴香油主要成分是含有酯基的芳香族化合物。实验室提取该茴香油的流程如下:

| A.操作A是利用沸点差异进行分离 |
| B.水蒸气蒸馏和减压蒸馏的原理相同 |
C.有机层加入的无水 可用碱石灰代替 可用碱石灰代替 |
| D.馏出液加NaCl至饱和可以提高茴香油的提取率 |
您最近一年使用:0次
7日内更新
|
44次组卷
|
2卷引用:浙江省杭州市学军中学2023-2024学年高三下学期5月阶段性考试
名校
解题方法
6 . 如图所示可以分离并回收废旧芯片中的几种贵金属。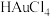 是一种强酸:②
是一种强酸:② 难溶。
难溶。
请回答:
(1)含金固体可溶于 和NaCl的混合溶液,写出反应的离子方程式:
和NaCl的混合溶液,写出反应的离子方程式:______ 。常温时 在碱性条件下能还原Z,写出反应的化学方程式:
在碱性条件下能还原Z,写出反应的化学方程式:______ 。
(2)金的分离还可以加王水,银钯的分离可重复利用某些溶液。
①下列说法正确的是______ 。
A.芯片中的金是芯片连接的绝佳材料,只是利用其物理性质
B.溶液X可以是NaCl溶液
C.配位能力:
D. 不直接还原固体Y可能的原因是得到的Ag纯度更高
不直接还原固体Y可能的原因是得到的Ag纯度更高
②加入盐酸,调pH≈1能将 转化为
转化为 ,解释其原因
,解释其原因______ 。
(3)溶液Z中加NaCl溶液是否有沉淀?______ (填“有”或“没有”)。设计实验验证溶液Z中银元素的存在______ 。
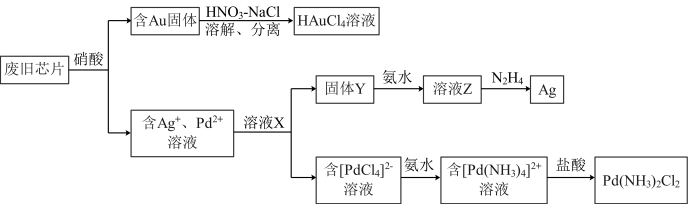
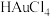 是一种强酸:②
是一种强酸:② 难溶。
难溶。请回答:
(1)含金固体可溶于
 和NaCl的混合溶液,写出反应的离子方程式:
和NaCl的混合溶液,写出反应的离子方程式: 在碱性条件下能还原Z,写出反应的化学方程式:
在碱性条件下能还原Z,写出反应的化学方程式:(2)金的分离还可以加王水,银钯的分离可重复利用某些溶液。
①下列说法正确的是
A.芯片中的金是芯片连接的绝佳材料,只是利用其物理性质
B.溶液X可以是NaCl溶液
C.配位能力:

D.
 不直接还原固体Y可能的原因是得到的Ag纯度更高
不直接还原固体Y可能的原因是得到的Ag纯度更高②加入盐酸,调pH≈1能将
 转化为
转化为 ,解释其原因
,解释其原因(3)溶液Z中加NaCl溶液是否有沉淀?
您最近一年使用:0次
7 . 按以下实验方案可从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物:

| A | B |
|
|
| 步骤① | 步骤② |
| C | D |
|
|
| 步骤③ | 步骤④ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 为了自制肥皂,某化学兴趣小组设计方案如下所示,下列说法不正确 的是

| A.步骤Ⅰ中,试剂Ⅰ可以为乙醇,作用是提供均相溶剂 |
| B.用玻璃棒蘸取混合液A,滴入装有冷水的试管中,观察有无滴浮在液面上来判断油脂是否水解完全 |
| C.步骤Ⅱ中,试剂Ⅱ为饱和食盐水,目的是降低高级脂肪酸钠盐溶解度,使其析出 |
| D.步骤Ⅲ中,可用多组纱布进行过滤操作 |
您最近一年使用:0次
名校
解题方法
9 . 根据下列实验操作和现象得出的结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 除去苯酚中混有的苯 | 加适量的NaOH溶液分液,向水层通入足量 过滤 过滤 |
| B | 向氯水中加入一定量铁粉,充分振荡后滴加几滴KSCN溶液,溶液呈浅绿色 | 该氯水为久置氯水 |
| C | 向浓度均为0.1mol/L的 、 、 混合溶液中逐滴加入NaOH溶液,先出现蓝色沉淀 混合溶液中逐滴加入NaOH溶液,先出现蓝色沉淀 | 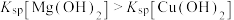 |
| D | 向某无色溶液中加入稀盐酸,将产生的气体通入澄清石灰水中,澄清石灰水变浑浊 | 原溶液中一定含有 或 或 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 某工厂废水中含有大量的FeSO4和较多的CuSO4。为制备晶体X并检验其部分性质,按如图流程进行相关实验:
②晶体X是一种含结晶水的化合物,制备X时加入的(NH4)2SO4与FeSO4溶液中溶质的物质的量相等。
(1)在制备晶体X的过程中,会使用少量酒精来洗涤晶体。其目的是_______ 。
(2)取少量铜粉加入浓盐酸中加热,铜粉溶解并生成H3[CuCl4],写出化学方程式_______ 。
(3)下列说法不正确 的是_______ (填字母)。
(4)取少量略变黄的绿矾溶于稀硫酸,请设计实验验证溶液中铁元素的存在形式_______ ;写出实验过程中所涉及的反应方程式_______ 。

②晶体X是一种含结晶水的化合物,制备X时加入的(NH4)2SO4与FeSO4溶液中溶质的物质的量相等。
(1)在制备晶体X的过程中,会使用少量酒精来洗涤晶体。其目的是
(2)取少量铜粉加入浓盐酸中加热,铜粉溶解并生成H3[CuCl4],写出化学方程式
(3)下列说法
| A.测得晶体X分子量为392,则其化学式可能为(NH4)2Fe(SO4)2•6H2O |
| B.晶体X中不含Fe3+,故不可以作净水剂和消毒剂 |
| C.晶体X比绿矾稳定的原因是(NH4)2SO4包裹在FeSO4外部,隔绝空气,防止Fe2+被氧化 |
| D.结合流程图信息,测定待测KMnO4溶液浓度时,用晶体X配标准液去滴定比绿矾误差更小 |
(4)取少量略变黄的绿矾溶于稀硫酸,请设计实验验证溶液中铁元素的存在形式
您最近一年使用:0次







