名校
解题方法
1 . 实验是探究化学过程的重要途径。用下列实验装置进行实验,能达到相应实验目的的是
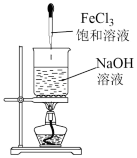 | 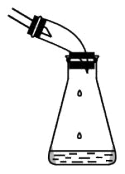 | 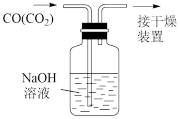 | 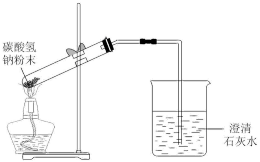 |
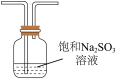
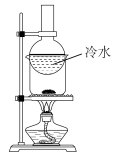
| A.制备Fe(OH)3胶体 | B.工业酒精加入生石灰蒸馏,提纯乙醇 | C.除去CO中的CO2 | D.检验碳酸氢钠受热分解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-02-17更新
|
557次组卷
|
3卷引用:重庆育才中学2021-2022高三下学期入学考试化学试题
重庆育才中学2021-2022高三下学期入学考试化学试题(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(天津专用)新疆乌鲁木齐市第十二中学2023-2024学年高三下学期2月月考化学试题
名校
解题方法
2 . 已知钴在加热时易被氧化,CoCl2易潮解,实验室制备CoCl2的装置示意图如图所示(加热装置略):
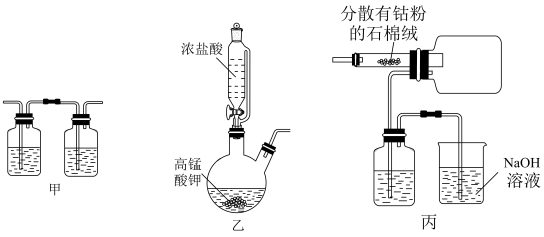
下列说法错误的是

下列说法错误的是
| A.装置乙中,盛装反应物原料的是滴液漏斗和双口烧瓶 |
| B.先加热装有石棉绒的硬质玻璃管,再滴加浓盐酸 |
| C.石棉绒的作用是增大反应接触面积 |
| D.3个洗气瓶中所盛装的试剂有2种 |
您最近一年使用:0次
名校
解题方法
3 . 下列除杂试剂选用正确且除杂过程涉及氧化还原的是
括号内为杂质 | 除杂试剂 | |
A |
| 铜粉 |
B |
|
|
C |
| 饱和 |
D |
| 酸性高锰酸钾溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-09更新
|
237次组卷
|
2卷引用:重庆市第七中学校2023-2024学年高一下学期第一次月考化学试卷
4 . 下列实验装置及试剂的使用正确,且能达到实验目的的是
|
|
|
|
| A.除去SO2中的HCl | B.制备氢氧化铁胶体 | C.分离乙酸乙酯和乙醇 | D.分离NH4Cl(s)和NaCl(s) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
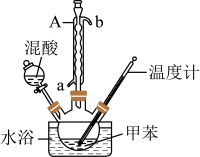
5 . 一硝基甲苯是一种重要的工业原料,某化学学习小组设计如图所示装置(夹持及搅拌装置已略去)制备一硝基甲苯,实验步骤如下:
①配制浓硫酸和浓硝酸的混合物(混酸,足量);
②在三颈烧瓶中加入15mL甲苯(密度为0.866g•cm-3);
③装好其他试剂,并组装好仪器;
④向三颈烧瓶中加入混酸,并不断搅拌;
⑤控制温度,反应大约10min至三颈烧瓶底部有大量液体(淡黄色油状)出现;
⑥分离出一硝基甲苯,经提纯最终得到一硝基甲苯12.5g。
(1)仪器A的名称是______ ,作用是______ 。
(2)本实验的关键是控制温度在30℃左右,如果温度过高,可能会产生_____ (填一种物质的名称)等副产物。写出甲苯与混酸反应生成2,4,6-三硝基甲苯的化学方程式:______ 。
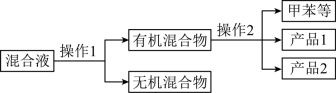
分离产品的方案如图:______ ,操作2的名称是______ 。
(4)经测定产品2的核磁共振氢谱中有3组峰,则产品2的结构简式为______ 。
(5)本实验中一硝基甲苯的产率为______ (结果保留三位有效数字)。
①配制浓硫酸和浓硝酸的混合物(混酸,足量);
②在三颈烧瓶中加入15mL甲苯(密度为0.866g•cm-3);
③装好其他试剂,并组装好仪器;
④向三颈烧瓶中加入混酸,并不断搅拌;
⑤控制温度,反应大约10min至三颈烧瓶底部有大量液体(淡黄色油状)出现;
⑥分离出一硝基甲苯,经提纯最终得到一硝基甲苯12.5g。
(1)仪器A的名称是
(2)本实验的关键是控制温度在30℃左右,如果温度过高,可能会产生
分离产品的方案如图:
(4)经测定产品2的核磁共振氢谱中有3组峰,则产品2的结构简式为
(5)本实验中一硝基甲苯的产率为
您最近一年使用:0次
2023-04-22更新
|
220次组卷
|
7卷引用:重庆市名校联盟2021-2022学年高二下学期5月大联考化学试题
名校
解题方法
6 . 我国首艘使用了钛合金材料的国产航母已成功下水,钛(Ti)常温下与酸、碱均不反应,但高温下能被空气氧化,由钛铁矿(主要成分是FeO和TiO2)提取金属钛的主要工艺流程如图。下列说法错误的是
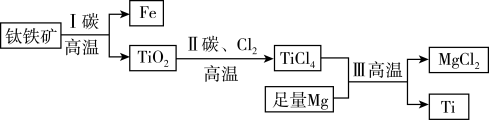
| A.步骤Ⅰ、II中均发生氧化还原反应 |
| B.步骤Ⅰ、Ⅱ中碳元素的化合价均升高 |
| C.步骤Ⅲ中反应可在氩气环境中进行,也可在空气中进行 |
| D.可用稀硫酸除去金属钛中的少量镁杂质 |
您最近一年使用:0次
2020-12-09更新
|
1025次组卷
|
13卷引用:重庆市西南大学附属中学校2021-2022学年高一上学期第一次定时训练(广延班)化学试题
重庆市西南大学附属中学校2021-2022学年高一上学期第一次定时训练(广延班)化学试题福建省泉州市安溪一中、养正中学、惠安一中、泉州实验中学2020-2021学年高一上学期期中联考化学试题吉林省长春外国语学校2020-2021学年高一上学期期末考试化学试题广东省汕头市金山中学2020-2021学年高一上学期期末考试化学试题安徽省芜湖市安庆市2020-2021学年高一上学期期末教学质量监控化学试题辽宁省庄河市高级中学2020-2021学年高一下学期期初考试化学试题四川省成都外国语学校2020-2021学年高一4月月考化学试题安徽省涡阳一中2020-2021年高一上学期期末考试化学试题广东省广州市广外附设外语学校2021-2022学年高一上学期12月月考化学试题福建省永春第一中学2021-2022学年高一上学期期中考试化学试题作业(十九) 常见的合金及其应用福建省福州市六校2023-2024学年高一上学期期中联考化学试题广东省广州市第六中学2023-2024学年高一上学期期末考试化学试题
名校
7 . 除去下列溶液中的杂质 括号内为杂质
括号内为杂质 所用的试剂或方法不正确的是
所用的试剂或方法不正确的是
 括号内为杂质
括号内为杂质 所用的试剂或方法不正确的是
所用的试剂或方法不正确的是A. 溶液【 溶液【 】:通入氯气 】:通入氯气 |
B. 溶液【 溶液【 】:用 】:用 溶液 溶液 |
C. 固体【 固体【 】:加热 】:加热 |
D.铁粉【铝粉】:用 溶液 溶液 |
您最近一年使用:0次
2023-07-30更新
|
225次组卷
|
4卷引用:重庆市2022-2023学年高一上学期期末考试化学试题
重庆市2022-2023学年高一上学期期末考试化学试题(已下线)【精品卷】3.1.2 铁的重要化合物课堂例题-人教版2023-2024学年必修第一册四川省成都市郫都区2023-2024学年高一上学期期末模拟化学试题四川省自贡市蜀光中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
8 . 硅是带来人类文明的重要元素之一,硅与二氧化硅广泛应用于通讯行业。
(1)工业上常用石英砂与焦炭在高温下反应制粗硅,其化学方程式是___________ 。
(2)工业上可以通过如图所示的流程制取纯硅:___________ 。
②整个过程中必须严格控制无氧。在有氧环境下,除了有不安全因素外还可能使产品中混有杂质___________ 。整个过程中可以循环利用的物质是___________ (填化学式)。
(3)如图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。___________ 。
②将洗净的石英砂研磨成粉末,目的是___________ 。
③在以上流程中,能否将盐酸改为NaOH溶液,请说明理由___________ 。
(1)工业上常用石英砂与焦炭在高温下反应制粗硅,其化学方程式是
(2)工业上可以通过如图所示的流程制取纯硅:
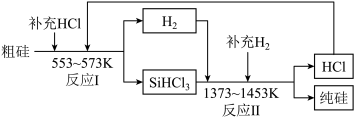
②整个过程中必须严格控制无氧。在有氧环境下,除了有不安全因素外还可能使产品中混有杂质
(3)如图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。
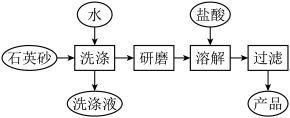
②将洗净的石英砂研磨成粉末,目的是
③在以上流程中,能否将盐酸改为NaOH溶液,请说明理由
您最近一年使用:0次
2023-07-06更新
|
234次组卷
|
5卷引用:重庆市朝阳中学2023-2024学年高一下学期期中考试化学试题
名校
解题方法
9 . 为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂正确的是
| 选项 | 被提纯的物质 | 除杂试剂 |
| A |  |  |
| B |  |  |
| C | 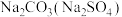 |  |
| D | 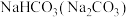 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-05更新
|
207次组卷
|
2卷引用:重庆市西南大学附属中学2022-2023学年高一上学期期中考试化学试题
名校
10 . 以绿茶为主要原料合成生物炭负载纳米铁(CT-FeNPs/BC)
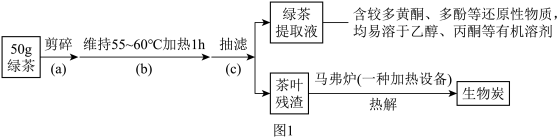
步骤1:绿茶提取液及生物炭的制备。按如图1流程实验:
 溶液和生物炭。
溶液和生物炭。
②通一段时间 后,将绿茶提取液以2mL·
后,将绿茶提取液以2mL·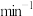 的速度全部滴入三颈烧瓶中,持续磁力搅拌1h,得黑色悬浊液。
的速度全部滴入三颈烧瓶中,持续磁力搅拌1h,得黑色悬浊液。
③离心分离,依次用乙醇和蒸馏水洗涤,真空干燥,产品密封备用。
回答下列问题:
(1)操作(b)中,应采用___________ 进行加热。
(2)图2中,盛装绿茶提取液的仪器名称为___________ ,加入绿茶提取液的目的是___________ 。
(3)离心分离后,用乙醇洗涤的作用是___________ 。
(4)判断产品洗涤干净的实验操作为___________ 。
(5)GT-FeNPs/BC可高效去除含铬强酸性废水中的六价铬(以 表示),反应过程如图3。
表示),反应过程如图3。 和
和 共同生成沉淀
共同生成沉淀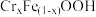 的离子方程式:
的离子方程式:___________ 。
②研究表明,GT-FeNPs/BC和 均可用于降解含
均可用于降解含 的废水。为探究两者降解效果,进行了如下实验,相同时间内得到如下实验结果:
的废水。为探究两者降解效果,进行了如下实验,相同时间内得到如下实验结果:
结合图3分析,实验3降解 效率显著增大的原因是
效率显著增大的原因是___________ 。
步骤1:绿茶提取液及生物炭的制备。按如图1流程实验:


 溶液和生物炭。
溶液和生物炭。②通一段时间
 后,将绿茶提取液以2mL·
后,将绿茶提取液以2mL·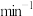 的速度全部滴入三颈烧瓶中,持续磁力搅拌1h,得黑色悬浊液。
的速度全部滴入三颈烧瓶中,持续磁力搅拌1h,得黑色悬浊液。③离心分离,依次用乙醇和蒸馏水洗涤,真空干燥,产品密封备用。
回答下列问题:
(1)操作(b)中,应采用
(2)图2中,盛装绿茶提取液的仪器名称为
(3)离心分离后,用乙醇洗涤的作用是
(4)判断产品洗涤干净的实验操作为
(5)GT-FeNPs/BC可高效去除含铬强酸性废水中的六价铬(以
 表示),反应过程如图3。
表示),反应过程如图3。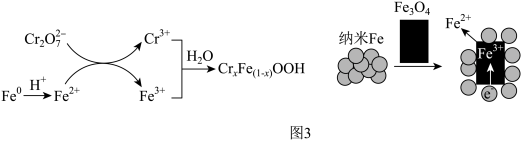
 和
和 共同生成沉淀
共同生成沉淀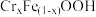 的离子方程式:
的离子方程式:②研究表明,GT-FeNPs/BC和
 均可用于降解含
均可用于降解含 的废水。为探究两者降解效果,进行了如下实验,相同时间内得到如下实验结果:
的废水。为探究两者降解效果,进行了如下实验,相同时间内得到如下实验结果:| 实验编号 | GT-FeNPs/BC(g/L) |  (g/L) (g/L) |  实际降解率 实际降解率 |
| 1 | 0.05 | 0 | 51.4% |
| 2 | 0 | 2 | 7.12% |
| 3 | 0.05 | 2 | 86.67% |
 效率显著增大的原因是
效率显著增大的原因是
您最近一年使用:0次

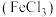
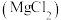

 溶液
溶液