解题方法
1 . I.通过海水晾晒可得粗盐,粗盐中除NaCl外,还含有 、
、 、
、 以及泥沙等杂质,为了将粗盐有效提纯,实验的各步操作流程如下:
以及泥沙等杂质,为了将粗盐有效提纯,实验的各步操作流程如下:______ (填名称)。
(2)操作溶解、过滤、蒸发都用到一种玻璃仪器是______ (填仪器名称),
(3)试剂a由三种试剂构成,除杂步骤中试剂可行的添加顺序有______(填标号)。
Ⅱ.某研究小组利用提纯后精盐配制饱和NaCl溶液,模拟侯德榜制碱法制取碱,流程如图:
(4)装置Ⅰ中,往饱和食盐水中优先通入的气体为______ (填化学式),装置Ⅰ中反应的化学方程式为____________ ;
(5)该流程中可循环利用的物质是______ (填化学式)
 、
、 、
、 以及泥沙等杂质,为了将粗盐有效提纯,实验的各步操作流程如下:
以及泥沙等杂质,为了将粗盐有效提纯,实验的各步操作流程如下:
(2)操作溶解、过滤、蒸发都用到一种玻璃仪器是
(3)试剂a由三种试剂构成,除杂步骤中试剂可行的添加顺序有______(填标号)。
A.① ② ② ③NaOH ③NaOH | B.① ②NaOH③ ②NaOH③ |
C.①NaOH② ③ ③ | D.① ② ② ③NaOH ③NaOH |
Ⅱ.某研究小组利用提纯后精盐配制饱和NaCl溶液,模拟侯德榜制碱法制取碱,流程如图:

| 物质 | NaCl |  |  |  |
| 溶解度 | 36.0 | 21.7 | 9.6 | 37.2 |
(4)装置Ⅰ中,往饱和食盐水中优先通入的气体为
(5)该流程中可循环利用的物质是
您最近一年使用:0次
名校
2 . 从某含有 、
、 、
、 的工业废液中回收铜并制备氯化铁晶体(
的工业废液中回收铜并制备氯化铁晶体( )的流程如下。下列说法正确的是
)的流程如下。下列说法正确的是

 、
、 、
、 的工业废液中回收铜并制备氯化铁晶体(
的工业废液中回收铜并制备氯化铁晶体( )的流程如下。下列说法正确的是
)的流程如下。下列说法正确的是
A.用酸性 溶液可检验溶液W中是否含有 溶液可检验溶液W中是否含有 |
| B.试剂a、b分别是铁粉和稀硫酸 |
C.加入试剂a过程中,有红色固体析出后,说明溶液中 已经反应完全 已经反应完全 |
| D.若操作Ⅱ前后固体质量减少28 g,则理论上该步骤应产生11.2 L气体 |
您最近一年使用:0次
2024-01-05更新
|
533次组卷
|
4卷引用:广东省东莞市东莞中学松山湖学校2023-2024学年高一上学期期中考试化学试卷
广东省东莞市东莞中学松山湖学校2023-2024学年高一上学期期中考试化学试卷广东省云浮市罗定中学2023-2024学年高一上学期12月月考化学试题(已下线)寒假作业07 铁及其化合物-【寒假分层作业】2024年高一化学寒假培优练(人教版2019必修第一册)广西钦州市第四中学2023-2024学年高一上学期11月考试化学试卷
3 . 我国制碱工业先驱侯德榜发明了侯氏制碱法。其模拟流程如图:

已知常温常压下,1体积水约可溶解700体积 ,1体积水约可溶解1.7体积
,1体积水约可溶解1.7体积 。
。
回答下列问题:
(1) 俗名为小苏打,写出其在生活中的一种用途:
俗名为小苏打,写出其在生活中的一种用途:___________ 。其焰色试验的颜色为___________ 色。
(2)食盐水中通入气体,要先通入___________ (填“ ”或“
”或“ ”)。
”)。
(3)进行操作a名称为___________ 。
(4)写出反应2的化学方程式为___________ 。
(5)工业生产的纯碱通常含有少量氯化钠,如何检验?___________ 。
(6)已知合成氨的反应为 ,当生成
,当生成 氨气时(标况条件下),被氧化的物质的质量为
氨气时(标况条件下),被氧化的物质的质量为___________ g。

已知常温常压下,1体积水约可溶解700体积
 ,1体积水约可溶解1.7体积
,1体积水约可溶解1.7体积 。
。回答下列问题:
(1)
 俗名为小苏打,写出其在生活中的一种用途:
俗名为小苏打,写出其在生活中的一种用途:(2)食盐水中通入气体,要先通入
 ”或“
”或“ ”)。
”)。(3)进行操作a名称为
(4)写出反应2的化学方程式为
(5)工业生产的纯碱通常含有少量氯化钠,如何检验?
(6)已知合成氨的反应为
 ,当生成
,当生成 氨气时(标况条件下),被氧化的物质的质量为
氨气时(标况条件下),被氧化的物质的质量为
您最近一年使用:0次
4 . 海带中含有碘元素,从海带中提取碘的实验过程如下所示。
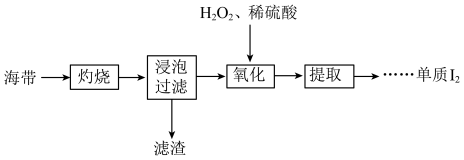
(1)“灼烧”时用到下列仪器中的___________。
(2)“浸泡过滤”后滤液中含有I-,“氧化”的离子方程式为___________ 。
(3)检验“氧化”产生I2的操作:取“氧化”后的少量溶液于试管中,___________ (实验操作及现象)。
(4)“提取”存在以下两种方案。
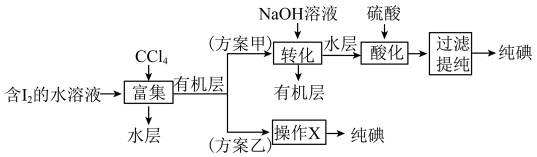
已知: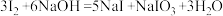 ;酸性条件下,I2在水溶液中的溶解度很小。
;酸性条件下,I2在水溶液中的溶解度很小。
①方案乙中“操作X”的名称是___________ 。
②方案甲中,“酸化”步骤氧化剂与还原剂物质的量之比为___________ 。
③该流程可循环利用的物质是___________ 。
④采用方案乙得到纯碘的产率较低,原因是___________ 。

(1)“灼烧”时用到下列仪器中的___________。
| A.酒精灯 | B.漏斗 | C.蒸发皿 | D.坩埚 |
(3)检验“氧化”产生I2的操作:取“氧化”后的少量溶液于试管中,
(4)“提取”存在以下两种方案。

已知:
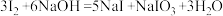 ;酸性条件下,I2在水溶液中的溶解度很小。
;酸性条件下,I2在水溶液中的溶解度很小。①方案乙中“操作X”的名称是
②方案甲中,“酸化”步骤氧化剂与还原剂物质的量之比为
③该流程可循环利用的物质是
④采用方案乙得到纯碘的产率较低,原因是
您最近一年使用:0次
名校
解题方法
5 . 某工厂以镍废渣(主要成分为Ni,含少量Fe、Fe3O4、Al2O3等)为原料制备翠矾(NiSO4·7H2O),其生产工艺如图。

(1)“碱浸”时发生反应的离子方程式为_______ 。
(2)实验室进行操作1需要用的玻璃仪器除了烧杯还有_______ 。
(3)通入空气氧化的目的是_______ ,也可以用一种绿色氧化剂代替空气中的氧气,写出该反应的离子方程式_______ 。
(4)滤渣B的成分是_______ (填化学式)。
(5)系列操作是将溶液经过_______ 、_______ 、过滤、洗涤、干燥得到NiSO4·7H2O晶体。
(6)NiSO4在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式_______ 。

(1)“碱浸”时发生反应的离子方程式为
(2)实验室进行操作1需要用的玻璃仪器除了烧杯还有
(3)通入空气氧化的目的是
(4)滤渣B的成分是
(5)系列操作是将溶液经过
(6)NiSO4在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
您最近一年使用:0次
名校
6 . 工业上采用 与
与 在350℃左右反应生成
在350℃左右反应生成 ,之后将其还原、结晶得到高纯度的单晶硅产品。已知
,之后将其还原、结晶得到高纯度的单晶硅产品。已知 的熔点为
的熔点为 ℃,沸点为33℃,且遇
℃,沸点为33℃,且遇 和
和 均剧烈反应。现要在实验室中制取少量
均剧烈反应。现要在实验室中制取少量 ,其实验装置如下图所示,则下列说法正确的是
,其实验装置如下图所示,则下列说法正确的是
 与
与 在350℃左右反应生成
在350℃左右反应生成 ,之后将其还原、结晶得到高纯度的单晶硅产品。已知
,之后将其还原、结晶得到高纯度的单晶硅产品。已知 的熔点为
的熔点为 ℃,沸点为33℃,且遇
℃,沸点为33℃,且遇 和
和 均剧烈反应。现要在实验室中制取少量
均剧烈反应。现要在实验室中制取少量 ,其实验装置如下图所示,则下列说法正确的是
,其实验装置如下图所示,则下列说法正确的是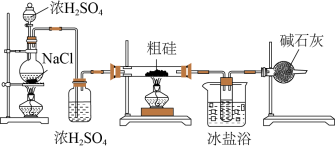
| A.反应时,应该先点燃“粗硅”处的酒精灯 |
B.使用浓 和 和 混合加热制取 混合加热制取 利用了浓 利用了浓 的脱水性和强酸性 的脱水性和强酸性 |
C.冰盐浴的目的为降低收集容器的温度,使 冷凝为液体 冷凝为液体 |
D.可以用无水 替换干燥管中的碱石灰 替换干燥管中的碱石灰 |
您最近一年使用:0次
2023-03-30更新
|
679次组卷
|
7卷引用:广东省东莞实验中学2022-2023学年高一下学期期中考试化学试题
解题方法
7 . 我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下(部分物质已略去)。

已知:氨气极易溶于水,无水氯化钙可与 反应生成固体
反应生成固体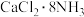 。
。
(1)写出过程①的化学方程式_______ 。原料有两种气体,应先通入_______ (填“ ”或“
”或“ ”),原因是
”),原因是_______ 。
(2)某同学用如图装置模拟工业过程①。实验时,须从_______ 管通入 (填“a”或“b”),装置c的作用是
(填“a”或“b”),装置c的作用是_______ 。

(3)若在实验室进行过裎③,实验操作的名称是_______ 。
(4)侯氏制碱法工业生产过程中,可循环利用的物质是_______ 、_______ 。

已知:氨气极易溶于水,无水氯化钙可与
 反应生成固体
反应生成固体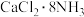 。
。(1)写出过程①的化学方程式
 ”或“
”或“ ”),原因是
”),原因是(2)某同学用如图装置模拟工业过程①。实验时,须从
 (填“a”或“b”),装置c的作用是
(填“a”或“b”),装置c的作用是
(3)若在实验室进行过裎③,实验操作的名称是
(4)侯氏制碱法工业生产过程中,可循环利用的物质是
您最近一年使用:0次
2023-01-10更新
|
574次组卷
|
2卷引用:广东省东莞市2022-2023学年高一上学期期末考试化学试题
解题方法
8 . 实验室可由软锰矿(主要成分为 )制备
)制备 方法如下:
方法如下:

下列说法不正确的是
 )制备
)制备 方法如下:
方法如下:
下列说法不正确的是
A.软锰矿制锰酸钾时, 发生反应转移电子 发生反应转移电子 |
| B.实验室进行“操作1”时,玻璃棒的作用主要是引流 |
C.锰酸钾酸化过程氧化剂和还原剂的物质的量之比为 |
| D.不能用盐酸酸化高锰酸钾溶液 |
您最近一年使用:0次
2023-01-10更新
|
301次组卷
|
3卷引用:广东省东莞市2022-2023学年高一上学期期末考试化学试题
名校
9 . 侯德榜先生是我国近代著名的化学家,他提出的联合制碱法得到世界各国的认可,主要化学反应为:NaCl+NH3+H2O+CO2=NaHCO3↓+NH4Cl。工业流程如图,下列说法正确的是
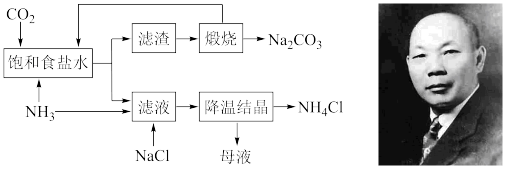

| A.应该向“饱和食盐水”中先通入足量NH3,再通入过量CO2 |
| B.该工艺流程中发生了复分解反应、分解反应、氧化还原反应 |
| C.滤渣主要成分是Na2CO3,在相同温度下碳酸氢钠溶解度比碳酸钠大 |
| D.最终所得“母液”不可循环利用 |
您最近一年使用:0次
2022-02-24更新
|
640次组卷
|
8卷引用:广东省东莞市东华高级中学2021-2022学年高一上学期期末考试化学试题
广东省东莞市东华高级中学2021-2022学年高一上学期期末考试化学试题河南省信阳高级中学2021-2022学年高一下学期第一次月考化学试题(已下线)【期末复习】必刷题(1)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)广东省广州市南武中学2022-2023学年高一上学期线上综合测试(二)化学试题广东省广州市海珠外国语实验中学2022-2023学年高一上学期第二次月考化学试题广东省广州市实验外语学校2022-2023学年高一上学期期末测试化学试题陕西省西安中学2023-2024学年高一上学期期中考试化学试题广东省江门市广雅中学2023-2024学年高一上学期12月月考化学试题B卷
名校
10 . 我国化学家侯德榜创立了著名的“侯氏制碱法”,实验室模拟流程简图如下。下列说法正确的是


| A.实验室可用无水氯化钙和浓氨水制备氨气 |
B.反应①的离子方程式: |
C.母液中的溶质只有 ,可直接用作氮肥 ,可直接用作氮肥 |
| D.操作1是过滤;操作2用到的主要仪器有蒸发皿酒精灯、玻璃棒等 |
您最近一年使用:0次
2021-11-11更新
|
275次组卷
|
2卷引用:广东省东莞市东华高级中学2021-2022学年高一上学期中段考试化学试题



