解题方法
1 . 实验台上摆放了六瓶液体试剂(如下图所示)。
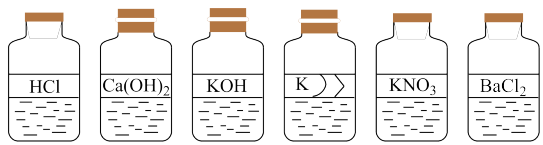
(1)上图的第4瓶的标签破损了。从物质类别上判断,这瓶试剂可能是___ 。
A.酸 B.碱 C.盐 D. 氧化物
(2)小明用pH试纸测试此试剂的酸碱度。正确的操作应该是:在白瓷板或玻璃片上放一小片pH试纸,将被测液滴到试纸上,______ ,即可得出被测液的pH,实验测得此试剂的pH值为10。
(3)小俊利用上图试剂鉴别出这瓶试剂是K2CO3溶液。请按小俊的做法,填写实验报告。

(1)上图的第4瓶的标签破损了。从物质类别上判断,这瓶试剂可能是
A.酸 B.碱 C.盐 D. 氧化物
(2)小明用pH试纸测试此试剂的酸碱度。正确的操作应该是:在白瓷板或玻璃片上放一小片pH试纸,将被测液滴到试纸上,
(3)小俊利用上图试剂鉴别出这瓶试剂是K2CO3溶液。请按小俊的做法,填写实验报告。
操作步骤 | 实验现象 | 结论及化学方程式 |
| 结论: 化学方程式: |
您最近一年使用:0次
解题方法
2 . 下列实验现象预测正确的是
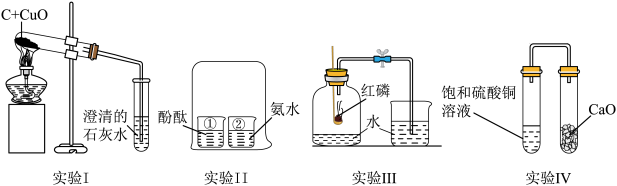

| A.实验I:加热后,试管中的粉末逐渐变成黑色 |
| B.实验II:放置一段时间后,②号烧杯中的液体呈红色 |
| C.实验III:红磷熄灭后打开止水夹,水面上升,浸没燃烧匙 |
| D.实验IV:放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
您最近一年使用:0次
3 . 某化学小组利用如图所示装置比较浓、稀硝酸氧化性的强弱。
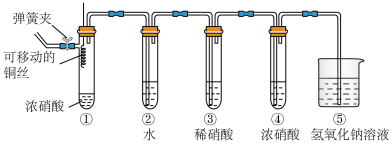
实验步骤如下:
Ⅰ.连接好装置,并检查装置的气密性;
Ⅱ.加入相应试剂,关闭弹簧夹,打开试管①,向其中加入适量的 粉末,立即盖上橡皮塞;
粉末,立即盖上橡皮塞;
Ⅲ.将铜丝伸入浓硝酸中,观察现象;
Ⅳ.将铜丝提起,打开弹簧夹,再向装置①中通入一定量的CO2气体……
回答下列问题:
(1)检查该装置气密性的方法为____________________________________________________________ 。
(2)加入少量 粉末的作用为
粉末的作用为________________________ ;通入一定量的CO2气体的作用为________________________ 。
(3)将铜丝伸入浓硝酸中,立即观察到试管①中有红棕色气体生成,发生反应的化学方程式为_________________________ ;红棕色气体进入试管②中后变成无色,发生反应的化学方程式为______________________________ ,试管③液面上方无红棕色气体出现,试管④液面上方产生红棕色气体同时溶液出现黄色,则试管④中发生反应的化学方程式为______________________________ ,说明浓硝酸的氧化性强于稀硝酸。
(4)NO2与氢氧化钠溶液反应生成两种盐,其离子方程式为______________________________ 。

实验步骤如下:
Ⅰ.连接好装置,并检查装置的气密性;
Ⅱ.加入相应试剂,关闭弹簧夹,打开试管①,向其中加入适量的
 粉末,立即盖上橡皮塞;
粉末,立即盖上橡皮塞;Ⅲ.将铜丝伸入浓硝酸中,观察现象;
Ⅳ.将铜丝提起,打开弹簧夹,再向装置①中通入一定量的CO2气体……
回答下列问题:
(1)检查该装置气密性的方法为
(2)加入少量
 粉末的作用为
粉末的作用为(3)将铜丝伸入浓硝酸中,立即观察到试管①中有红棕色气体生成,发生反应的化学方程式为
(4)NO2与氢氧化钠溶液反应生成两种盐,其离子方程式为
您最近一年使用:0次
4 . 某同学为探究MnO2与浓盐酸的反应,用如图所示的装置进行实验。
(1)B是用来收集气体的装置,但未将导管画全,请在装置图中将导管补画完整。_________
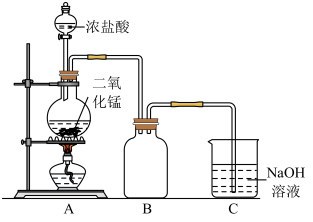
(2)制备实验开始时,先检查装置气密性,接下来的操作依次是_________ (填字母)。
A.往烧瓶中加入MnO2粉末 B.加热 C.往烧瓶中滴加浓盐酸
(3)实验中该同学取8.7g MnO2和50mL 12mol/L浓盐酸在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有固体剩余,该同学还检测到有一定量的盐酸剩余。
①MnO2与浓盐酸反应的化学方程式为_________ 。
②为什么有一定量的盐酸剩余但未能使MnO2完全溶解?_________ 。
③下列试剂中,能证明反应停止后烧瓶中有盐酸剩余的是_________ (填字母)。
A.硝酸银溶液 B.碳酸钠溶液 C.氯化钠溶液
(4)为了测定反应残余液中盐酸的浓度,该同学设计了两个实验方案:
方案一:将A中产生的气体缓缓通过已称量的装有足量NaOH溶液的洗气瓶,反应停止后再次称量,两次质量差即是Cl2的质量,据此可求剩余盐酸的量。
方案二:当MnO2与浓盐酸的反应结束后,在装置A中加入足量的锌粉,用排水法测得产生H2的体积为V L(已换算为标准状况下)。
①实际上方案一不合理,原因为_________ 。
②根据方案二,写出剩余盐酸的物质的量浓度的计算式(假设反应前后溶液的体积保持不变)_________ 。
(1)B是用来收集气体的装置,但未将导管画全,请在装置图中将导管补画完整。

(2)制备实验开始时,先检查装置气密性,接下来的操作依次是
A.往烧瓶中加入MnO2粉末 B.加热 C.往烧瓶中滴加浓盐酸
(3)实验中该同学取8.7g MnO2和50mL 12mol/L浓盐酸在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有固体剩余,该同学还检测到有一定量的盐酸剩余。
①MnO2与浓盐酸反应的化学方程式为
②为什么有一定量的盐酸剩余但未能使MnO2完全溶解?
③下列试剂中,能证明反应停止后烧瓶中有盐酸剩余的是
A.硝酸银溶液 B.碳酸钠溶液 C.氯化钠溶液
(4)为了测定反应残余液中盐酸的浓度,该同学设计了两个实验方案:
方案一:将A中产生的气体缓缓通过已称量的装有足量NaOH溶液的洗气瓶,反应停止后再次称量,两次质量差即是Cl2的质量,据此可求剩余盐酸的量。
方案二:当MnO2与浓盐酸的反应结束后,在装置A中加入足量的锌粉,用排水法测得产生H2的体积为V L(已换算为标准状况下)。
①实际上方案一不合理,原因为
②根据方案二,写出剩余盐酸的物质的量浓度的计算式(假设反应前后溶液的体积保持不变)
您最近一年使用:0次
名校
解题方法
5 . “化学多米诺实验”是只需控制第一个反应,就能使若干化学实验依次发生,如图所示。已知:①Cu2++4NH3•H2O=4H2O+[Cu(NH3)4]2+(该反应产物可作为H2O2的催化剂);②已知装置A、C中所用硫酸的浓度相同,装置B、D中所用金属锌的质量完全相同

下列说法错误的是( )

下列说法错误的是( )
| A.该实验成功的关键条件是整套装置的气密性良好 |
| B.因为形成原电池,所以装置D中生成氢气的反应速率一定大于B |
| C.导管a的作用是平衡A和B内气压 |
| D.装置H中出现浅黄色浑浊,可证明非金属性:O>S |
您最近一年使用:0次
2020-06-16更新
|
709次组卷
|
4卷引用:山西省太原市2020届高三模拟试题(二)理科综合化学试题
山西省太原市2020届高三模拟试题(二)理科综合化学试题(已下线)第26讲 化学实验基本操作及实验安全-2021年高考化学一轮复习名师精讲练安徽省淮北市第一中学 2021-2022学年高二上学期第一次月考化学试题湖南省临澧县第一中学2021-2022学年高一下学期第三次阶段性考试化学试题
6 . 实验室探究SO2性质的装置如图所示。下列说法错误的是( )


| A.装置a中的反应可用铜片和浓硫酸代替 |
| B.若X为H2S溶液,装置b中产生淡黄色沉淀 |
| C.若X为含HCl、BaCl2的FeCl3溶液,装置b中产生白色沉淀 |
| D.反应后装置c中溶液的pH降低 |
您最近一年使用:0次
2020-06-08更新
|
522次组卷
|
5卷引用:山西省太原市2021届高三上学期期末考试化学试题
7 . 84消毒液的主要成份是NaCl和NaClO。实验小组同学围绕“84消毒液能否与医用酒精发生反应”这一问题进行了如下实验。
下列推理不合理的是
| 序号 | 实验 | 现象 |
| ① | 分别取40 mL84消毒液和医用酒精混合均匀,并测量溶液温度变化 | 溶液温度由20℃升高至23℃,并产生大量气泡,略有刺激性气味,溶液颜色无明显变化 |
| ② | 分别取40 mL医用酒精和蒸馏水混合均匀,水浴至23℃ | 溶液中无明显现象 |
| ③ | 分别取40 mL84消毒液和蒸馏水混合均匀,水浴至23℃ | 溶液中无明显现象,略有刺激性气味 |
| ④ | 分别取40 mL84消毒液、40 mL医用酒精和少量白醋,混合均匀 | 产生大量气泡,有强烈地刺激性气味,溶液逐渐变为淡黄色 |
下列推理不合理的是
| A.由①②可知,①中产生的大量气泡与酒精挥发无关 |
| B.由①③可知,①中刺激性气味的产生可能与酒精无关 |
| C.由①②③可推断,84消毒液与医用酒精混合后,溶液中发生了化学反应 |
| D.由①④可推断,酸性条件有利于84消毒液与医用酒精发生反应 |
您最近一年使用:0次
2020-06-07更新
|
917次组卷
|
13卷引用:山西省晋城市第一中学2022-2023学年高一上学期第三次调研考试化学试题
山西省晋城市第一中学2022-2023学年高一上学期第三次调研考试化学试题北京市海淀区2020届高三二模化学试题(已下线)【浙江新东方】87.江苏省徐州一中、兴化中学2021届高三上学期第二次适应性考试化学试题河南省新蔡县2021届高三上学期期末调研考试化学试题(已下线)第31讲 乙醇和乙酸(精练)-2022年高考化学一轮复习讲练测(已下线)北京市第四中学2021-2022学年高一上学期期中考试化学试题福建省厦门市双十中学2022-2023学年高一上学期10月月考化学试题北京市第二十中学2022-2023学年高一上学期期中考试化学试题福建省厦门第二中学2023-2024学年高一上学期第一次月考化学试题福建省宁德第一中学2023-2024学年高一上学期10月月考化学试题北京师范大学附属中学2023-2024学年高一上学期期中考试化学试题广东省广州市真光中学2023-2024学年高一上学期12月阶段性测试化学试题
名校
解题方法
8 . 某小组同学用如图装置进行铜与浓硫酸反应时,发现试管中有黑色物质产生。同学猜测,黑色物质中可能含有CuO、Cu2S和CuS,针对产生的黑色物质,该小组同学继续进行实验探究,获得数据如表。下列说法不正确 的是
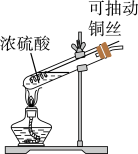
| 硫酸浓度/ mol·L﹣1 | 黑色物质出现的温度∕℃ | 黑色物质消失的温度∕℃ |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
| A.硫酸浓度越大,黑色物质越易出现、越难消失 |
| B.黑色物质消失过程中有SO2、H2S生成 |
| C.硫酸浓度为16 mol·L﹣1时,先升温至250℃以上,再将铜丝与浓硫酸接触,可以避免产生黑色物质 |
| D.取黑色物质洗涤、干燥后,加稀硫酸充分混合,固体质量不变,说明黑色物质中不含CuO |
您最近一年使用:0次
2020-06-06更新
|
388次组卷
|
3卷引用:山西省太原市第五中学2021-2022学年上学期高三第四次模块诊断化学试题
山西省太原市第五中学2021-2022学年上学期高三第四次模块诊断化学试题北京市丰台区2020届高三下学期高三综合练习(二)化学试题(已下线)北京市第四中学2023-22024学年高一下学期期中考试 化学试题
9 . SO2是中学化学中的常见气体,也是大气污染物的主要组成成分。回答下列问题:
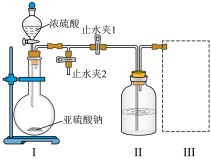
⑴甲组同学利用下列装置制备并收集干燥的 SO2:
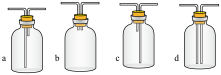
装置Ⅰ中盛装亚硫酸钠的仪器名称是_______ ,装置 II 的作用是对 SO2气体进行干燥,该装置中所盛 试剂名称为_________ ,装置 III 为集气装置,应选取填入 III 中的集气装置为___________ (选填字母代号)。
⑵乙组同学利用下列装置制备 SO2并探究其性质:
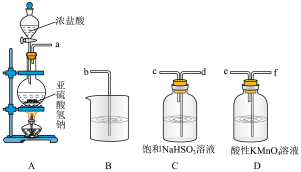
①该组同学的实验装置中,依次连接的合理顺序为a→_________ 。装置C中饱和NaHSO3溶液的作用是________ 。
②能证明SO2具有还原性的现象是___________ ,该反应的离子方程式为_________________ 。
③装置B的作用吸收SO2尾气,该装置中盛装的试剂是_______________ 。
⑶设计实验证明H2SO3为弱电解质:________________ 。

⑴甲组同学利用下列装置制备并收集干燥的 SO2:

装置Ⅰ中盛装亚硫酸钠的仪器名称是
⑵乙组同学利用下列装置制备 SO2并探究其性质:

①该组同学的实验装置中,依次连接的合理顺序为a→
②能证明SO2具有还原性的现象是
③装置B的作用吸收SO2尾气,该装置中盛装的试剂是
⑶设计实验证明H2SO3为弱电解质:
您最近一年使用:0次
名校
10 . 实验室模拟氨催化氧化法制硝酸的装置如图所示(无水CaCl2可用于吸收氨气),下列说法错误的是
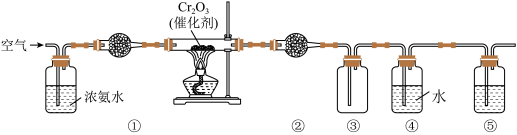

| A.装置①、②、⑤依次盛装碱石灰、无水CaCl2、NaOH溶液 |
| B.装置③中气体呈红棕色 |
| C.装置④中溶液可使紫色石蕊溶液变红,说明有HNO3生成 |
| D.通空气的主要作用是鼓出氨气,空气可用N2代替 |
您最近一年使用:0次
2020-05-02更新
|
1957次组卷
|
15卷引用:山西省晋中市现代双语学校2020-2021学年高一下学期第一次月考化学试题
山西省晋中市现代双语学校2020-2021学年高一下学期第一次月考化学试题广东省广州市2020届高三4月第一次模拟考试理综化学试题江苏省苏州市苏州中学2019-2020学年高一下学期期中考试化学试题广东省深圳市高级中学2021届高三第三次阶段性测试(10月)化学试题人教版2019必修第二册 第五章 第二节 第2课时 氨和铵盐广东省中山市第二中学2020-2021学年高一下学期第一次段考化学试题(已下线)第11周 周测卷-备战2022年高考化学周测与晚练(新高考专用)河北省实验中学2021届高三上学期第一次月考化学试题福建省长汀县第一中学2021-2022学年高三上学期第二次月考化学试题四川省宜宾市叙州区第一中学校2022届高三高考适应性考试理综化学试题黑龙江省齐齐哈尔市第八中学校2022-2023学年高一下学期3月月考化学试题江苏省苏州中学2022-2023学年高一下学期期中考试化学试题甘肃省永昌县第一高级中学2022-2023学年高一下学期期中考试化学试题02 2024年苏州昆山一中高一3月月考山东省济宁市育才中学2023-2024学年高一下学期4月月考化学试题



