1 . 某兴趣小组用下图的装置制取ICl,并用ICl的冰醋酸溶液来测定某油脂的不饱和度。油脂的不饱和度是指一个油脂分子最多可加成的氢分子数。
已知:①ICl的熔点为13.9℃,沸点为97.4℃,化学性质与氯气相似易水解;
② ,ICl3的熔点为111℃。
,ICl3的熔点为111℃。
(1)写出第一个装置中发生反应的化学方程式:___________ 。
(2)虚线框内应选用的装置是___________ (填“甲”或“乙”)。___________ (用接口的字母表示)。
(4)下列有关说法正确的是___________。
(5)用ICl的冰醋酸溶液测定某油脂的不饱和度,进行如下实验,实验过程中有关反应为:
将含有0.05mol某油脂的样品溶于CCl4后形成100mL溶液;从中取出10mL,加入20mL含有IC1物质的量为n mol的冰醋酸溶液(过量);充分反应后,加入足量KI溶液;生成的碘单质用a 的
的 标准溶液滴定;重复上述实验两次,测得滴定所需Na2S2O3的平均值为V mL。
标准溶液滴定;重复上述实验两次,测得滴定所需Na2S2O3的平均值为V mL。
①滴定前,需要将装有标准液的滴定管中的气泡排尽,应选择图中___________ 。___________ (用含a、n、V的表达式表示)。
已知:①ICl的熔点为13.9℃,沸点为97.4℃,化学性质与氯气相似易水解;
②
 ,ICl3的熔点为111℃。
,ICl3的熔点为111℃。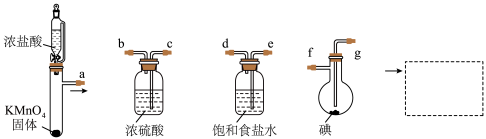
(1)写出第一个装置中发生反应的化学方程式:
(2)虚线框内应选用的装置是
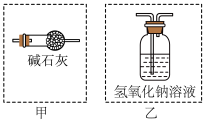
(4)下列有关说法正确的是___________。
| A.上述实验装置中的KMnO4固体也可用MnO2代替 |
| B.恒压滴液漏斗使用时应打开上面的玻璃塞 |
C.ICl与NaOH溶液反应的方程式为: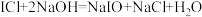 |
| D.若所制得的ICl中溶有少量ICl3杂质,可以采用蒸馏法进行提纯 |
(5)用ICl的冰醋酸溶液测定某油脂的不饱和度,进行如下实验,实验过程中有关反应为:
① ;②
;② ;③
;③
将含有0.05mol某油脂的样品溶于CCl4后形成100mL溶液;从中取出10mL,加入20mL含有IC1物质的量为n mol的冰醋酸溶液(过量);充分反应后,加入足量KI溶液;生成的碘单质用a
 的
的 标准溶液滴定;重复上述实验两次,测得滴定所需Na2S2O3的平均值为V mL。
标准溶液滴定;重复上述实验两次,测得滴定所需Na2S2O3的平均值为V mL。①滴定前,需要将装有标准液的滴定管中的气泡排尽,应选择图中
A.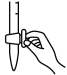 B.
B. 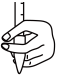 C.
C. 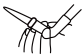 D.
D.
您最近一年使用:0次
2 . 镁及其合金是用途很广的金属材料,可以通过以下步骤从海水中提取镁。
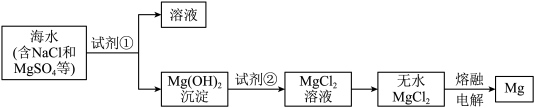
下列说法不正确 的是

下列说法
| A.试剂①可以选用石灰乳 |
B.加入试剂①后,能够分离得到 沉淀的方法是过滤 沉淀的方法是过滤 |
C. 溶液通过蒸发结晶可得到无水 溶液通过蒸发结晶可得到无水 |
D.电解熔融 所得副产物 所得副产物 是工业制备试剂②的主要原料 是工业制备试剂②的主要原料 |
您最近一年使用:0次
2024-04-18更新
|
271次组卷
|
2卷引用:浙江绍兴市2023-2024学年高三下学期选考科目适应性考试化学试题
名校
解题方法
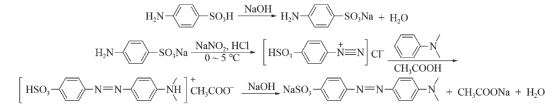
3 . 合成甲基橙( ,分子量为327,变色范围
,分子量为327,变色范围 值为
值为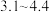 )的实验步骤如下:
)的实验步骤如下:
①在一只试管中加入 对氨基苯磺酸(分子量为173),
对氨基苯磺酸(分子量为173),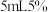 的氢氧化钠溶液,使其溶解,另加入
的氢氧化钠溶液,使其溶解,另加入 亚硝酸钠溶于
亚硝酸钠溶于 水中,加入上述反应液的溶液。在(a)冰盐浴冷却并搅拌下,将该混合液加入盛有
水中,加入上述反应液的溶液。在(a)冰盐浴冷却并搅拌下,将该混合液加入盛有 水和
水和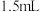 浓盐酸的烧杯中,温度始终保持在
浓盐酸的烧杯中,温度始终保持在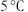 以下,直至产生白色沉淀(已知此反应大量放热)。
以下,直至产生白色沉淀(已知此反应大量放热)。
②在试管中将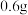 的N,N-二甲基苯胺(分子量为121)和
的N,N-二甲基苯胺(分子量为121)和 冰乙酸混合均匀。在搅拌下将该溶液滴加到冷却的重氮盐溶液中,加完后继续搅拌
冰乙酸混合均匀。在搅拌下将该溶液滴加到冷却的重氮盐溶液中,加完后继续搅拌 ,此时溶液为深红色。在搅拌下,慢慢加入
,此时溶液为深红色。在搅拌下,慢慢加入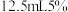 氢氧化钠溶液,此时有固体析出,(b)溶液变成橙黄色,在沸水浴加热5分钟,抽滤,依次用少量水、乙醇、乙醚洗涤。得到(c)紫色晶体,产率约
氢氧化钠溶液,此时有固体析出,(b)溶液变成橙黄色,在沸水浴加热5分钟,抽滤,依次用少量水、乙醇、乙醚洗涤。得到(c)紫色晶体,产率约 。
。
③将粗产品用0.4%的氢氧化钠水溶液进行重结晶,得到橙黄色明亮的小叶片状晶体。
上述合成实验中得到甲基橙的质量约为
 ,分子量为327,变色范围
,分子量为327,变色范围 值为
值为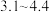 )的实验步骤如下:
)的实验步骤如下:①在一只试管中加入
 对氨基苯磺酸(分子量为173),
对氨基苯磺酸(分子量为173),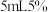 的氢氧化钠溶液,使其溶解,另加入
的氢氧化钠溶液,使其溶解,另加入 亚硝酸钠溶于
亚硝酸钠溶于 水中,加入上述反应液的溶液。在(a)冰盐浴冷却并搅拌下,将该混合液加入盛有
水中,加入上述反应液的溶液。在(a)冰盐浴冷却并搅拌下,将该混合液加入盛有 水和
水和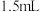 浓盐酸的烧杯中,温度始终保持在
浓盐酸的烧杯中,温度始终保持在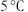 以下,直至产生白色沉淀(已知此反应大量放热)。
以下,直至产生白色沉淀(已知此反应大量放热)。②在试管中将
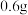 的N,N-二甲基苯胺(分子量为121)和
的N,N-二甲基苯胺(分子量为121)和 冰乙酸混合均匀。在搅拌下将该溶液滴加到冷却的重氮盐溶液中,加完后继续搅拌
冰乙酸混合均匀。在搅拌下将该溶液滴加到冷却的重氮盐溶液中,加完后继续搅拌 ,此时溶液为深红色。在搅拌下,慢慢加入
,此时溶液为深红色。在搅拌下,慢慢加入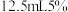 氢氧化钠溶液,此时有固体析出,(b)溶液变成橙黄色,在沸水浴加热5分钟,抽滤,依次用少量水、乙醇、乙醚洗涤。得到(c)紫色晶体,产率约
氢氧化钠溶液,此时有固体析出,(b)溶液变成橙黄色,在沸水浴加热5分钟,抽滤,依次用少量水、乙醇、乙醚洗涤。得到(c)紫色晶体,产率约 。
。③将粗产品用0.4%的氢氧化钠水溶液进行重结晶,得到橙黄色明亮的小叶片状晶体。

上述合成实验中得到甲基橙的质量约为
A. | B.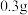 | C. | D.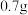 |
您最近一年使用:0次
4 . 宋应星《天工开物》载有一种矿石“银矿铅”,该矿石是与辉银矿(主要成分为 )共生的方铅矿(主要成分为
)共生的方铅矿(主要成分为 )。由于中国古代对银的需求量高,故对该矿大量开采以弥补银的短缺情况。古人在劳动过程中发现两种矿石常共生,故有“上有铅者,其下有银”(《管子·地数篇》)的说法。现利用该矿石制备铅蓄电池正极材料
)。由于中国古代对银的需求量高,故对该矿大量开采以弥补银的短缺情况。古人在劳动过程中发现两种矿石常共生,故有“上有铅者,其下有银”(《管子·地数篇》)的说法。现利用该矿石制备铅蓄电池正极材料 和超细银粉,工艺流程如下:
和超细银粉,工艺流程如下: 杂质;
杂质;
②“酸化”过程中 会与热的浓盐酸反应生成
会与热的浓盐酸反应生成 (微溶);在浓盐酸中有
(微溶);在浓盐酸中有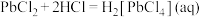 ,而
,而 与热的浓盐酸不反应,但可以与氰化物反应生成二氰合银离子;
与热的浓盐酸不反应,但可以与氰化物反应生成二氰合银离子; 和
和 可以类似的形成四氰合锌离子。
可以类似的形成四氰合锌离子。
③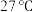 下,
下,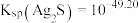 ,反应
,反应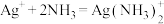 的平衡常数
的平衡常数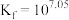 。
。
回答下列问题:
(1)浮选剂是头部为亲硫基、尾部为长烃链(憎水基)的分子,可吸引粉碎后的矿物中的含硫基团,从而完成对矿物中硫化物的富集。“浮选”步骤的目的是_______ 。
(2)“还原”步骤发生反应的离子方程式为_______ ,流程中可重复利用的物质是_______ (填化学式)。
(3)有同学认为在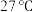 下“溶银”过程可以用浓氨水代替
下“溶银”过程可以用浓氨水代替 溶液,但经实验二者混合后无明显现象,请通过计算溶液中
溶液,但经实验二者混合后无明显现象,请通过计算溶液中 的浓度达到
的浓度达到 所需要的最小氨浓度解释其原因
所需要的最小氨浓度解释其原因_______ 。(计算结果保留指数形式,忽略 与
与 之间的转化)
之间的转化)
(4)“酸化”过程中生成的 会威胁人体健康。已知
会威胁人体健康。已知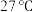 下某车间(空气体积为
下某车间(空气体积为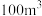 )
) 的挥发速率
的挥发速率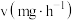 与时间
与时间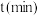 有
有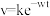 成立,式中k,w为常数。气相色谱仪测定车间
成立,式中k,w为常数。气相色谱仪测定车间 浓度结果拟合为如图所示的曲线,则
浓度结果拟合为如图所示的曲线,则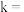
_______ , 的挥发半衰期(挥发
的挥发半衰期(挥发 的量首次达到挥发
的量首次达到挥发 总量的一半的时间)
总量的一半的时间)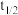
_______ (填“>”“<”“=”或“不确定”) ;
; 的最高容许浓度为
的最高容许浓度为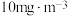 ,则该车间环境
,则该车间环境_______ (填“是”或“否”)符合国家标准。
 )共生的方铅矿(主要成分为
)共生的方铅矿(主要成分为 )。由于中国古代对银的需求量高,故对该矿大量开采以弥补银的短缺情况。古人在劳动过程中发现两种矿石常共生,故有“上有铅者,其下有银”(《管子·地数篇》)的说法。现利用该矿石制备铅蓄电池正极材料
)。由于中国古代对银的需求量高,故对该矿大量开采以弥补银的短缺情况。古人在劳动过程中发现两种矿石常共生,故有“上有铅者,其下有银”(《管子·地数篇》)的说法。现利用该矿石制备铅蓄电池正极材料 和超细银粉,工艺流程如下:
和超细银粉,工艺流程如下: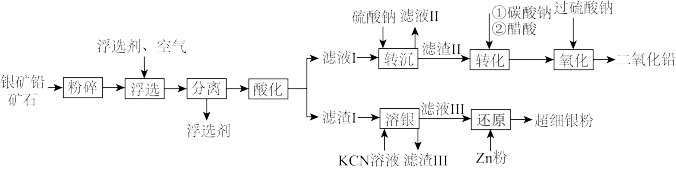
 杂质;
杂质;②“酸化”过程中
 会与热的浓盐酸反应生成
会与热的浓盐酸反应生成 (微溶);在浓盐酸中有
(微溶);在浓盐酸中有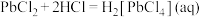 ,而
,而 与热的浓盐酸不反应,但可以与氰化物反应生成二氰合银离子;
与热的浓盐酸不反应,但可以与氰化物反应生成二氰合银离子; 和
和 可以类似的形成四氰合锌离子。
可以类似的形成四氰合锌离子。③
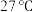 下,
下,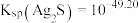 ,反应
,反应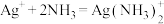 的平衡常数
的平衡常数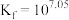 。
。回答下列问题:
(1)浮选剂是头部为亲硫基、尾部为长烃链(憎水基)的分子,可吸引粉碎后的矿物中的含硫基团,从而完成对矿物中硫化物的富集。“浮选”步骤的目的是
(2)“还原”步骤发生反应的离子方程式为
(3)有同学认为在
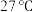 下“溶银”过程可以用浓氨水代替
下“溶银”过程可以用浓氨水代替 溶液,但经实验二者混合后无明显现象,请通过计算溶液中
溶液,但经实验二者混合后无明显现象,请通过计算溶液中 的浓度达到
的浓度达到 所需要的最小氨浓度解释其原因
所需要的最小氨浓度解释其原因 与
与 之间的转化)
之间的转化)(4)“酸化”过程中生成的
 会威胁人体健康。已知
会威胁人体健康。已知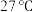 下某车间(空气体积为
下某车间(空气体积为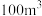 )
) 的挥发速率
的挥发速率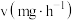 与时间
与时间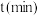 有
有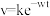 成立,式中k,w为常数。气相色谱仪测定车间
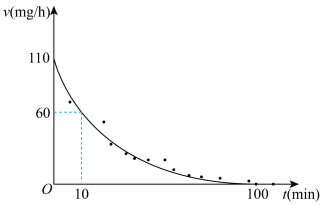
成立,式中k,w为常数。气相色谱仪测定车间 浓度结果拟合为如图所示的曲线,则
浓度结果拟合为如图所示的曲线,则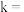
 的挥发半衰期(挥发
的挥发半衰期(挥发 的量首次达到挥发
的量首次达到挥发 总量的一半的时间)
总量的一半的时间)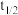
 ;
;
 的最高容许浓度为
的最高容许浓度为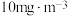 ,则该车间环境
,则该车间环境
您最近一年使用:0次
23-24高三上·辽宁锦州·期末
5 . 工业上可通过“酸性歧化法”制备KMnO4:将软锰矿(主要成分为MnO2)先氧化成K2MnO4,进而在酸性条件下制备KMnO4,流程如下图所示。实验室中模拟“酸性歧化法”制备KMnO4下列说法正确的是

| A.“熔融”操作应在石英坩埚中进行 |
| B.“酸化”反应中氧化产物与还原产物的物质的量之比为2:1 |
| C.“酸化”时可改用盐酸代替CO2 |
| D.“结晶”过程中加热蒸发至有较多晶体析出时停止加热 |
您最近一年使用:0次
6 . 三草酸合铁(Ⅲ)酸钾的化学式为 ,是用于制备负载型活性铁催化剂的主要原料,也是一些有机反应的催化剂,具有工业生产价值。实验室采用如下方案制备三草酸合铁酸钾。
,是用于制备负载型活性铁催化剂的主要原料,也是一些有机反应的催化剂,具有工业生产价值。实验室采用如下方案制备三草酸合铁酸钾。
步骤①:先在烧杯中加入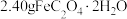 晶体,再加入
晶体,再加入 饱和草酸钾溶液,水浴加热
饱和草酸钾溶液,水浴加热 ,用滴管慢慢加入
,用滴管慢慢加入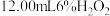 溶液,不断搅拌,充分反应后溶液为绿色并有红褐色沉淀生成。
溶液,不断搅拌,充分反应后溶液为绿色并有红褐色沉淀生成。
步骤②:加热溶液至沸腾,然后将适量草酸溶液逐滴滴入上述溶液中,不断搅拌至沉淀完全溶解为透明的绿色溶液。
步骤③:最后冷却后,缓慢加入无水乙醇,结晶、过滤、洗涤、干燥得到粗产品。
已知:三草酸合铁酸钾为翠绿色晶体,易溶于水,难溶于乙醇,光照时分解得到黄色晶体 。
。
(1)步骤①中发生的化学方程式是_______ 。
(2)步骤②“加热至沸腾”的目的是_______ ,步骤③乙醇要缓慢加入的原因是_______ 。
(3)下列有关说法正确的是_______。
(4)用高锰酸钾滴定法测产品的纯度。
①标定高锰酸钾溶液浓度,请选择以下正确的操作并排序:配制 草酸基准试剂
草酸基准试剂
_______  配制约
配制约_______ 高锰酸钾溶液
_______ 
_______ ,平行滴定三次,计算高锰酸钾溶液的浓度
a.用移液管移取 草酸基准试剂于
草酸基准试剂于 锥形瓶中
锥形瓶中
b.用移液管移取 草酸基准试剂于
草酸基准试剂于 锥形瓶中
锥形瓶中
c.
d.
e.
f.装入洁净干燥的酸式滴定管中
g.装入洁净干燥的碱式滴定管中
h.滴定至溶液由红色变无色且 内不变色
内不变色
i.滴定至溶液由无色变微红色且 内不褪色
内不褪色
j.滴定至溶液由无色变紫红色且 内不褪色
内不褪色
三次滴定数据记录如下:
②准确称取 产品三草酸合铁酸钾晶体
产品三草酸合铁酸钾晶体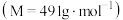 ,用上述已标定浓度的高锰酸钾溶液滴定,消耗
,用上述已标定浓度的高锰酸钾溶液滴定,消耗 高锰酸钾溶液,则该次实验制得的产品纯度为
高锰酸钾溶液,则该次实验制得的产品纯度为_______ 。
 ,是用于制备负载型活性铁催化剂的主要原料,也是一些有机反应的催化剂,具有工业生产价值。实验室采用如下方案制备三草酸合铁酸钾。
,是用于制备负载型活性铁催化剂的主要原料,也是一些有机反应的催化剂,具有工业生产价值。实验室采用如下方案制备三草酸合铁酸钾。步骤①:先在烧杯中加入
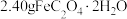 晶体,再加入
晶体,再加入 饱和草酸钾溶液,水浴加热
饱和草酸钾溶液,水浴加热 ,用滴管慢慢加入
,用滴管慢慢加入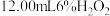 溶液,不断搅拌,充分反应后溶液为绿色并有红褐色沉淀生成。
溶液,不断搅拌,充分反应后溶液为绿色并有红褐色沉淀生成。步骤②:加热溶液至沸腾,然后将适量草酸溶液逐滴滴入上述溶液中,不断搅拌至沉淀完全溶解为透明的绿色溶液。
步骤③:最后冷却后,缓慢加入无水乙醇,结晶、过滤、洗涤、干燥得到粗产品。
已知:三草酸合铁酸钾为翠绿色晶体,易溶于水,难溶于乙醇,光照时分解得到黄色晶体
 。
。(1)步骤①中发生的化学方程式是
(2)步骤②“加热至沸腾”的目的是
(3)下列有关说法正确的是_______。
| A.可将乙二醇滴入酸性重铬酸钾溶液中制得草酸溶液 |
B.光照三草酸合铁酸钾发生: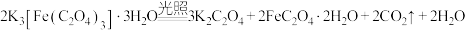 |
| C.步骤②的目的是将氢氧化铁沉淀转化为三草酸合铁酸钾以提高产率 |
D.步骤③中“洗涤”可采用冷水或 酒精洗涤 酒精洗涤 |
(4)用高锰酸钾滴定法测产品的纯度。
①标定高锰酸钾溶液浓度,请选择以下正确的操作并排序:配制
 草酸基准试剂
草酸基准试剂
 配制约
配制约

a.用移液管移取
 草酸基准试剂于
草酸基准试剂于 锥形瓶中
锥形瓶中b.用移液管移取
 草酸基准试剂于
草酸基准试剂于 锥形瓶中
锥形瓶中c.

d.

e.

f.装入洁净干燥的酸式滴定管中
g.装入洁净干燥的碱式滴定管中
h.滴定至溶液由红色变无色且
 内不变色
内不变色i.滴定至溶液由无色变微红色且
 内不褪色
内不褪色j.滴定至溶液由无色变紫红色且
 内不褪色
内不褪色三次滴定数据记录如下:
| 序号 | 1 | 2 | 3 |
滴定前读数 | 0.98 | 1.26 | 1.01 |
滴定后读数 | 11.00 | 10.12 | 10.99 |
 产品三草酸合铁酸钾晶体
产品三草酸合铁酸钾晶体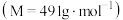 ,用上述已标定浓度的高锰酸钾溶液滴定,消耗
,用上述已标定浓度的高锰酸钾溶液滴定,消耗 高锰酸钾溶液,则该次实验制得的产品纯度为
高锰酸钾溶液,则该次实验制得的产品纯度为
您最近一年使用:0次
解题方法
7 . 工业制备茉莉醛( )的流程如图所示。下列说法正确的是
)的流程如图所示。下列说法正确的是
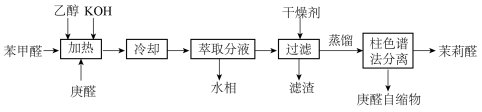
| A.乙醇只作溶剂,苯甲醛和庚醛直接混合后保温反应 |
| B.萃取分液过程中需酸洗、水洗,干燥剂可选用浓硫酸 |
| C.可将最后两步“分馏”和“柱色谱分离”合并为“真空减压分馏” |
| D.可采用质谱法测定茉莉醛部分结构信息 |
您最近一年使用:0次
解题方法
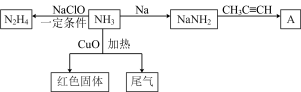
8 . 氨气用途非常广泛,以下是氨气的部分转化关系图。
②随着杂化轨道中s成分的增加,电子云更靠近原子核,核对电子的吸引力增强
(1) 又称联氨,不如氨气稳定,还原性强于氨气,与
又称联氨,不如氨气稳定,还原性强于氨气,与 反应释放出大量热、产物无污染、产生大量气体,可作为火箭推进剂。
反应释放出大量热、产物无污染、产生大量气体,可作为火箭推进剂。
①写出 用于火箭推进剂反应的化学方程式
用于火箭推进剂反应的化学方程式___________ 。
②从分子结构角度分析, 不如氨气稳定的原因是
不如氨气稳定的原因是___________ 。
(2)下列说法正确的是___________。
(3)结合已知信息,写出生成A的化学方程式___________ 。
(4)实验中在加热条件下通入过量的 与CuO反应,设计实验验证尾气中比较活泼的两种气体
与CuO反应,设计实验验证尾气中比较活泼的两种气体___________ 。

②随着杂化轨道中s成分的增加,电子云更靠近原子核,核对电子的吸引力增强
(1)
 又称联氨,不如氨气稳定,还原性强于氨气,与
又称联氨,不如氨气稳定,还原性强于氨气,与 反应释放出大量热、产物无污染、产生大量气体,可作为火箭推进剂。
反应释放出大量热、产物无污染、产生大量气体,可作为火箭推进剂。①写出
 用于火箭推进剂反应的化学方程式
用于火箭推进剂反应的化学方程式②从分子结构角度分析,
 不如氨气稳定的原因是
不如氨气稳定的原因是(2)下列说法正确的是___________。
A.以上转化关系中 只表现出还原性 只表现出还原性 |
| B.若CuO无剩余,红色固体的组分可能有三种情况 |
| C.制备氨基钠需在无水、无氧环境中进行 |
D.为了增加 的产量,往往加入过量的NaClO 的产量,往往加入过量的NaClO |
(3)结合已知信息,写出生成A的化学方程式
(4)实验中在加热条件下通入过量的
 与CuO反应,设计实验验证尾气中比较活泼的两种气体
与CuO反应,设计实验验证尾气中比较活泼的两种气体
您最近一年使用:0次
9 . 硫脲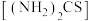 是制造磺胺药物的原料。150℃时硫脲部分异构化为
是制造磺胺药物的原料。150℃时硫脲部分异构化为 ,硫脲能溶于水和乙醇,但不溶于乙醚等有机溶剂。一种制备硫脲的新工艺如图所示。
,硫脲能溶于水和乙醇,但不溶于乙醚等有机溶剂。一种制备硫脲的新工艺如图所示。

(1)“合成”时,反应釜中加入石灰氮( )和水,边搅拌边通入H2S,化学方程式为:
)和水,边搅拌边通入H2S,化学方程式为:_____ 。
(2)洗液、母液循环回收用于“合成”工序,目的是___________ 。
(3)硫脲与尿素、聚乙烯醇熔融生成固体电解质(SPE)。用导电性很弱的丙酮作溶剂,浸取SPE得到丙酮浸出液并进行如下实验:
①向浸出液中滴加盐酸,测得溶液导电率与盐酸体积关系如图2所示。实验发现:CD段产生沉淀质量最大,用元素分析仪测定该沉淀仅含氮、氢、氯三种元素,进一步实验发现,该沉淀有固定熔点,与NaOH浓溶液共热产生一种能使湿润的红色石蕊试纸变蓝色的气体。由此推知,产生沉淀的成分是___________ (填化学式),BC段导电率降低的主要原因是___________ 。

②用下图装置及后续实验可证明固体电解质导电离子是 ,请写出后续实验操作:
,请写出后续实验操作:___________ (注: 不参与电极反应)。
不参与电极反应)。

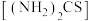 是制造磺胺药物的原料。150℃时硫脲部分异构化为
是制造磺胺药物的原料。150℃时硫脲部分异构化为 ,硫脲能溶于水和乙醇,但不溶于乙醚等有机溶剂。一种制备硫脲的新工艺如图所示。
,硫脲能溶于水和乙醇,但不溶于乙醚等有机溶剂。一种制备硫脲的新工艺如图所示。
(1)“合成”时,反应釜中加入石灰氮(
 )和水,边搅拌边通入H2S,化学方程式为:
)和水,边搅拌边通入H2S,化学方程式为:(2)洗液、母液循环回收用于“合成”工序,目的是
(3)硫脲与尿素、聚乙烯醇熔融生成固体电解质(SPE)。用导电性很弱的丙酮作溶剂,浸取SPE得到丙酮浸出液并进行如下实验:
①向浸出液中滴加盐酸,测得溶液导电率与盐酸体积关系如图2所示。实验发现:CD段产生沉淀质量最大,用元素分析仪测定该沉淀仅含氮、氢、氯三种元素,进一步实验发现,该沉淀有固定熔点,与NaOH浓溶液共热产生一种能使湿润的红色石蕊试纸变蓝色的气体。由此推知,产生沉淀的成分是

②用下图装置及后续实验可证明固体电解质导电离子是
 ,请写出后续实验操作:
,请写出后续实验操作: 不参与电极反应)。
不参与电极反应)。
您最近一年使用:0次
10 . 甘氨酸亚铁[ ],是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组模拟其合成方法如下:
],是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组模拟其合成方法如下:

已知:①甘氨酸、甘氨酸亚铁易溶于水,微溶于乙醇、丙酮等有机溶剂
②异抗坏血酸易溶于水和乙醇、丙酮,有弱酸性和强还原性
③不同铁盐在有机溶剂中的溶解度如下表所示:
注:- -为不溶解;-为溶解不明显;+ -为溶解明显,+ +为全部溶解
请回答:
(1)如图所示合成装置中仪器b的名称是___________ 。

(2)流程中的亚铁盐和有机溶剂A应选择___________。
(3)合成过程中,本实验为了防止 被氧化,采取的措施除通入N2,还有
被氧化,采取的措施除通入N2,还有___________ 。
(4)步骤Ⅱ生成甘氨酸亚铁络合物的离子方程式___________ 。
(5)下列说法正确的是___________。
(6)合成过程需控制pH=5.5,试说明理由___________ 。
(7)产品分析:
①用酸性高锰酸钾溶液滴定法测定产品甘氨酸亚铁的 含量,进而计算产品甘氨酸亚铁的纯度,测定结果产品纯度总是大于100%,试分析主要原因可能是
含量,进而计算产品甘氨酸亚铁的纯度,测定结果产品纯度总是大于100%,试分析主要原因可能是___________ (滴定过程各项操作均正确)
②经查阅文献后,改用硫酸铈溶液滴定。称取5.000 g产品加酸溶解,用容量瓶配成250 mL溶液,移取25.00 mL于锥形瓶中,用0.1000 mol/L硫酸铈溶液滴定至终点。平行测定三次,平均消耗硫酸铈标准滴定溶液20.00 mL,计算产品中 的纯度为
的纯度为___________ 。(每1 mL 0.1000 mol/L硫酸铈溶液相当于20.40 mg甘氨酸亚铁)
 ],是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组模拟其合成方法如下:
],是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组模拟其合成方法如下:
已知:①甘氨酸、甘氨酸亚铁易溶于水,微溶于乙醇、丙酮等有机溶剂
②异抗坏血酸易溶于水和乙醇、丙酮,有弱酸性和强还原性
③不同铁盐在有机溶剂中的溶解度如下表所示:
| 铁盐 | 乙醇的体积分数/% | 丙酮的体积分数/% | ||||||||||||
| 100 | 90 | 80 | 70 | 60 | 50 | 40 | 100 | 90 | 80 | 70 | 60 | 50 | 40 | |
 | - - | - | - | - | - | - | + - | - - | - | - | - | - | - | + - |
 | + + | + + | + + | + + | + + | + + | + + | - - | - | - | - | - | - | + - |
请回答:
(1)如图所示合成装置中仪器b的名称是

(2)流程中的亚铁盐和有机溶剂A应选择___________。
A. 乙醇 乙醇 | B. 丙酮 丙酮 |
C. 乙醇 乙醇 | D. 丙酮 丙酮 |
 被氧化,采取的措施除通入N2,还有
被氧化,采取的措施除通入N2,还有(4)步骤Ⅱ生成甘氨酸亚铁络合物的离子方程式
(5)下列说法正确的是___________。
| A.滴入液体前,应先打开滴液漏斗a的上口玻璃塞 |
| B.步骤Ⅱ应采用水浴加热 |
| C.步骤Ⅲ中的分离方法是过滤 |
| D.步骤Ⅲ加入有机溶剂A的目的是降低甘氨酸亚铁在水中的溶解度,促使其结晶析出,同时除去杂质 |
(7)产品分析:
①用酸性高锰酸钾溶液滴定法测定产品甘氨酸亚铁的
 含量,进而计算产品甘氨酸亚铁的纯度,测定结果产品纯度总是大于100%,试分析主要原因可能是
含量,进而计算产品甘氨酸亚铁的纯度,测定结果产品纯度总是大于100%,试分析主要原因可能是②经查阅文献后,改用硫酸铈溶液滴定。称取5.000 g产品加酸溶解,用容量瓶配成250 mL溶液,移取25.00 mL于锥形瓶中,用0.1000 mol/L硫酸铈溶液滴定至终点。平行测定三次,平均消耗硫酸铈标准滴定溶液20.00 mL,计算产品中
 的纯度为
的纯度为
您最近一年使用:0次



