名校
1 . 氯气和亚氯酸钠(NaClO2)都是重要的漂白剂。
(I)某小组以KMnO4和浓盐酸为原料制备干燥、纯净的氯气___________ 。
(2)制备氯气时,可选用的发生装置为___________ (填序号),选择上述合适的装置,其连接顺序为:发生装置→___________ →i(按气流方向,用小写字母表示)。
(3)F装置所盛溶液是___________ (填溶液名称)。
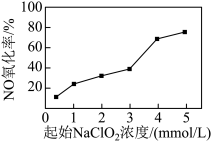
(II)工业上NaClO2可由ClO2、H2O2和NaOH溶液混合制得,实验流程如下:___________ 。
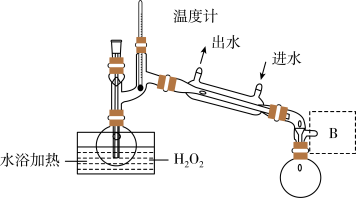
(5)已知H2O2(沸点150℃)浓度对反应速率有影响。通过下图所示装置将少量30% H2O2溶液浓缩至40%,B处应增加一个设备。该设备的作用是___________ 。___________ 。
(I)某小组以KMnO4和浓盐酸为原料制备干燥、纯净的氯气
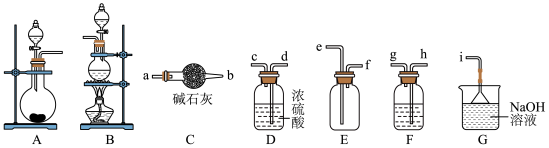
(2)制备氯气时,可选用的发生装置为
(3)F装置所盛溶液是
(II)工业上NaClO2可由ClO2、H2O2和NaOH溶液混合制得,实验流程如下:

(5)已知H2O2(沸点150℃)浓度对反应速率有影响。通过下图所示装置将少量30% H2O2溶液浓缩至40%,B处应增加一个设备。该设备的作用是
您最近半年使用:0次
2 . 用如图装置(夹持装置已略去)进行 制备及性质实验,下列说法不正确的是
制备及性质实验,下列说法不正确的是
 制备及性质实验,下列说法不正确的是
制备及性质实验,下列说法不正确的是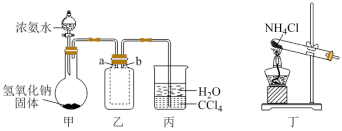
A.甲中制备 利用了 利用了 的分解反应,丁也可以用于制备氨气 的分解反应,丁也可以用于制备氨气 |
| B.乙中的集气瓶内a导管短、b导管长 |
C.不能将丙中的 换成食用油 换成食用油 |
D.向收集好的 中通入少量 中通入少量 ,可能观察到白烟 ,可能观察到白烟 |
您最近半年使用:0次
3 . 镁及其合金是用途很广的金属材料,可以通过以下步骤从海水中提取镁。
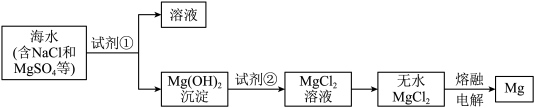
下列说法不正确 的是

下列说法
| A.试剂①可以选用石灰乳 |
B.加入试剂①后,能够分离得到 沉淀的方法是过滤 沉淀的方法是过滤 |
C. 溶液通过蒸发结晶可得到无水 溶液通过蒸发结晶可得到无水 |
D.电解熔融 所得副产物 所得副产物 是工业制备试剂②的主要原料 是工业制备试剂②的主要原料 |
您最近半年使用:0次
2024-04-18更新
|
202次组卷
|
2卷引用:浙江绍兴市2023-2024学年高三下学期选考科目适应性考试化学试题
名校
4 . 四氮化四硫( ,S为+2价)是重要的硫一氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于
,S为+2价)是重要的硫一氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于 等有机溶剂,可用
等有机溶剂,可用 与
与 (红棕色液体)反应制备,反应装置如图所示(夹持装置略)。
(红棕色液体)反应制备,反应装置如图所示(夹持装置略)。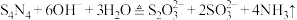 ,回答下列问题:
,回答下列问题:
(1)仪器a的名称为________ ;装置D的作用是________ 。
(2)四氮化四硫( )为双楔形笼状结构,如下图(a)所示。S和N原子交替构成一个假想的八元环,各S-N键长几乎相等。请回答以下问题:
)为双楔形笼状结构,如下图(a)所示。S和N原子交替构成一个假想的八元环,各S-N键长几乎相等。请回答以下问题: 的双楔形笼状结构可通过
的双楔形笼状结构可通过________ 实验测得。
② 分子中正、负电荷的重心完全重合,则为分子
分子中正、负电荷的重心完全重合,则为分子________ (填“极性”或“非极性”)。
③已知:多原子分子中相互平行的多条p轨道,连贯重叠构成一个整体,p电子在多个原子间运动形成大π键,如苯分子存在 型大π键。有研究者提出
型大π键。有研究者提出 的另一种平面八元环结构,如上图(b),S原子的杂化方式为
的另一种平面八元环结构,如上图(b),S原子的杂化方式为________ ;请写出平面 中的大π键类型
中的大π键类型________ 。
(3)装置C中生成 的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为
的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为________ ;证明 反应完全的现象是
反应完全的现象是________ 。
(4)分离产物后测定产品纯度:
i.取0.1000g样品加入三颈烧瓶中,再加入足量NaOH溶液并加热蒸出 ;
;
ii.将蒸出的 通入含甲基橙的
通入含甲基橙的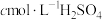 标准溶液中,消耗
标准溶液中,消耗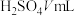 。
。
根据上述实验,计算样品中 的纯度
的纯度________ (列出表达式)。
 ,S为+2价)是重要的硫一氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于
,S为+2价)是重要的硫一氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于 等有机溶剂,可用
等有机溶剂,可用 与
与 (红棕色液体)反应制备,反应装置如图所示(夹持装置略)。
(红棕色液体)反应制备,反应装置如图所示(夹持装置略)。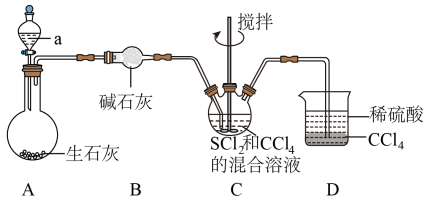
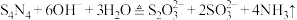 ,回答下列问题:
,回答下列问题:(1)仪器a的名称为
(2)四氮化四硫(
 )为双楔形笼状结构,如下图(a)所示。S和N原子交替构成一个假想的八元环,各S-N键长几乎相等。请回答以下问题:
)为双楔形笼状结构,如下图(a)所示。S和N原子交替构成一个假想的八元环,各S-N键长几乎相等。请回答以下问题: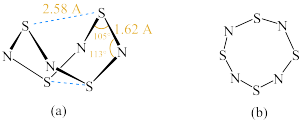
 的双楔形笼状结构可通过
的双楔形笼状结构可通过②
 分子中正、负电荷的重心完全重合,则为分子
分子中正、负电荷的重心完全重合,则为分子③已知:多原子分子中相互平行的多条p轨道,连贯重叠构成一个整体,p电子在多个原子间运动形成大π键,如苯分子存在
 型大π键。有研究者提出
型大π键。有研究者提出 的另一种平面八元环结构,如上图(b),S原子的杂化方式为
的另一种平面八元环结构,如上图(b),S原子的杂化方式为 中的大π键类型
中的大π键类型(3)装置C中生成
 的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为
的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为 反应完全的现象是
反应完全的现象是(4)分离产物后测定产品纯度:
i.取0.1000g样品加入三颈烧瓶中,再加入足量NaOH溶液并加热蒸出
 ;
;ii.将蒸出的
 通入含甲基橙的
通入含甲基橙的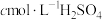 标准溶液中,消耗
标准溶液中,消耗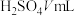 。
。根据上述实验,计算样品中
 的纯度
的纯度
您最近半年使用:0次
2024-04-11更新
|
104次组卷
|
2卷引用:浙江省舟山中学2023-2024学年高二下学期4月月考化学试题
5 . 实验室由安息香制备二苯乙二酮的反应如下:
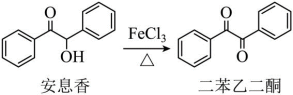
相关信息列表如下:
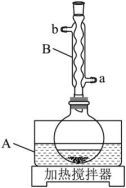
装置示意图如下图所示,实验步骤为:
①在圆底烧瓶中加入10mL冰乙酸、5mL水及 ,边搅拌边加热,至固体全部溶解。
,边搅拌边加热,至固体全部溶解。
②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min。
③加入50mL水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g。
回答下列问题:
(1)仪器A中应加入_______ (填“水”或“油”)作为热传导介质。
(2)仪器B的名称是_______ ;冷却水应从_______ (填“a”或“b”)口通入。
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是_______ 。
(4)在本实验中, 为氧化剂且过量,写出安息香制备二苯乙二酮的化学方程式
为氧化剂且过量,写出安息香制备二苯乙二酮的化学方程式_______ ;某同学改进本实验:用少量 并通入空气制备二苯乙二酮。简述该方案中氯化铁为何只需少量的
并通入空气制备二苯乙二酮。简述该方案中氯化铁为何只需少量的 参与反应。
参与反应。_______ 。
(5)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是_______ 。
(6)若粗品中混有少量未氧化的安息香,可用少量_______ 洗涤的方法除去(填标号)。若要得到更高纯度的产品,可用重结晶的方法进一步提纯。
a.热水 b.乙酸 c.冷水 d.乙醇
(7)本实验的产率最接近于_______ (填标号)。
a.85% b.80% c.75% d.70%

相关信息列表如下:
| 物质 | 性状 | 熔点/℃ | 沸点/℃ | 溶解性 |
| 安息香 | 白色固体 | 133 | 344 | 难溶于冷水 溶于热水、乙醇、乙酸 |
| 二苯乙二酮 | 淡黄色固体 | 95 | 347 | 不溶于水 溶于乙醇、苯、乙酸 |
| 冰乙酸 | 无色液体 | 17 | 118 | 与水、乙醇互溶 |

①在圆底烧瓶中加入10mL冰乙酸、5mL水及
 ,边搅拌边加热,至固体全部溶解。
,边搅拌边加热,至固体全部溶解。②停止加热,待沸腾平息后加入2.0g安息香,加热回流45~60min。
③加入50mL水,煮沸后冷却,有黄色固体析出。
④过滤,并用冷水洗涤固体3次,得到粗品。
⑤粗品用75%的乙醇重结晶,干燥后得淡黄色结晶1.6g。
回答下列问题:
(1)仪器A中应加入
(2)仪器B的名称是
(3)实验步骤②中,安息香必须待沸腾平息后方可加入,其主要目的是
(4)在本实验中,
 为氧化剂且过量,写出安息香制备二苯乙二酮的化学方程式
为氧化剂且过量,写出安息香制备二苯乙二酮的化学方程式 并通入空气制备二苯乙二酮。简述该方案中氯化铁为何只需少量的
并通入空气制备二苯乙二酮。简述该方案中氯化铁为何只需少量的 参与反应。
参与反应。(5)本实验步骤①~③在乙酸体系中进行,乙酸除作溶剂外,另一主要作用是
(6)若粗品中混有少量未氧化的安息香,可用少量
a.热水 b.乙酸 c.冷水 d.乙醇
(7)本实验的产率最接近于
a.85% b.80% c.75% d.70%
您最近半年使用:0次
6 . Ⅰ.按要求回答下列问题:
(1)下列物质中① ;②乙醇;③熔融
;②乙醇;③熔融 ;④
;④ 溶液;⑤固态
溶液;⑤固态 ,其中属于电解质的是
,其中属于电解质的是___________ (只填序号,下同),属于非电解质的是___________ 。所给状态下能导电的是___________ 。
(2)配平方程式,并在方程式上用双线桥表示出电子转移情况。____________ 。

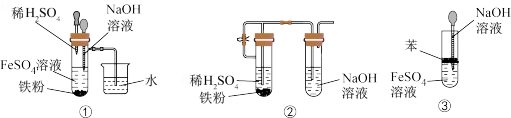
Ⅱ.下图所示装置,可用来制取 和观察
和观察 在空气中被氧化的颜色变化。实验时必须使用铁屑和
在空气中被氧化的颜色变化。实验时必须使用铁屑和 的硫酸,其他试剂任选。
的硫酸,其他试剂任选。
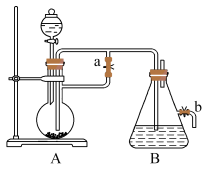
(3)实验开始时应先将活塞a___________ (填“打开”或“关闭”)。
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为___________ 。
(5)下图中___________ 装置能较长时间看到 白色沉淀(填装置序号)。
白色沉淀(填装置序号)。
(1)下列物质中①
 ;②乙醇;③熔融
;②乙醇;③熔融 ;④
;④ 溶液;⑤固态
溶液;⑤固态 ,其中属于电解质的是
,其中属于电解质的是(2)配平方程式,并在方程式上用双线桥表示出电子转移情况。

Ⅱ.下图所示装置,可用来制取
 和观察
和观察 在空气中被氧化的颜色变化。实验时必须使用铁屑和
在空气中被氧化的颜色变化。实验时必须使用铁屑和 的硫酸,其他试剂任选。
的硫酸,其他试剂任选。
(3)实验开始时应先将活塞a
(4)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为
(5)下图中
 白色沉淀(填装置序号)。
白色沉淀(填装置序号)。
您最近半年使用:0次
解题方法
7 . 下图是工业生产纯碱的工艺流程示意图。
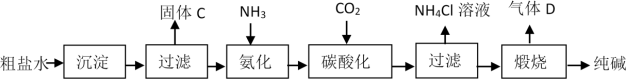
已知:①粗盐水中含有MgCl2、CaCl2;②常温下,NH3极易溶于水,CO2能溶于水,完成下列填空:
(1)粗盐水加入沉淀剂NaOH、___________ (填化学式)以分别除去MgCl2、CaCl2杂质,实验室过滤使用的仪器除烧杯、玻璃棒外还需要的玻璃仪器是___________ 。
(2)在工业生产纯碱工艺流程中,“碳酸化”时,NaCl、NH3、CO2和H2O相互作用析出NaHCO3,写出该反应的化学方程式___________ 。
(3)“煅烧”时,NaHCO3分解方程式是___________ 。
(4)鉴别产品纯碱中是否含有碳酸氢钠的方法是___________ 。

已知:①粗盐水中含有MgCl2、CaCl2;②常温下,NH3极易溶于水,CO2能溶于水,完成下列填空:
(1)粗盐水加入沉淀剂NaOH、
(2)在工业生产纯碱工艺流程中,“碳酸化”时,NaCl、NH3、CO2和H2O相互作用析出NaHCO3,写出该反应的化学方程式
(3)“煅烧”时,NaHCO3分解方程式是
(4)鉴别产品纯碱中是否含有碳酸氢钠的方法是
您最近半年使用:0次
名校
8 . 苯环的结构很稳定,常温下较难发生化学反应。某实验小组利用下列装置探究苯在一定条件下的反应产物。回答下列问题:
I.实验室制取硝基苯常采用如图所示装置。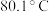 、
、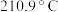 ,且二者互溶。
,且二者互溶。
(1)①开始时应向试管中加入一定量的苯、浓硫酸和___________ 。
②该装置采取水浴加热并控制温度在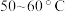 的原因是
的原因是___________ ;写出制取硝基苯的化学方程式:___________ 。制得的产物可通过___________ 方法提纯。
Ⅱ.该小组同学还设计了A、B、C三组实验装置用来制取溴苯。___________ ,三个装置中所共同发生的有机反应的化学方程式为___________ 。
(3)实验结束后,小明取装置A中锥形瓶中的水溶液少许,加入 溶液得到浅黄色沉淀,证明苯与溴发生了取代反应,该结论
溶液得到浅黄色沉淀,证明苯与溴发生了取代反应,该结论___________ (填“正确”或“错误”),原因是___________ 。
(4)装置B中足量 的作用是
的作用是___________ 。
(5)装置B也存在两个明显的缺点,使实验的效果不好或不能正常进行。这两个缺点是原料逸出使利用率降低和___________ 。
I.实验室制取硝基苯常采用如图所示装置。
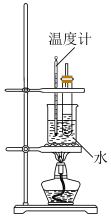
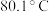 、
、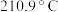 ,且二者互溶。
,且二者互溶。(1)①开始时应向试管中加入一定量的苯、浓硫酸和
②该装置采取水浴加热并控制温度在
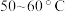 的原因是
的原因是Ⅱ.该小组同学还设计了A、B、C三组实验装置用来制取溴苯。
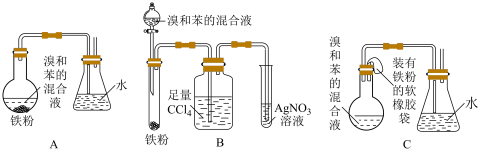
(3)实验结束后,小明取装置A中锥形瓶中的水溶液少许,加入
 溶液得到浅黄色沉淀,证明苯与溴发生了取代反应,该结论
溶液得到浅黄色沉淀,证明苯与溴发生了取代反应,该结论(4)装置B中足量
 的作用是
的作用是(5)装置B也存在两个明显的缺点,使实验的效果不好或不能正常进行。这两个缺点是原料逸出使利用率降低和
您最近半年使用:0次
2024-03-30更新
|
579次组卷
|
3卷引用:浙江省宁波市镇海中2023-2024学年高二下学期期中考试化学试题
名校
9 . 某实验小组用如下实验装置模拟工业上制取硝酸:________________ 。
(2)由于水的比热容较大,A中挥发的水蒸气会影响B中的反应温度,所以在AB之间插入装有________________ 的干燥装置。
A.浓H2SO4 B.碱石灰
(3)装置C的作用除了防止有水蒸气进入B外,主要是除去混合气中的________________ 。
(4)装置D的作用为________________ 。
(5)工业上要获得浓度较大的硝酸,往往在稀硝酸中加入吸水剂硝酸镁,然后在较低温度下进行蒸馏,不能采用较高温度的原因是(用方程式表示)________________ 。
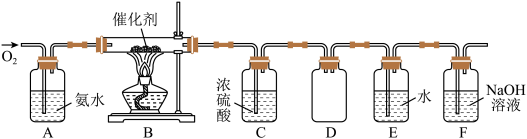
(2)由于水的比热容较大,A中挥发的水蒸气会影响B中的反应温度,所以在AB之间插入装有
A.浓H2SO4 B.碱石灰
(3)装置C的作用除了防止有水蒸气进入B外,主要是除去混合气中的
(4)装置D的作用为
(5)工业上要获得浓度较大的硝酸,往往在稀硝酸中加入吸水剂硝酸镁,然后在较低温度下进行蒸馏,不能采用较高温度的原因是(用方程式表示)
您最近半年使用:0次
10 . 四氮化四硫(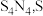 为
为 价)是重要的硫氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于
价)是重要的硫氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于 等有机溶剂,可用
等有机溶剂,可用 与
与 (红棕色液体)反应制备,反应装置如图所示(夹持装置略)。
(红棕色液体)反应制备,反应装置如图所示(夹持装置略)。
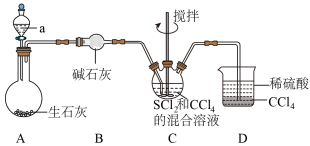
已知:
回答下列问题:
(1)试剂a是___________ 。
(2)装置C中生成 的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为
的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为___________ ;证明 反应完全的现象是
反应完全的现象是___________ 。
(3)分离产物后测定产品纯度:
i.蒸氨:取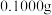 样品加入三颈烧瓶中,再加入足量
样品加入三颈烧瓶中,再加入足量 溶液并加热蒸出的
溶液并加热蒸出的 通入含有
通入含有 标准溶液的锥形瓶中。
标准溶液的锥形瓶中。
ii.滴定:用 溶液滴定剩余的
溶液滴定剩余的 ,消耗
,消耗 溶液。
溶液。
①滴定管的正确操作顺序:检漏 蒸馏水洗涤
蒸馏水洗涤
___________ (填标号) 开始滴定。
开始滴定。
a.装入滴定液至“0”刻度以上 b.调整滴定液液面至“0”刻度
c.排除气泡 d.用滴定液润洗2至3次 e.记录起始读数
② 的纯度表达式为
的纯度表达式为___________ 。
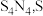 为
为 价)是重要的硫氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于
价)是重要的硫氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于 等有机溶剂,可用
等有机溶剂,可用 与
与 (红棕色液体)反应制备,反应装置如图所示(夹持装置略)。
(红棕色液体)反应制备,反应装置如图所示(夹持装置略)。
已知:

回答下列问题:
(1)试剂a是
(2)装置C中生成
 的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为
的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为 反应完全的现象是
反应完全的现象是(3)分离产物后测定产品纯度:
i.蒸氨:取
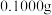 样品加入三颈烧瓶中,再加入足量
样品加入三颈烧瓶中,再加入足量 溶液并加热蒸出的
溶液并加热蒸出的 通入含有
通入含有 标准溶液的锥形瓶中。
标准溶液的锥形瓶中。ii.滴定:用
 溶液滴定剩余的
溶液滴定剩余的 ,消耗
,消耗 溶液。
溶液。①滴定管的正确操作顺序:检漏
 蒸馏水洗涤
蒸馏水洗涤
 开始滴定。
开始滴定。a.装入滴定液至“0”刻度以上 b.调整滴定液液面至“0”刻度
c.排除气泡 d.用滴定液润洗2至3次 e.记录起始读数
②
 的纯度表达式为
的纯度表达式为
您最近半年使用:0次
2024-03-16更新
|
30次组卷
|
2卷引用:浙江省杭州学军中学海创园学校2023-2024学年高二上学期期末考试化学试题



