名校
解题方法
1 . 碘( Godine)是人体必需的微量元素,是维持人体甲状腺正常功能所必需的元素, 人体缺碘时就会患甲状腺肿大,人们主要从饮水、粮食、蔬菜和周围环境中获取碘。多食海带,海鱼等含碘丰富的食品,对于防治甲状腺肿大很有效。某化学课外活动小组在实验室以海带为原料获得少量碘水,并以四氯化碳(沸点76.8℃)为溶剂将碘从碘水中提取出来,甲同学设计实验流程如图所示。请回答下列问题:
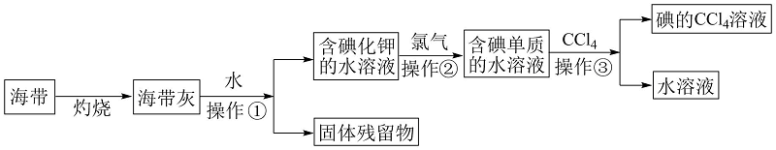
(1)上述流程中灼烧时必须用到最主要 的实验仪器有酒精灯、泥三角和___________ (填名称)。
(2)操作①的名称为___________ ;
(3)操作②中发生反应的离子方程式为______________________ ,乙同学对操作②进行了改进,用绿色氧化剂H2O2代替氯气并加适量稀盐酸,则所发生的离子反应方程式是____________________________________ 。
(4)操作③的实验名称为___________ ,最主要的 实验仪器的名称为___________ ;
(5)丙同学补充增加了一步操作:从碘的CCl4溶液中经过___________ 提取了碘单质并回收CCl4(填该操作名称)
(6)目前,我国推行全民食用的加碘盐是在食盐中加入___________ 这一物质(填写化学式)。

(1)上述流程中灼烧时
(2)操作①的名称为
(3)操作②中发生反应的离子方程式为
(4)操作③的实验名称为
(5)丙同学补充增加了一步操作:从碘的CCl4溶液中经过
(6)目前,我国推行全民食用的加碘盐是在食盐中加入
您最近一年使用:0次
名校
2 . 碘是动植物和人体必需的微量元素,I-的氧化和单质I2的分离是海带中碘元素分离的关键步骤。某学习小组在实验室对海带中碘元素进行分离和含量测定,并进行实验改进。
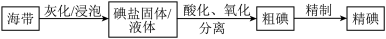
(1)海带中的碘元素以碘化物的形式存在,在酸化、氧化操作中,该小组首先选用氯水作为氧化剂,当氯水过量时碘单质被继续氧化成IO ,与该过程相关的离子方程式为
,与该过程相关的离子方程式为______ 、_____ 。
(2)针对以上出现的问题,该小组对实验进行改进,采用双氧水做氧化剂,逐滴滴加到过量I-溶液中,溶液颜色逐渐由黄色变为棕色。其反应原理为:①2I-+2H++H2O2=I2+2H2O②I-+I2=I (低浓度为黄色,高浓度为棕色)。过氧化氢过量时:③I2+5H2O2=HIO3(无色溶液)+4H2O。如果双氧水滴加过量,造成的影响为
(低浓度为黄色,高浓度为棕色)。过氧化氢过量时:③I2+5H2O2=HIO3(无色溶液)+4H2O。如果双氧水滴加过量,造成的影响为_____ 。而且该反应过程放出大量热,会对I2的提取造成的影响是_____ 。
(3)该小组针对问题又提出新的解决办法,采用溶液反加法,将I-溶液缓慢滴加到足量酸酸化的H2O2中,其反应如下:①2I-+2H++H2O2=I2+2H2O②I2+5H2O2=2HIO3+4H2O③4HI+2HIO3=3I2+6H2O。缓慢滴加过程中至反应结束,可观察到混合液颜色变化和现象为_____ 。
A.黄色逐渐加深,直到紫色沉淀析出
B.紫色逐渐加深,直到紫色沉淀析出
C.黄色逐渐变为棕色,直到紫色沉淀析出
D.黄色变无色,再变为黄色,搅拌后变为无色……,直到紫色沉淀析出
该实验改进措施最大的优点为_____ 。

(1)海带中的碘元素以碘化物的形式存在,在酸化、氧化操作中,该小组首先选用氯水作为氧化剂,当氯水过量时碘单质被继续氧化成IO
 ,与该过程相关的离子方程式为
,与该过程相关的离子方程式为(2)针对以上出现的问题,该小组对实验进行改进,采用双氧水做氧化剂,逐滴滴加到过量I-溶液中,溶液颜色逐渐由黄色变为棕色。其反应原理为:①2I-+2H++H2O2=I2+2H2O②I-+I2=I
 (低浓度为黄色,高浓度为棕色)。过氧化氢过量时:③I2+5H2O2=HIO3(无色溶液)+4H2O。如果双氧水滴加过量,造成的影响为
(低浓度为黄色,高浓度为棕色)。过氧化氢过量时:③I2+5H2O2=HIO3(无色溶液)+4H2O。如果双氧水滴加过量,造成的影响为(3)该小组针对问题又提出新的解决办法,采用溶液反加法,将I-溶液缓慢滴加到足量酸酸化的H2O2中,其反应如下:①2I-+2H++H2O2=I2+2H2O②I2+5H2O2=2HIO3+4H2O③4HI+2HIO3=3I2+6H2O。缓慢滴加过程中至反应结束,可观察到混合液颜色变化和现象为
A.黄色逐渐加深,直到紫色沉淀析出
B.紫色逐渐加深,直到紫色沉淀析出
C.黄色逐渐变为棕色,直到紫色沉淀析出
D.黄色变无色,再变为黄色,搅拌后变为无色……,直到紫色沉淀析出
该实验改进措施最大的优点为
您最近一年使用:0次
解题方法
3 . 下列有关实验操作能达到相应实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 将干海带灼烧、浸取、过滤 | 获得含 的水溶液 的水溶液 |
| B | 将表面积相同的镁条和铝条放入相同浓度相同温度的稀盐酸中 | 比较镁铝的失电子能力 |
| C | 将 固体高温加热成熔融,测其熔融态导电性 固体高温加热成熔融,测其熔融态导电性 | 证明 中含有离子键 中含有离子键 |
| D | 取相同体积不同浓度的 溶液于两试管中,分别向两试管中加入等体积等浓度的 溶液于两试管中,分别向两试管中加入等体积等浓度的 | 探究浓度对化学反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 碘是人体生长发育不可缺少的微量元素,海带中富含碘元素,从海带中提取碘的工艺流程如下。回答下列问题:

(1)步骤①中发生反应的离子方程式为_______ ,当生成0.3molI2时,转移电子的物质的量为_______ mol。
(2)向含有I2的水溶液中加入CCl4振荡静置后的实验现象为_______ 。
(3)步骤③中发生反应的化学方程式为_______ 。
(4)步骤⑤的实验操作名称为_______ 。
(5)步骤③④是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为_______ 法。

(1)步骤①中发生反应的离子方程式为
(2)向含有I2的水溶液中加入CCl4振荡静置后的实验现象为
(3)步骤③中发生反应的化学方程式为
(4)步骤⑤的实验操作名称为
(5)步骤③④是利用化学转化法将富集在四氯化碳中的碘单质重新富集在水中,该方法称为
您最近一年使用:0次
名校
5 . 在“海带提碘”实验中,下列不能达到实验目的的是
| A.用过滤的方法除去浸泡液中的海带灰 |
| B.用氯水氧化I-获得碘单质 |
| C.用淀粉溶液检验碘水中的碘单质 |
| D.用酒精萃取碘水中的碘单质 |
您最近一年使用:0次
6 . 下列说法不正确 的是
| A.干燥海带的灼烧在通风处或者通风橱中进行 |
B.亚硝酸钠与 酸性溶液反应, 酸性溶液反应, 溶液由橙色变为绿色 溶液由橙色变为绿色 |
| C.用蒸馏的方法分离汽油和水 |
D. 溶液在滴定过程中宜选用棕色酸式滴定管 溶液在滴定过程中宜选用棕色酸式滴定管 |
您最近一年使用:0次
名校
7 . 海带中含有较多的碘元素,某化学兴趣小组通过以下步骤提取海带中的碘:
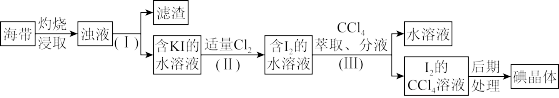
(1)步骤(Ⅰ)中分离操作的名称是_______ ,该操作中用到的玻璃仪器有漏斗、烧杯和_______ 。
(2)写出步骤(Ⅱ)中KI和Cl2反应的离子方程式_______ ,取少量反应后的溶液滴入淀粉试液,溶液呈_______ 色;
(3)步骤(Ⅲ)中萃取后分层, 的
的 溶液在
溶液在_______ (填“上层”或“下层”)。
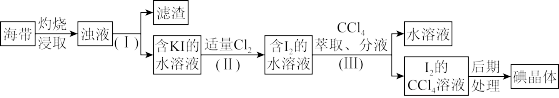
(1)步骤(Ⅰ)中分离操作的名称是
(2)写出步骤(Ⅱ)中KI和Cl2反应的离子方程式
(3)步骤(Ⅲ)中萃取后分层,
 的
的 溶液在
溶液在
您最近一年使用:0次
2022-04-20更新
|
117次组卷
|
2卷引用:福建省莆田第二十五中学2022-2023学年高一下学期期中考试化学试题
8 . 溴、碘主要存在于海水中,有“海洋元素”的美称。从海带中提取碘单质,工艺流程如下图。
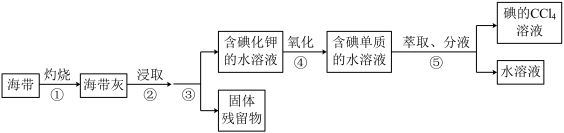
下列操作错误的是

下列操作错误的是
| A | B | C | D |
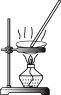 | 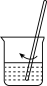 | 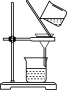 | 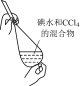 |
| 步骤①操作 | 步骤②操作 | 步骤③操作 | 步骤⑤中振荡萃取操作 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 海带中富含碘元素(主要以KI形式存在)。下面是从海带中提取碘的流程图:
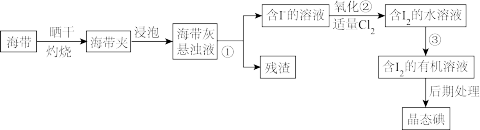
(1)操作①的名称是____ ,在该操作中除了用到玻璃棒、烧杯外,还缺少的玻璃仪器有___ ;操作③的名称是___ ,在该操作中用到的主要玻璃仪器是____ 。
(2)③过程中,可供选择的有关试剂是____ 。
A.酒精 B.四氯化碳 C.醋酸
将你所选择的试剂滴加到含I2的水溶液中,振荡后静置,可观察到的现象是___ 。
(3)请设计一种检验提取碘后的水层中是否还含有单质碘的简单方法_______ 。

(1)操作①的名称是
(2)③过程中,可供选择的有关试剂是
A.酒精 B.四氯化碳 C.醋酸
将你所选择的试剂滴加到含I2的水溶液中,振荡后静置,可观察到的现象是
(3)请设计一种检验提取碘后的水层中是否还含有单质碘的简单方法
您最近一年使用:0次
2021-06-25更新
|
194次组卷
|
2卷引用:福建省莆田二中2019-2020学年高一上学期期中考试化学试题
解题方法
10 . 化学与生产、生活密切相关。下列叙述正确的是
| A.燃煤脱硫有利于实现“碳达峰、碳中和” |
| B.SO2可漂白纸浆,不可用于杀菌、消毒 |
| C.将“84”消毒液与75%酒精1:1混合,消毒效果更好 |
| D.工业上可用离子交换法提高海带中碘的提取率 |
您最近一年使用:0次



