四川省乐山市犍为一中2020届高三模拟考试理综化学试题
四川
高三
阶段练习
2020-05-23
408次
整体难度:
适中
考查范围:
认识化学科学、化学与STSE、化学实验基础、有机化学基础、物质结构与性质、常见无机物及其应用、化学反应原理
四川省乐山市犍为一中2020届高三模拟考试理综化学试题
四川
高三
阶段练习
2020-05-23
408次
整体难度:
适中
考查范围:
认识化学科学、化学与STSE、化学实验基础、有机化学基础、物质结构与性质、常见无机物及其应用、化学反应原理
一、单选题 添加题型下试题
1. 化学与生活、生产、环境密切相关。下列说法错误的是( )
| A.侯德榜制碱法制备NaHCO3的原理是利用溶解度较大的物质制备溶解度较小的物质 |
| B.“雷雨肥庄稼”含义是N2最终转化成NO3-,此转化过程中氮元素被还原 |
| C.“金柔锡柔,合两柔则为刚”中“金”为铜,说明合金的硬度一般大于各组分金属 |
| D.我国科学家利用蜡虫肠道菌群将塑料降解的时间由500年缩减到24小时,有助于解决“白色污染”问题 |
您最近一年使用:0次
2020-04-02更新
|
407次组卷
|
5卷引用:2019年天一大联考高三六联理综——化学试题
单选题
|
较易(0.85)
名校
解题方法
2. 实验室用SO2还原MnO2制备MnSO4的装置如图所示,下列说法正确的是


| A.装置B中试剂可为Na2SO3溶液,其作用是除去SO2中的HCl |
| B.装置D中水浴温度应控制在80℃左右,温度过高时反应速率可能减慢 |
| C.将装置D中所得MnSO4溶液蒸干可获得纯净的MnSO4·H2O |
| D.装置E中发生反应的离子方程式为SO2+2OH-=SO32-+H2O |
您最近一年使用:0次
2020-05-22更新
|
103次组卷
|
2卷引用:四川省乐山市犍为一中2020届高三模拟考试理综化学试题
单选题
|
适中(0.65)
名校
解题方法
3. 旋烷是一类比较特殊的碳氢化合物,其张力较大。如下给出了几种旋烷的结构。下列说法不正确的是


| A.旋烷①与三甲苯互为同分异构体 |
| B.旋烷②的二氯代物种类数小于其十四氯代物的种类数 |
| C.1 mol旋烷③完全燃烧时消耗20 mol O2,生成10 mol H2O |
| D.旋烷系列分子中含碳量为0. 9 |
您最近一年使用:0次
2020-05-22更新
|
104次组卷
|
3卷引用:四川省乐山市犍为一中2020届高三模拟考试理综化学试题
单选题
|
适中(0.65)
名校
解题方法
4. 2019年被联合国定为“国际化学元素周期表年”,如图为元素周期表的一部分,其中W、X、Y、Z均为短周期元素,Y的氧化物易形成酸雨。下列叙述正确的是
| W | X | ||
| Y | Z |
| A.X的简单氢化物为强酸 |
| B.Z的氧化物对应水化物的酸性强于Y的氧化物对应水化物的酸性 |
| C.WY2分子中每个原子最外层均达到8电子稳定结构 |
| D.X单质能够从Z的盐溶液中置换出Z单质 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
5. 下列实验方案与现象正确且能达到相应实验目的的是
| 选项 | 实验目的 | 实验方案与现象 |
| A | 证明新制氯水具有酸性 | 向新制氯水中滴加紫色石蕊试液,溶液变为红色且颜色保持不变 |
| B | 证明酸性条件下,氧化性:H2O2 > Fe3 + | 向Fe(NO3)2溶液中滴加用硫酸酸化的H2O2溶液,溶液变黄色 |
| C | 证明同温下,溶度积常数: Ksp(AgCl)> Ksp(Ag2CrO4) | 向体积为100 mL、浓度均为0.01 mol·L-1的NaCl和Na2CrO4混合溶液中滴加 0.01 mol·L-1AgNO3溶液,先产生白色沉淀,后产生砖红色沉淀Ag2CrO4 |
| D | 证明溶液X中含有 | 向溶液X中先滴加盐酸无明显现象,再滴加BaCl2溶液,出现白色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-05-22更新
|
104次组卷
|
2卷引用:四川省乐山市犍为一中2020届高三模拟考试理综化学试题
单选题
|
适中(0.65)
名校
解题方法
6. 我国成功研发一种新型铝-石墨双离子电池,这种新型电池采用石墨、铝锂合金作为电极材料,以常规锂盐和碳酸酯溶剂为电解液。电池总反应为Cx(PF6) +LiAl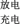 xC + PF6-+Li+ +Al。该电池放电时的工作原理如图所示。下列说法不正确的是
xC + PF6-+Li+ +Al。该电池放电时的工作原理如图所示。下列说法不正确的是
 xC + PF6-+Li+ +Al。该电池放电时的工作原理如图所示。下列说法不正确的是
xC + PF6-+Li+ +Al。该电池放电时的工作原理如图所示。下列说法不正确的是
| A.放电时,B极的电极反应为LiAl-e-=Li+ +Al |
| B.Li2SO4溶液可作该电池的电解质溶液 |
| C.充电时A极的电极反应式为xC + PF6--e-=Cx(PF6) |
| D.该电池放电时,若电路中通过0.01 mol电子,B电极减重0.07 g |
【知识点】 原电池电极反应式书写解读 原电池原理的综合应用解读 新型电池解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
7. 室温下,向100mL饱和的H2S溶液中通入SO2气体(气体体积换算成标准状况),发生反应:2H2S+SO2=3S↓+2H2O,测得溶液pH与通入SO2的关系如图所示。下列有关说法正确的是


| A.整个过程中,水的电离程度逐渐增大 |
| B.该温度下H2S的Ka1数量级为10-7 |
| C.曲线y代表继续通入SO2气体后溶液pH的变化 |
D.a点之后,随SO2气体的通入, 的值始终减小 的值始终减小 |
您最近一年使用:0次
2020-04-20更新
|
473次组卷
|
4卷引用:湖北省襄阳市第五中学,夷陵中学2020届高三下学期联考理综化学试题
二、解答题 添加题型下试题
解答题-工业流程题
|
较难(0.4)
名校
解题方法
8. 锆石(ZrSiO4)酷似钻石且价格低廉,是钻石很好的代用品。天然锆石的主要成分是ZrSiO4,另外还常含有Fe、Al、Cu的氧化物杂质。工业上以天然锆石为原料制备ZrO2的工艺流程如下:
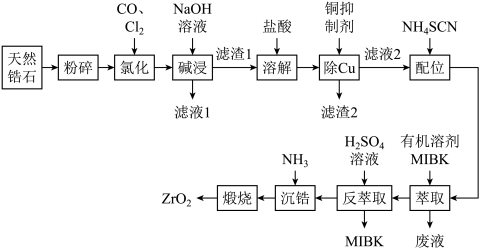
已知:i.氯化过程中除C、O外,其他元素均转化为其最高价氯化物;
ⅱ.Zr在化合物中通常显+4价;ZrC14易溶于水,400 ℃时升华;
ⅲ.“配合”生成的Fe(SCN)3难溶于MIBK,Zr(SCN)4在水中的溶解度小于在MIBK中的溶解度。
(1)将锆石“粉碎”的目的是_______________________________ 。
(2)“氯化”过程中,ZrSiO4发生反应的化学方程式为_______________ ,由下图可知,“氯化”过程选择的最佳反应条件是_________ ;若“氯化”温度过高会导致ZrC14产率降低,原因是________ 。
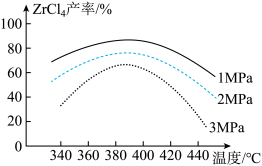
(3)常用的铜抑制剂为NaCN,它可与重金属离子生成沉淀,如Cu(CN)2,其Ksp=4.0×10-10。已知盐酸溶解后的溶液中Cu2+的浓度为1mol·L-1,若溶液中Cu2+的浓度小于等于1.0×10-6mol·L-1时可视为沉淀完全,则Cu2+沉淀完全时溶液中CN-的浓度为________ mol•L-1。
(4)由于NaCN有剧毒,所以需要对“废液”中的NaCN进行处理,通常选用漂白液(有效成分是NaClO)在碱性条件下将其氧化,其产物之一是空气中的主要成分,则上述反应的离子方程式为___________ 。
(5)流程中“萃取”与“反萃取”可以分离铁、富集锆,简述“萃取”的原理:________________ 。

已知:i.氯化过程中除C、O外,其他元素均转化为其最高价氯化物;
ⅱ.Zr在化合物中通常显+4价;ZrC14易溶于水,400 ℃时升华;
ⅲ.“配合”生成的Fe(SCN)3难溶于MIBK,Zr(SCN)4在水中的溶解度小于在MIBK中的溶解度。
(1)将锆石“粉碎”的目的是
(2)“氯化”过程中,ZrSiO4发生反应的化学方程式为

(3)常用的铜抑制剂为NaCN,它可与重金属离子生成沉淀,如Cu(CN)2,其Ksp=4.0×10-10。已知盐酸溶解后的溶液中Cu2+的浓度为1mol·L-1,若溶液中Cu2+的浓度小于等于1.0×10-6mol·L-1时可视为沉淀完全,则Cu2+沉淀完全时溶液中CN-的浓度为
(4)由于NaCN有剧毒,所以需要对“废液”中的NaCN进行处理,通常选用漂白液(有效成分是NaClO)在碱性条件下将其氧化,其产物之一是空气中的主要成分,则上述反应的离子方程式为
(5)流程中“萃取”与“反萃取”可以分离铁、富集锆,简述“萃取”的原理:
您最近一年使用:0次
2020-05-22更新
|
438次组卷
|
3卷引用:四川省乐山市犍为一中2020届高三模拟考试理综化学试题
解答题-实验探究题
|
较难(0.4)
名校
解题方法
9. 硫酸铜是一种常见的化工产品,它在纺织、印染、医药、化工、电镀以及木材和纸张的防腐等方面有极其广泛的用途。实验室制备硫酸铜的步骤如下:
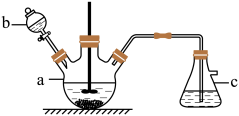
①在仪器a中先加入20 g铜片、60 mL水,再缓缓加入 17 mL浓硫酸;在仪器b中加入39 mL浓硝酸;在仪器c中 加入20%的石灰乳150 mL。
②从仪器b中放出约5 mL浓硝酸,开动搅拌器,然后采用滴加的方式逐渐将浓硝酸加到仪器a中,搅拌器间歇开动。当最后一滴浓硝酸加完以后,完全开动搅拌器,等反应基本停止下来时,开始用电炉加热直至仪器a中的红棕色气体完全消失,立即将导气管从仪器c中取出,再停止加热。
③将仪器a中的液体倒出,取出未反应完的铜片,溶液冷却至室温,析出蓝色晶体。
试回答下列问题:
(1)仪器b的名称为_______ ;将仪器b中液体滴入仪器a中的具体操作是_____________ 。
(2)写出仪器a中反应的化学方程式:________________ 。
(3)步骤②中将导气管先从仪器c中取出再停止加热的目的是____________________ 。
(4)为提高尾气吸收,防止空气污染,下列装置___________ (填字母)适合吸收逸出的气体(反应中产生的气体因来不及被石灰乳吸收而逸出)。
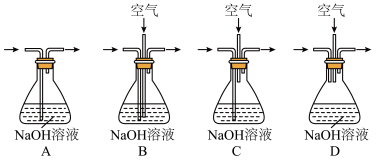
(5)根据表中五水硫酸铜和硝酸铜在不同温度下的溶解度,分析步骤③中溶液冷却至室温析出蓝色晶体的主要原因:_________ 。除去硫酸铜晶体中的少量硝酸铜可采用____________ 方法,检验硝酸铜是否被除净的方法:_____________ 。
(6)本实验采用硝酸氧化法制取硫酸铜,工业上也常采用将铜在450 ℃左右焙烧,再与一定浓度的硫酸反应制取硫酸铜的方法。采用硝酸氧化法的优点在于__________________ 。
(7)用滴定法测定蓝色晶体中Cu2+的含量。取a g试样配成 100 mL 溶液,每次取 20. 00 mL,用 c mol • L-1 EDTA (H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液bmL。 滴定反应为Cu2++ H2Y2-→CuY2-+2H+。计算蓝色晶体中Cu2+质量分数w=____________ 。

①在仪器a中先加入20 g铜片、60 mL水,再缓缓加入 17 mL浓硫酸;在仪器b中加入39 mL浓硝酸;在仪器c中 加入20%的石灰乳150 mL。
②从仪器b中放出约5 mL浓硝酸,开动搅拌器,然后采用滴加的方式逐渐将浓硝酸加到仪器a中,搅拌器间歇开动。当最后一滴浓硝酸加完以后,完全开动搅拌器,等反应基本停止下来时,开始用电炉加热直至仪器a中的红棕色气体完全消失,立即将导气管从仪器c中取出,再停止加热。
③将仪器a中的液体倒出,取出未反应完的铜片,溶液冷却至室温,析出蓝色晶体。
试回答下列问题:
(1)仪器b的名称为
(2)写出仪器a中反应的化学方程式:
(3)步骤②中将导气管先从仪器c中取出再停止加热的目的是
(4)为提高尾气吸收,防止空气污染,下列装置

(5)根据表中五水硫酸铜和硝酸铜在不同温度下的溶解度,分析步骤③中溶液冷却至室温析出蓝色晶体的主要原因:
T/K | 273 | 293 | 313 | 333 | 353 | 373 | |
| 溶解度/ (g/100g) | 五水硫酸铜 | 23.1 | 32.0 | 44.6 | 61.8 | 83.8 | 114.0 |
| 硝酸铜 | 83.5 | 125.0 | 163.0 | 182.0 | 208.0 | 247.0 | |
(7)用滴定法测定蓝色晶体中Cu2+的含量。取a g试样配成 100 mL 溶液,每次取 20. 00 mL,用 c mol • L-1 EDTA (H2Y2-)标准溶液滴定至终点,平均消耗EDTA溶液bmL。 滴定反应为Cu2++ H2Y2-→CuY2-+2H+。计算蓝色晶体中Cu2+质量分数w=
您最近一年使用:0次
解答题-原理综合题
|
较难(0.4)
名校
解题方法
10. 甲醇是一种可再生能源,具有广阔的开发和应用前景,可用Pt/Al2O3、Pd/C、 Rh/SiO2等作催化剂,采用如下反应来合成甲醇:2H2 (g)+CO(g)⇌CH3OH(g)
(1)下表所列数据是各化学键的键能,该反应的ΔH=_______ (用含字母的代数式表示)。
(2)某科研小组用Pd/C作催化剂,在450℃时,研究了n(H):n(CO)分别为2:1、3:1时CO转化率的变化情况(如图),则图中表示n(H2):n(CO)=3:1的变化曲线为______ (填“曲线a"或“曲线b”)。

(3)某化学研究性学习小组模拟工业合成甲醇的反应,在2L的恒容密闭容器内充入1 mol CO和2molH2,加入合适催化剂后在某温度下开始反应,并用压力计监测容器内压强的变化如下:
则从反应开始到20min时,CO的平均反应速率为________ ,该温度下的平衡常数K为_______ .
(4)将CO和H2加入密闭容器中,在一定条件下发生反应:CO(g)+2H2(g) ⇌CH3OH(g) ΔH<0。平衡时CO的体积分数(%)与温度和压强的关系如下图所示(虚线框表示没有测定该条件下的数据)。

T1、T2、T3由大到小的关系是_________ ,判断理由是____________
(5)美国的两家公司合作开发了多孔硅甲醇直接燃料电池,其工作原理如图

①石墨2为__________ (填“正“或“负“)极。
②石墨1极发生的电极反应式为________
(1)下表所列数据是各化学键的键能,该反应的ΔH=
| 化学键 | H-H |  | C-H | C-O | O-H |
| 键能(kJ/mol) | a | b | c | d | e |
(2)某科研小组用Pd/C作催化剂,在450℃时,研究了n(H):n(CO)分别为2:1、3:1时CO转化率的变化情况(如图),则图中表示n(H2):n(CO)=3:1的变化曲线为

(3)某化学研究性学习小组模拟工业合成甲醇的反应,在2L的恒容密闭容器内充入1 mol CO和2molH2,加入合适催化剂后在某温度下开始反应,并用压力计监测容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
则从反应开始到20min时,CO的平均反应速率为
(4)将CO和H2加入密闭容器中,在一定条件下发生反应:CO(g)+2H2(g) ⇌CH3OH(g) ΔH<0。平衡时CO的体积分数(%)与温度和压强的关系如下图所示(虚线框表示没有测定该条件下的数据)。

T1、T2、T3由大到小的关系是
(5)美国的两家公司合作开发了多孔硅甲醇直接燃料电池,其工作原理如图

①石墨2为
②石墨1极发生的电极反应式为
您最近一年使用:0次
2019-05-31更新
|
531次组卷
|
4卷引用:【市级联考】福建省福州市2019届高三第三次质量检测理科综合化学试题
解答题-结构与性质
|
较难(0.4)
名校
解题方法
11. 近年来,在西藏自治区的铜金多金属成矿带多次发现罕见的金属互化物。金属互化物是合金中的一种,可表示为如Cu-Ni-Zn 或CaCux等形式。
(1)某种金属互化物具有自范性,原子在微观空间里呈现周期性的有序排列,该金属互化物属于____________ (填“晶体”或“非晶体”)。
(2)铜在元素周期表中的位置是____________ ,基态Cu原子核外有__________ 种能量不同的电子。
(3)Ni2+能与许多配体形成配合物,如[Ni(CN)4]2-、二丁二酮肟合镍(Ⅱ)等。
①写出一种与CN-互为等电子体的分子:_______________ (用化学式表示)。
②二丁二酮肟合镍(Ⅱ)的结构如图1所示,Ni的配位数为____________ ,配位原子为____________ ,其中C原子的杂化方式为_____________ 。

(4)甲烷、氨气和水分子中的C、N、O原子均采用sp3杂化,VSEPR模型均为正四面体构型,比较三种分子的键角由大到小的顺序为_________ ,其原因是__________ 。
(5)CaCux可看作由如图2所示(a)(b)两种原子层交替堆积排列而成,图(c)表示CaCux晶胞结构图。合金CaCux中x=____________ 。已知同一层中Ca、Ca原子间的距离均为294pm,根据图示求同层的Ca、Ca原子间的距离为____________ pm(取 =1.73,结果保留整数)。
=1.73,结果保留整数)。

(1)某种金属互化物具有自范性,原子在微观空间里呈现周期性的有序排列,该金属互化物属于
(2)铜在元素周期表中的位置是
(3)Ni2+能与许多配体形成配合物,如[Ni(CN)4]2-、二丁二酮肟合镍(Ⅱ)等。
①写出一种与CN-互为等电子体的分子:
②二丁二酮肟合镍(Ⅱ)的结构如图1所示,Ni的配位数为

(4)甲烷、氨气和水分子中的C、N、O原子均采用sp3杂化,VSEPR模型均为正四面体构型,比较三种分子的键角由大到小的顺序为
(5)CaCux可看作由如图2所示(a)(b)两种原子层交替堆积排列而成,图(c)表示CaCux晶胞结构图。合金CaCux中x=
 =1.73,结果保留整数)。
=1.73,结果保留整数)。
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
名校
解题方法
12. 化合物I(4-对羟基苯基-2-丁酮)是国际公认的既安全又获广泛应用的合成香料。由化合物A制备I的一种合成路线如下:

回答下列问题:
(1)A的化学名称为________________ 。
(2)B中的官能团名称是_________________ 。
(3)F的结构简式为_______________ 。
(4)⑤的反应类型是________________ 。
(5)写出满足下列条件的G的同分异构体的结构简式:______________ 。
i.属于芳香族化合物;
ii.既能发生银镜反应,又能发生水解反应;
iii.核磁共振氢谱为三组峰,峰面积比为6︰2︰1。
(6)设计由氯乙烷和丙二酸制备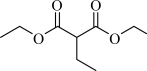 的合成路线:
的合成路线:______ (无机试剂任选)。

回答下列问题:
(1)A的化学名称为
(2)B中的官能团名称是
(3)F的结构简式为
(4)⑤的反应类型是
(5)写出满足下列条件的G的同分异构体的结构简式:
i.属于芳香族化合物;
ii.既能发生银镜反应,又能发生水解反应;
iii.核磁共振氢谱为三组峰,峰面积比为6︰2︰1。
(6)设计由氯乙烷和丙二酸制备
 的合成路线:
的合成路线:
您最近一年使用:0次
2020-05-22更新
|
104次组卷
|
2卷引用:四川省乐山市犍为一中2020届高三模拟考试理综化学试题
试卷分析
整体难度:适中
考查范围:认识化学科学、化学与STSE、化学实验基础、有机化学基础、物质结构与性质、常见无机物及其应用、化学反应原理
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 氧化还原反应基本概念 “白色污染”危害及防治 金属与合金性能比较 化学在农业中的应用 | |
| 2 | 0.85 | 常见无机物的制备 物质制备的探究 | |
| 3 | 0.65 | 根据元素种类、原子个数、有机物类别确定分子式 同分异构体的数目的确定 | |
| 4 | 0.65 | 根据物质性质进行元素种类推断 “位构性”关系理解及应用 | |
| 5 | 0.65 | 氯气与水的反应 溶度积常数与溶解度的关系 物质检验和鉴别的基本方法选择及应用 化学实验方案的设计与评价 | |
| 6 | 0.65 | 原电池电极反应式书写 原电池原理的综合应用 新型电池 | |
| 7 | 0.65 | 影响水电离的因素 弱电解质的电离平衡 弱电解质在水溶液中的电离平衡 电离平衡常数及影响因素 | |
| 二、解答题 | |||
| 8 | 0.4 | 离子方程式的书写 溶度积常数相关计算 物质分离、提纯综合应用 | 工业流程题 |
| 9 | 0.4 | 探究物质组成或测量物质的含量 物质制备的探究 综合实验设计与评价 | 实验探究题 |
| 10 | 0.4 | 根据△H=反应物的键能之和-生成物的键能之和进行计算 化学反应速率计算 化学平衡的有关计算 原电池电极反应式书写 | 原理综合题 |
| 11 | 0.4 | 物质结构与性质综合考查 价层电子对互斥理论 配合物的结构与性质 晶胞的有关计算 | 结构与性质 |
| 12 | 0.4 | 有机物的合成 逆合成分析法 根据题给物质选择合适合成路线 有机推断综合考查 | 有机推断题 |



