9. 碱性锌锰电池的工作原理:Zn+2MnO
2+2H
2O=2MnO(OH)+Zn(OH)
2,其中的电解质溶液是KOH溶液。某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料Mn
xZn
(1-x)Fe
2O
4,其工艺流程如图所示:
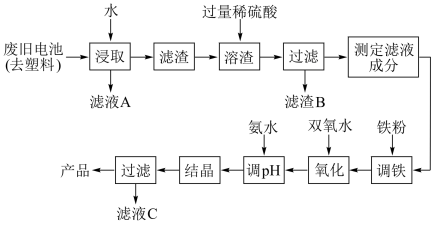
(1)滤液A中溶质的电子式为
____________。
(2)已知Mn
xZn
(1-x)Fe
2O
4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中锰元素的化合价相同,则铁元素的化合价为
_________。
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn
2+,写出该反应的离子方程式:
_____________________________。
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式Mn
xZn
(1-X)Fe
2O
4相符合。
①写出“调铁"工序中发生反应的离子方程式:
_________________,
___________________。
②若测得滤液的成分为c(Mn
2+)+c(Zn
2+)=amol.L
-1,c(Fe
2+)+c(Fe
3+)=bmol.L
-1,滤液体积为1m
3,“调铁”工序中,需加入的铁粉质量为
________kg(忽略溶液体积变化,用含a、b的代数式表示)。
(5)在“氧化"工序中,加入双氧水的目的是把Fe
2+氧化为Fe
3+;生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是
_______________。
(6)用氨水“调pH"后,经“结晶”“过滤”可得到产品和滤液C,从滤液C中还可分离出一种氮肥,该氮肥的溶液中的离子浓度由小到大的顺序为
_____________________。