10. 空间站处理

的一种重要方法是对

进行收集和再生处理,重新生成可供人体呼吸的氧气。其技术路线可分为以下三步:
Ⅰ.固态胺吸收与浓缩

在水蒸气存在下固态胺吸收

反应生成酸式碳酸盐(该反应是放热反应),再解吸出

的简单方法是加热。
Ⅱ.

的加氢甲烷化

还原

制

的部分反应如下:
i.CO
2(g)+H
2(g)

CO(g)+H
2O(g)

ii.CO(g)+3H
2
CH
4(g)+H
2O(g)
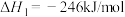
(1)反应CO
2(g)+4H
2(g)

CH
4(g)+2H
2O(g)的
 ___________
___________
。
(2)向恒容绝热的密闭容器中充入amolCO与2amolH
2,进行反应ii,下列能判断反应已达化学平衡状态的是
___________;
a.容器中混合气体密度不变
b.混合气体中
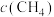
与
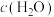
之比不变
c.
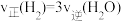
d.容器内温度不变
Ⅲ.和

合成甲烷也是资源化利用的重要方法。对于上述(1)的反应

,催化剂的选择是甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得转化率和生成

选择性随温度变化的影响如下图所示:
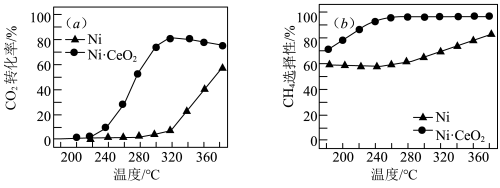
(3)高于320℃后,以Ni为催化剂,

转化率仍在上升,其原因是
___________。
(4)对比上述两种催化剂的催化性能,工业上应选择的催化剂是
___________,使用的合适温度为
___________。
(5)控制起始时
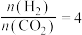
,P=1atm,恒容条件下,若只发生反应i、ii,平衡时各物质的量分数随温度的变化如图所示:
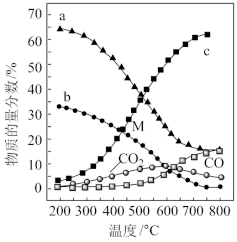
①随投料比增大,CO
2的转化率如何变化
___________(填增大,减小或者不变)。
②图中代表

的曲线是
___________(填“a”、“b”或“c”);温度低于500℃时,CO的物质的量分数约为0,说明此条件下,反应
___________(填“i”或“ii”)化学平衡常数大,反应完全。
③反应CO
2(g)+4H
2(g)

CH
4(g)+2H
2O(g)的平衡常数
 ___________
___________
(用平衡分压代替平衡浓度计算,分压总压物质的量分数)。