河南省洛阳市2020届高三第二次模拟考试理科综合化学试题
河南
高三
二模
2020-10-11
1466次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学反应原理、有机化学基础、物质结构与性质、化学实验基础
河南省洛阳市2020届高三第二次模拟考试理科综合化学试题
河南
高三
二模
2020-10-11
1466次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学反应原理、有机化学基础、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
1. 化学与生产、生活密切相关,下列有关说法正确的是( )
| A.煤的气化、液化与石油的裂化、分馏均为化学变化 |
| B.用K2FeO4处理自来水,既可杀菌消毒又可除去水中悬浮的杂质 |
| C.刚玉、玛瑙、分子筛的主要成分都是含硅化合物 |
| D.泡沫灭火器可用于一般的起火,也适用于电器起火 |
【知识点】 氧化铝 明矾的净水作用及原理解读 化石能源
您最近一年使用:0次
单选题
|
适中(0.65)
名校
2. 设NA为阿伏加 德罗常数的值,下列说法正确的是( )
| A.常温常压下,48gO3,所含的氧原子数为3NA |
| B.等物质的量的P4与CO2所含共价键数目之比为3:1 |
| C.1mol乙酸与足量的C2H518OH充分发生酯化反应可生成CH3CO18OC2H5分子NA个 |
| D.浓度均为1mol/L的醋酸和醋酸钠溶液等体积混合,溶液中CH3COOH和CH3COO-的总数为2NA |
您最近一年使用:0次
2020-10-10更新
|
460次组卷
|
3卷引用:河南省洛阳市2020届高三第二次模拟考试理科综合化学试题
单选题
|
适中(0.65)
名校
3. 下列实验不能达到实验目的的是
| A | B | C | D | |
| 实验 | 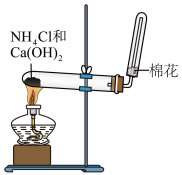 |  |  | 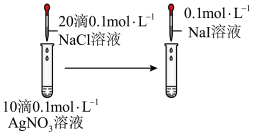 |
| 实验目的 | 实验室制取氨气 | 证明乙炔可使溴水褪色 | 检验蔗糖的水解产物具有还原性 | 证明溶解度: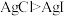 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-06-11更新
|
768次组卷
|
7卷引用:北京市朝阳区2020届高三上学期期末教学统一检测化学试题
北京市朝阳区2020届高三上学期期末教学统一检测化学试题山东省滨州市2020届高三第二次模拟考试(5月)化学试题天津市武清区杨村一中2020届高三模拟考试化学试题河南省洛阳市2020届高三第二次模拟考试理科综合化学试题湖北省2020-2021学年高二3月联考化学试题(已下线)小题06 装置型实验选择题(侧重物质的制备、分离提纯) ——备战2021年高考化学经典小题考前必刷(全国通用)北京市顺义区杨镇第一中学2022-2023学年高三上学期9月阶段性质量检测化学试题
单选题
|
适中(0.65)
4. 有机化学在药物合成中发挥着重要的作用,下列关于药物的说法正确的是( )
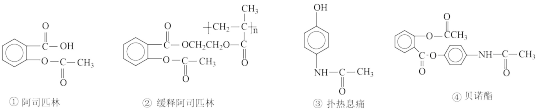

| A.1mol的①与足量NaOH溶液反应,最多可以消耗2molNaOH |
| B.②能够延长药效,1mol②完全水解能够产生1mol① |
| C.③中含有三种官能团,可发生水解反应和酯化反应 |
| D.④可通过阿司匹林与扑热息痛两种药物反应制得 |
您最近一年使用:0次
单选题
|
适中(0.65)
5. 一种新型漂白剂(如图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素。W、Y、Z的最外层电子数之和等于X的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述错误 的是( )
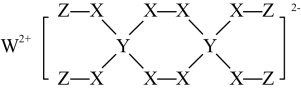

| A.X与Z能够形成两种常见的化合物 |
| B.Y的最高价氧化物对应的水化物为弱酸 |
| C.该漂白剂中X、Y均满足8电子稳定结构 |
| D.工业上通过电解熔融的WX来制得W |
您最近一年使用:0次
单选题
|
较难(0.4)
解题方法
6. 2019年诺贝尔化学奖颁给了三位为锂离子电池发展作出重要贡献的科学家。磷酸铁锂锂离子电池充电时阳极反应式为:LiFePO4–xLi+-xe-→xFePO4+(1-x)LiFePO4。放电工作示意图如图。下列叙述正确的是( )
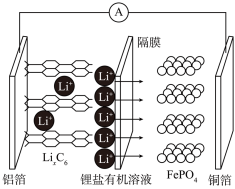
| A.放电时,Li+通过隔膜移向负极 |
| B.充电时,电子从电源经铜箔流入正极材料 |
| C.放电时正极反应为:FePO4+xLi++xe-→xLiFePO4+(1-x)FePO4 |
| D.磷酸铁锂锂离子电池充放电过程通过Li+迁移实现,C、Fe、P元素化合价均不发生变化 |
您最近一年使用:0次
单选题
|
适中(0.65)
7. 在25℃时,甘氨酸在水溶液中解离情况如下:
H3N+CH2COOH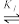 H3N+CH2COO-
H3N+CH2COO-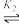 H2NCH2COO-
H2NCH2COO-
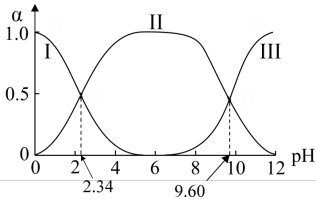
改变溶液pH值,三种甘氨酸相关离子的分布分数α(平衡时某物种的浓度占各物种浓度之和的分数)变化如图所示。当调节溶液的pH值使甘氨酸所带的净电荷为零,此时溶液的pH叫等电点。下列说法正确的是( )
H3N+CH2COOH
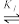 H3N+CH2COO-
H3N+CH2COO-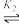 H2NCH2COO-
H2NCH2COO-改变溶液pH值,三种甘氨酸相关离子的分布分数α(平衡时某物种的浓度占各物种浓度之和的分数)变化如图所示。当调节溶液的pH值使甘氨酸所带的净电荷为零,此时溶液的pH叫等电点。下列说法正确的是( )

| A.曲线I、II、III分别代表的微粒为A-、A±、A+ |
| B.pH=4时,c(A±)>c(A-)>c(A+) |
| C.在pH=2.34的溶液中加NaOH溶液,α(A±)+α(A+)+α(A-)保持不变 |
| D.K1=10-9.60,且K1对应的解离基团为—NH2 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
较难(0.4)
解题方法
8. 连二亚硫酸钠(Na2S2O4),也称为保险粉,Na2S2O4)易溶于水,难溶于甲醇,具有极强的还原性,易被空气氧化,在碱性介质中稳定。工业上常用制备Na2S2O4的方法有I.锌粉法、II.甲酸钠法。
I.实验室模拟锌粉法的装置如图(加热等辅助仪器略去)

反应原理为:
Zn+2SO2=ZnS2O4
ZnS2O4+2NaOH=Zn(OH)2↓+Na2S2O4
(1)连接好装置后,首先要检验装置的气密性,方法为___ 。
(2)①装置A中分液漏斗中的试剂是___ 。
A.稀硫酸 B.98%的硫酸 C.70%的硫酸
②装置B中反应结束后,取出混合物进行以下操作,得到Na2S2O4晶体。
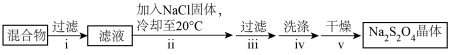
操作ii加入NaCl固体的目的是__ (用平衡移动原理解释),操作iv洗涤中选用的试剂是__ (填“水”或“甲醇”)。
(3)实验室保存新制Na2S2O4晶体的方法是___ 。
II.实验室模拟甲酸钠法的装置如图(加热等辅助仪器略去)

第一步,在F装置中加入甲酸钠、氢氧化钠、甲醇(溶剂)的混合液;
第二步,向装置F中通入二氧化硫;
第三步,75℃加热一段时间,装置中有晶体析出,并产生大量气体:
第四步,过滤、洗涤、干燥,收集产品。
(4)装置F的名称___ ,在其中制备连二亚硫酸钠的离子方程式可表示为___ 。
(5)已知某温度下,H2SO3的电离常数为K1≈1.5×10-2,K2≈1.0×10-7,H2CO3的电离常数为K1ˊ≈4.4×10-7,K2ˊ≈4.7×10-11。装置G用于吸收未反应完的SO2和反应产生的CO2。该温度下当G溶液中HSO 、SO
、SO 离子浓度相等时,溶液的pH约为
离子浓度相等时,溶液的pH约为___ 。
(6)甲酸钠法于1968年实现工业化,继而逐渐替代了锌粉法生产连二亚硫酸钠。与锌粉法相比,甲酸钠法的优点在于___ 。
I.实验室模拟锌粉法的装置如图(加热等辅助仪器略去)

反应原理为:
Zn+2SO2=ZnS2O4
ZnS2O4+2NaOH=Zn(OH)2↓+Na2S2O4
(1)连接好装置后,首先要检验装置的气密性,方法为
(2)①装置A中分液漏斗中的试剂是
A.稀硫酸 B.98%的硫酸 C.70%的硫酸
②装置B中反应结束后,取出混合物进行以下操作,得到Na2S2O4晶体。

操作ii加入NaCl固体的目的是
(3)实验室保存新制Na2S2O4晶体的方法是
II.实验室模拟甲酸钠法的装置如图(加热等辅助仪器略去)

第一步,在F装置中加入甲酸钠、氢氧化钠、甲醇(溶剂)的混合液;
第二步,向装置F中通入二氧化硫;
第三步,75℃加热一段时间,装置中有晶体析出,并产生大量气体:
第四步,过滤、洗涤、干燥,收集产品。
(4)装置F的名称
(5)已知某温度下,H2SO3的电离常数为K1≈1.5×10-2,K2≈1.0×10-7,H2CO3的电离常数为K1ˊ≈4.4×10-7,K2ˊ≈4.7×10-11。装置G用于吸收未反应完的SO2和反应产生的CO2。该温度下当G溶液中HSO
 、SO
、SO 离子浓度相等时,溶液的pH约为
离子浓度相等时,溶液的pH约为(6)甲酸钠法于1968年实现工业化,继而逐渐替代了锌粉法生产连二亚硫酸钠。与锌粉法相比,甲酸钠法的优点在于
您最近一年使用:0次
解答题-工业流程题
|
适中(0.65)
9. 我国是世界上主要产钼国家之一,栾川有“中国钼都”的称号,钼资源十分丰富,以辉钼矿为主。将辉钼矿精矿(主要成分为MoS2,杂质为CaCO3、SiO2、FeS2、CuFeS2、PbS等)除杂提纯可得到粗MoS2,通过精制转化最终可得到纯度更高的MoS2。
已知:
①MoS2具有类似石墨的层状结构,有金属光泽,熔点1185 ℃,密度4.80 g/cm3,硬度很低,被广泛地应用在润滑领域。
②MoS2一般不溶于水、酸、碱和有机溶剂,但溶于王水和煮沸的浓硫酸。在空气中加热至350℃以上开始被氧化,生成钼的氧化物。
③钼元素化合价有+2、+4和+6价等,其中+6价钼最稳定。
有人提出了如图制取高纯MoS2的工艺流程:_______ 。
(2)滤液1中存在的阳离子除H+、Ca2+、Pb2+外,还有_________ 。写出“除杂1”中发生的其中1个有FeCl3参与的氧化还原反应的化学方程式________ 。
(3)“通空气并控温”这步操作的目的是________ 。必须控制好温度的原因_______ 。
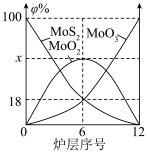
(4)转化1焙烧所用的装置是多层焙烧炉,如图为各炉层固体物料的物质的量的百分数(φ),则x=_______ 。_________ 。
(6)上述流程中,哪些步骤发生了氧化还原反应________ 。
A.除杂1 B.除杂2 C.转化1 D.转化2
E.转化3 F.转化4 G.转化5
(7)上述流程中,可以循环使用的一种物质为_______ (写化学式)。
已知:
①MoS2具有类似石墨的层状结构,有金属光泽,熔点1185 ℃,密度4.80 g/cm3,硬度很低,被广泛地应用在润滑领域。
②MoS2一般不溶于水、酸、碱和有机溶剂,但溶于王水和煮沸的浓硫酸。在空气中加热至350℃以上开始被氧化,生成钼的氧化物。
③钼元素化合价有+2、+4和+6价等,其中+6价钼最稳定。
有人提出了如图制取高纯MoS2的工艺流程:
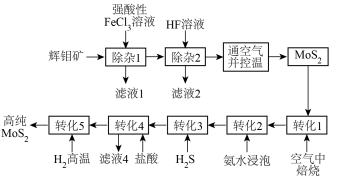
(2)滤液1中存在的阳离子除H+、Ca2+、Pb2+外,还有
(3)“通空气并控温”这步操作的目的是
(4)转化1焙烧所用的装置是多层焙烧炉,如图为各炉层固体物料的物质的量的百分数(φ),则x=
(6)上述流程中,哪些步骤发生了氧化还原反应
A.除杂1 B.除杂2 C.转化1 D.转化2
E.转化3 F.转化4 G.转化5
(7)上述流程中,可以循环使用的一种物质为
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
解题方法
10. 氨在人类的生产生活中有着非常重要的作用,请回答下列有关问题:
(1)已知:2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ·mol-1,查阅文献资料,化学键键能如表:
①氨分解反应NH3(g)
 N2(g)+
N2(g)+ H2(g)的活化能Ea1=300kJ·mol-1,则合成氨反应
H2(g)的活化能Ea1=300kJ·mol-1,则合成氨反应 N2(g)+
N2(g)+  H2(g)
H2(g) NH3(g)的活化能Ea1=
NH3(g)的活化能Ea1=___ 。
②氨气完全燃烧生成氮气和气态水的热化学方程式为___ 。
(2)已知NH3·H2O为一元弱碱。N2H4·H2O为二元弱玻,在水溶液中的一级电离方程式表示为:N2H4·H2O+H2O N2H5·H2O++OH-。则可溶性盐盐酸肼(N2H6Cl2)第一步水解的离子方程式为
N2H5·H2O++OH-。则可溶性盐盐酸肼(N2H6Cl2)第一步水解的离子方程式为___ ;溶液中离子浓度由大到小的排列顺序为___ 。
(3)某实验小组模拟工业合成氨:N2(g)+3H2(g) 2NH3(g)ΔH<0,在一恒温恒容的密闭容器中充入氮气和氢气。
2NH3(g)ΔH<0,在一恒温恒容的密闭容器中充入氮气和氢气。
①t1时刻到达平衡后,在t2时刻改变某一条件,其反应过程如图所示,下列说法正确的是___ 。
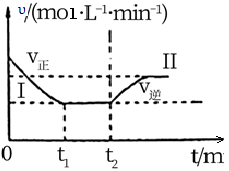
A.I、II两过程到达平衡时,平衡常数:KI<KII
B.I、II两过程到达平衡时,NH3的体积分数:I<II
C.I、II两过程到达平衡的标志:混合气体密度不再发生变化
D.t2时刻改变的条件可以是向密闭容器中加N2和H2混合气
②若向恒容的密闭容器中投入5molN2、15molH2,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。

温度T1、T2、T3大小关系是__ 。M点的平衡常数Kp=___ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,列出计算表达式)。
(4)目前科学家利用生物燃料电池原理(电池工作时MV2+/MV+在电极与酶之间传递电子),研究室温下合成氨并取得初步成果,示意图如图:

①导线中电子移动方向是___ 。
②固氮酶区域发生反应的离子方程式是___ 。
(1)已知:2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ·mol-1,查阅文献资料,化学键键能如表:
| 化学键 | H—H | N N N | N—H |
| E/kJ·mol-1 | 436 | 946 | 391 |
①氨分解反应NH3(g)

 N2(g)+
N2(g)+ H2(g)的活化能Ea1=300kJ·mol-1,则合成氨反应
H2(g)的活化能Ea1=300kJ·mol-1,则合成氨反应 N2(g)+
N2(g)+  H2(g)
H2(g) NH3(g)的活化能Ea1=
NH3(g)的活化能Ea1=②氨气完全燃烧生成氮气和气态水的热化学方程式为
(2)已知NH3·H2O为一元弱碱。N2H4·H2O为二元弱玻,在水溶液中的一级电离方程式表示为:N2H4·H2O+H2O
 N2H5·H2O++OH-。则可溶性盐盐酸肼(N2H6Cl2)第一步水解的离子方程式为
N2H5·H2O++OH-。则可溶性盐盐酸肼(N2H6Cl2)第一步水解的离子方程式为(3)某实验小组模拟工业合成氨:N2(g)+3H2(g)
 2NH3(g)ΔH<0,在一恒温恒容的密闭容器中充入氮气和氢气。
2NH3(g)ΔH<0,在一恒温恒容的密闭容器中充入氮气和氢气。①t1时刻到达平衡后,在t2时刻改变某一条件,其反应过程如图所示,下列说法正确的是

A.I、II两过程到达平衡时,平衡常数:KI<KII
B.I、II两过程到达平衡时,NH3的体积分数:I<II
C.I、II两过程到达平衡的标志:混合气体密度不再发生变化
D.t2时刻改变的条件可以是向密闭容器中加N2和H2混合气
②若向恒容的密闭容器中投入5molN2、15molH2,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示。

温度T1、T2、T3大小关系是
(4)目前科学家利用生物燃料电池原理(电池工作时MV2+/MV+在电极与酶之间传递电子),研究室温下合成氨并取得初步成果,示意图如图:

①导线中电子移动方向是
②固氮酶区域发生反应的离子方程式是
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
解题方法
11. 稀土是重要的战略资源,在目前已探明的稀土储量中,我国居第一。我国已经形成了对全球稀土产业链的统治力,在稀土开采技术方面,我国遥遥领先,无论是美国的芒廷帕斯还是澳大利亚的稀土矿山,均为在我国技术的参与下才能实现产出。我国科学家最早研究的是稀土——钴化合物的结构。请回答下列问题:
(1)钴原子的核外电子排布式为___ ,其M层上共有__ 个不同运动状态的电子。
(2)酞菁钴的结构如图所示。
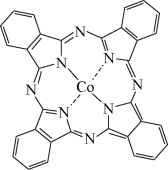
①酞菁钴中C原子的杂化类型是___ 。
②酞菁钴中所含元素原子的第一电离能由小到大的顺序是___ 。
③酞菁钴中三种非金属原子的电负性由大到小的顺序为___ 。
④酞菁钴中N、C原子分别与H原子可形成N2H4和C2H4,试判断其沸点的高低:N2H4__ C2H4(填“>”或“<”),其原因是__ 。
(3)[Co(NH3)6]3+的几何构型与氯化钠晶胞中钠离子占据的空隙类型相同,则其几何构型为___ ,若将[Co(NH3)6]3+中的两个NH3分子换成两个Cl-,可以形成__ 种不同的结构。
(4)稀土钴系(Sm-Co)永磁合金的六方晶胞结构如图所示。已知同一层的Sm-Sm的最近距离为apm,不同层间Sm-Sm的最近距离为bpm。

①Sm-Co永磁合金的化学式为___ 。
②已知阿伏加 德罗常数的值为NA,则该合金的密度ρ为___ g/cm3(列出计算表达式)。
(1)钴原子的核外电子排布式为
(2)酞菁钴的结构如图所示。

①酞菁钴中C原子的杂化类型是
②酞菁钴中所含元素原子的第一电离能由小到大的顺序是
③酞菁钴中三种非金属原子的电负性由大到小的顺序为
④酞菁钴中N、C原子分别与H原子可形成N2H4和C2H4,试判断其沸点的高低:N2H4
(3)[Co(NH3)6]3+的几何构型与氯化钠晶胞中钠离子占据的空隙类型相同,则其几何构型为
(4)稀土钴系(Sm-Co)永磁合金的六方晶胞结构如图所示。已知同一层的Sm-Sm的最近距离为apm,不同层间Sm-Sm的最近距离为bpm。

①Sm-Co永磁合金的化学式为
②已知阿伏加 德罗常数的值为NA,则该合金的密度ρ为
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
名校
解题方法
12. 环丁基甲酸是有机合成中一种有用的中间体。某研究小组以丙烯醛为原料,设计了如图路线合成环丁基甲酸(部分反应条件、产物已省略)。
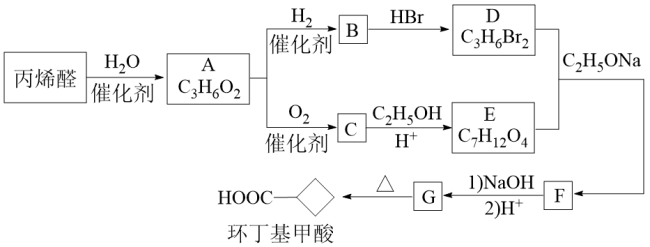
已知:
i.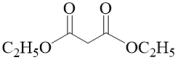 +2RBr
+2RBr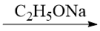
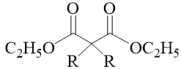 +2HBr
+2HBr
ii.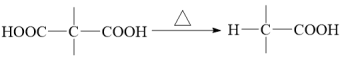 +CO2↑
+CO2↑
请回答下列问题:
(1)化合物A中含有的官能团名称为___ ;由C生成E的反应类型为___ 。
(2)化合物B的结构简式是___ 。
(3)下列说法中正确的是___ (选填字母符号)
A.化合物B和C可通过加聚反应合成高聚物
B.化合物G的分子式为C6H8O4
C.1mol化合物B与足量金属钠反应能生成1mol氢气
D.环丁基甲酸和乙酸属于同系物
(4)写出D+E→F的化学方程式___ 。
(5)写出符合下列条件的G的一种同分异构体的结构简式__ 。
①能使酸性KMnO4溶液褪色
②1mol该物质与足量的NaHCO3反应生成2molCO2
③不存在环状结构
④在1H-NMR谱上显示两组峰,且面积比为3:1
(6)以1,3-丁二烯和E为原料可制备环戊基甲酸(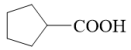 ),请你选用必要试剂,设计并完成下面合成路线
),请你选用必要试剂,设计并完成下面合成路线___ 。
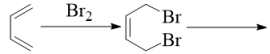

已知:
i.
 +2RBr
+2RBr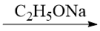
 +2HBr
+2HBrii.
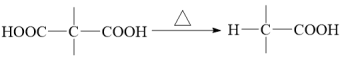 +CO2↑
+CO2↑请回答下列问题:
(1)化合物A中含有的官能团名称为
(2)化合物B的结构简式是
(3)下列说法中正确的是
A.化合物B和C可通过加聚反应合成高聚物
B.化合物G的分子式为C6H8O4
C.1mol化合物B与足量金属钠反应能生成1mol氢气
D.环丁基甲酸和乙酸属于同系物
(4)写出D+E→F的化学方程式
(5)写出符合下列条件的G的一种同分异构体的结构简式
①能使酸性KMnO4溶液褪色
②1mol该物质与足量的NaHCO3反应生成2molCO2
③不存在环状结构
④在1H-NMR谱上显示两组峰,且面积比为3:1
(6)以1,3-丁二烯和E为原料可制备环戊基甲酸(
 ),请你选用必要试剂,设计并完成下面合成路线
),请你选用必要试剂,设计并完成下面合成路线
【知识点】 根据题给物质选择合适合成路线解读 有机推断综合考查解读
您最近一年使用:0次
2020-10-10更新
|
365次组卷
|
3卷引用:河南省洛阳市2020届高三第二次模拟考试理科综合化学试题
试卷分析
导出
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、认识化学科学、化学反应原理、有机化学基础、物质结构与性质、化学实验基础
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 氧化铝 明矾的净水作用及原理 化石能源 | |
| 2 | 0.65 | 阿伏加德罗常数的应用 结合物质结构基础知识与NA相关推算 | |
| 3 | 0.65 | 氨气的实验室制法 溶度积常数与溶解度的关系 乙炔制取实验所得气体的净化及收集 蔗糖水解相关实验 | |
| 4 | 0.65 | 酚类的化学性质 含酯基有机物水解消耗NaOH的量的计算 多官能团有机物的结构与性质 | |
| 5 | 0.65 | 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 “位构性”关系理解及应用 | |
| 6 | 0.4 | 原电池原理 原电池电极反应式书写 新型电池 电解原理 | |
| 7 | 0.65 | 弱电解质的电离平衡 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 | |
| 二、解答题 | |||
| 8 | 0.4 | 二氧化硫与其他强氧化剂的反应 化学平衡的移动及其影响因素 电离平衡常数及影响因素 常见无机物的制备 | 实验探究题 |
| 9 | 0.65 | 氧化还原反应在生活、生产中的应用 物质分离、提纯综合应用 物质制备的探究 | 工业流程题 |
| 10 | 0.65 | 根据△H=反应物的键能之和-生成物的键能之和进行计算 化学平衡图像分析 化学平衡状态的判断方法 原电池原理 | 原理综合题 |
| 11 | 0.65 | 物质结构与性质综合考查 分子的性质 配合物 晶胞的有关计算 | 结构与性质 |
| 12 | 0.4 | 根据题给物质选择合适合成路线 有机推断综合考查 | 有机推断题 |



