福建省福州市第三中学2021届高三下学期第八次质量检测化学试题
福建
高三
阶段练习
2021-03-02
488次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、常见无机物及其应用、化学反应原理、有机化学基础、物质结构与性质、化学实验基础
福建省福州市第三中学2021届高三下学期第八次质量检测化学试题
福建
高三
阶段练习
2021-03-02
488次
整体难度:
适中
考查范围:
化学与STSE、认识化学科学、常见无机物及其应用、化学反应原理、有机化学基础、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
1. 纵观古今,化学与环境、材料、生产、生活关系密切,下列说法不正确的是
| A.“华为麒麟980”手机芯片的主要成分是单质硅 |
| B.蛋白质作为营养物质,在人体内代谢,最终的代谢产物只有水和二氧化碳 |
| C.在阳光照射下,利用水和二氧化碳合成的甲醇属于可再生燃料 |
| D.制作N95型口罩的核心材料是聚丙烯,属于有机高分子材料 |
您最近一年使用:0次
2020-12-30更新
|
243次组卷
|
2卷引用:湖北山东部分重点中学2021届高三12月教学质量联合检测化学试题
单选题
|
适中(0.65)
2. 设 NA 为阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,2.24LNO与1.12LO2混合后气体分子总数为0.1NA |
| B.50 mL 12 mol/L盐酸与足量MnO2加热反应,转移的电子数目为0.3NA |
| C.向含 0.1 molNH4Al(SO4)2的溶液中滴加NaOH溶液至沉淀恰好完全溶解,消耗OH-数目为0.5NA |
| D.电解精炼铜时,若阴极得电子数为2NA,则阳极质量减少64克 |
您最近一年使用:0次
2020-12-28更新
|
161次组卷
|
2卷引用:辽宁省丹东市五校2021届高三12月联考化学试题
单选题
|
适中(0.65)
名校
3. 下列关于有机物的说法不正确的是
A. 和 和 互为同系物 互为同系物 |
B.4-甲基-2-己醇的键线式为: |
| C.分子式为C4H2Cl8的同分异构体有9种 |
| D.甲烷中混有的乙烯可以用溴水除去 |
【知识点】 同系物
您最近一年使用:0次
2021-02-28更新
|
1206次组卷
|
3卷引用:福建省福州市第三中学2021届高三下学期第八次质量检测化学试题
福建省福州市第三中学2021届高三下学期第八次质量检测化学试题(已下线)第1章 认识有机化合物(基础过关卷)-2020-2021学年高二化学选修5章末集训必刷卷(人教版)陕西省延安市富县高级中学2021-2022学年高二上学期期末考试化学试题
单选题
|
较易(0.85)
名校
4. 应用下列实验装置或方案能达到实验目的的是
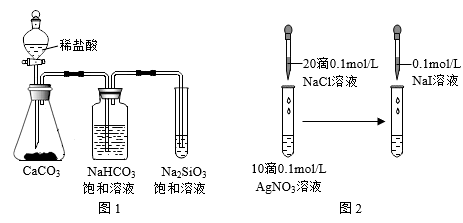



| A.用图1装置,可证明非金属性:C1>C>Si |
| B.用图2装置,可证明:Ksp(AgI)<Ksp(AgC1) |
| C.用图3装置,检验氯化铵受热分解产物 |
| D.用图4装置,制备Fe(OH)2白色沉淀 |
您最近一年使用:0次
2020-12-30更新
|
476次组卷
|
3卷引用:山东省2021届高三12月大联考化学试题
单选题
|
适中(0.65)
名校
解题方法
5. 短周期主族元素R、X、Y、Z的原子序数依次增大,由这些元素组成的物质之间的转化关系如图所示,其中,c、d为单质,a、b、g为二元化合物。b、g分别是10电子分子、18电子分子。下列说法正确的是( )


| A.简单离子半径:Y>Z>X |
| B.e和f含化学键类型相同 |
| C.0.1 mol·L-1的e和f溶液,后者pH较大 |
| D.含X、R、Z三种元素的化合物只有一种 |
【知识点】 盐类水解的原理解读 根据物质性质进行元素种类推断解读
您最近一年使用:0次
2020-11-24更新
|
476次组卷
|
8卷引用:四川省成都实验中学2021届高三上学期10月月考理综化学试题
四川省成都实验中学2021届高三上学期10月月考理综化学试题辽宁省丹东市五校2021届高三12月联考化学试题福建省福州市第三中学2021届高三下学期第八次质量检测化学试题河南省开封市五县联考2020-2021学年高二下学期期末考试化学试题宁夏石嘴山市第三中学2021届高三上学期第三次月考(期末)化学试题(已下线)押新高考卷06题 元素周期表元素周期律-备战2022年高考化学临考题号押题(新高考通版)(已下线)专题卷10 根据元素周期表片段和物质转化关系元素推断-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)湖南省长沙市第一中学2023-2024学年高三上学期月考卷(四)化学试题
单选题
|
适中(0.65)
名校
解题方法
6. 硫化氢空气质子交换膜燃料电池实现了发电、环保的有效结合,已知2H2S(g)+O2(g)=S2(s)+2H2O(l) △H=-632kJ/mol,下列说法正确的是


| A.电极a发生反应为还原反应 |
| B.标准状况下,每11.2LH2S参与反应,有1molH+经固体电解质膜进入正极区 |
| C.当电极a的质量增加64 g时,电池内部释放632 kJ的热能 |
| D.电极b上发生的电极反应为O2+2H2O+4e-=4OH- |
您最近一年使用:0次
2021-06-03更新
|
271次组卷
|
7卷引用:湖北省孝感市云梦县黄香高级中学2021届高三上学期期中考试化学试题
单选题
|
适中(0.65)
名校
7. 某学习小组设计实验制备Ca(NO2)2。实验装置如图所示(夹持装置已略去)。已知:2NO+CaO2=Ca(NO2)2; 2NO2+CaO2=Ca(NO3)2下列说法不正确的是


| A.通入N2是为了排尽装置中的空气 |
| B.装置B、D中的试剂可分别为水和浓硫酸,F装置中的试剂也可使用氢氧化钠溶液 |
| C.若将铜片换成木炭,则不可以制备纯净的亚硝酸钙 |
| D.借助装置A及氢氧化钠溶液和稀硫酸可以分离CO2和CO |
您最近一年使用:0次
2021-02-28更新
|
552次组卷
|
6卷引用:福建省福州市第三中学2021届高三下学期第八次质量检测化学试题
福建省福州市第三中学2021届高三下学期第八次质量检测化学试题黑龙江省哈尔滨市第六中学2020-2021学年高一4月月考化学试题吉林省松原市实验高级中学2021届高三5月月考化学试题内蒙古赤峰市2020-2021学年高二下学期期末考试化学(A)试题湖南省永州市第一中学中2022届高三下学期第二次模拟考试化学试题(已下线)素养卷07 微型物质制备方案设计-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)
单选题
|
适中(0.65)
名校
解题方法
8. 高铁酸钾(K2FeO4)是一种环保、高效、多功能饮用水处理剂,制备流程如图所示:
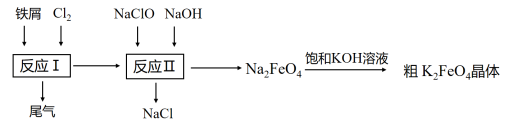
下列叙述不正确的是

下列叙述不正确的是
| A.每生成1molNa2Fe O4反应II中转移电子4mol |
| B.反应I不能在常温下进行 |
| C.反应I中尾气可用FeCl2溶液吸收再利用 |
| D.最后一步能制取K2FeO4的原因可能是相同温度下K2FeO4的溶解度小于Na2FeO4的 |
【知识点】 氧化还原反应有关计算 物质制备的探究解读
您最近一年使用:0次
2021-02-28更新
|
174次组卷
|
7卷引用:江苏省2021届高三百校第二次联考化学试题
9. 下列图象与描述相符的是


A.图甲表示反应 ,保持其他条件不变,改变CO的物质的量,平衡时 ,保持其他条件不变,改变CO的物质的量,平衡时 的体积分数变化情况。由图可知, 的体积分数变化情况。由图可知, 的转化率: 的转化率: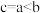 |
B.图乙表示 氧化反应分别在有、无催化剂的情况下反应过程中的能量变化 氧化反应分别在有、无催化剂的情况下反应过程中的能量变化 |
C.图丙是室温下 和 和 的饱和溶液中离子浓度的关系曲线,说明该温度下反应 的饱和溶液中离子浓度的关系曲线,说明该温度下反应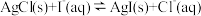 的平衡常数 的平衡常数 |
D.图丁表示炭黑作用下 生成活化氧过程中能量变化情况,说明每活化一个氧分子吸收 生成活化氧过程中能量变化情况,说明每活化一个氧分子吸收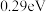 的能量 的能量 |
【知识点】 化学平衡图像分析 转化率的相关计算及判断解读 溶度积常数相关计算解读
您最近一年使用:0次
2020-12-17更新
|
556次组卷
|
6卷引用:江苏省2021届高三百校第二次联考化学试题
江苏省2021届高三百校第二次联考化学试题福建省福州市第三中学2021届高三下学期第八次质量检测化学试题江苏省百校联考2021届高三第二次考试化学试题(已下线)押山东卷第14题 化学反应速率和平衡-备战2021年高考化学临考题号押题(山东卷)江苏省盐城市阜宁中学2021-2022学年高三上学期第二次阶段检测化学试题湖南省株洲市第一中学2022-2023学年高二下学期第一次月考化学试题
单选题
|
适中(0.65)
名校
解题方法
10. 常温下,将等溶液的NaOH溶液分别滴加到等pH、等体积的HA、HB两种弱酸溶液中,溶液的pH与粒子浓度比值的对数关系如图所示。下列叙述错误的是


| A.酸性: HA>HB |
| B.a点时,溶液中由水电离出的c(OH-)约为1×10-10mol·L-1 |
| C.向HB溶液中滴加NaOH溶液至pH=7时:c(B- )> c(HB) |
| D.b点时,c(Na+)>c(B-)= c(HB)> c(H+)>c(OH- ) |
【知识点】 弱电解质的电离平衡 盐溶液中离子浓度大小的比较解读
您最近一年使用:0次
2021-02-28更新
|
165次组卷
|
4卷引用:福建省福州市第三中学2021届高三下学期第八次质量检测化学试题
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
解题方法
11. 工业上可以直接氧化PCl3制备POCl3。某兴趣小组模拟该工艺设计实验装置如下(某些夹持装置、加热装置已略去):
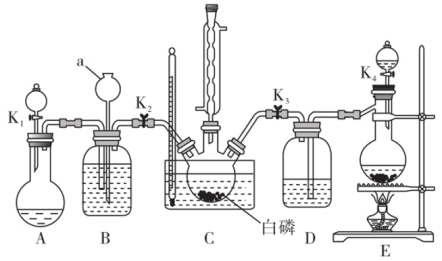
部分物质的性质如下表:
实验步骤如下:
I.连接仪器,检查装置气密性。关闭K1、K2,打开K3、K4,点燃酒精灯制备气体。
II.缓慢向C中通入适量气体至C中白磷消失,熄灭酒精灯。
III.关闭K3、K4,打开K1、K2,A中开始发生反应。
IV.C装置控制反应在60℃~65℃,最终制得POCl3产品。回答下列问题:
(1)B、D装置中盛放的相同试剂是_______ ,B装置的作用有_______ (写出两条)。
(2)仪器a的名称是_______ ,装置E中发生反应的离子方程式为_______ 。
(3)步骤IV控制温度60℃~65℃,其主要目的是_______ 。
(4)该实验装置存在一处明显的设计缺陷,改进方法是_______ 。
(5)通过下面步骤可以测定三氯氧磷产品中Cl的含量:
I.取xg产品于锥形瓶中,加入足量NaOH溶液,产品完全反应后加稀硝酸至酸性。
II.向锥形瓶中加入0.1000mol/L的AgNO3溶液40.00mL,使Cl-完全沉淀。
III.向其中加入20mL硝基苯,振荡,使沉淀表面被有机物覆盖。
IV.加入指示剂,用cmol/LNH4SCN溶液滴定过量Ag+至终点,记下所用体积VmL。
(已知:Ag3PO4溶于酸,Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12)
①滴定选用的指示剂是_______ (填标号)
a.酚酞 b.淀粉 c.NH4Fe(SO4)2 d.甲基橙
②步骤III若不加入硝基苯,所测元素Cl含量将会_______ (填“偏大”、“偏小”或“不变”)。

部分物质的性质如下表:
| 熔点/℃ | 沸点/℃ | 其他 | |
PCl3 | -112 | 75.5 | 遇水生成H3PO3和HCl,遇O2生成POCl3,缓慢通入氧气POCl3产率较高 |
POCl3 | 2 | 105.3 | 遇水生成H3PO4和HCl,能溶于PCl3 |
I.连接仪器,检查装置气密性。关闭K1、K2,打开K3、K4,点燃酒精灯制备气体。
II.缓慢向C中通入适量气体至C中白磷消失,熄灭酒精灯。
III.关闭K3、K4,打开K1、K2,A中开始发生反应。
IV.C装置控制反应在60℃~65℃,最终制得POCl3产品。回答下列问题:
(1)B、D装置中盛放的相同试剂是
(2)仪器a的名称是
(3)步骤IV控制温度60℃~65℃,其主要目的是
(4)该实验装置存在一处明显的设计缺陷,改进方法是
(5)通过下面步骤可以测定三氯氧磷产品中Cl的含量:
I.取xg产品于锥形瓶中,加入足量NaOH溶液,产品完全反应后加稀硝酸至酸性。
II.向锥形瓶中加入0.1000mol/L的AgNO3溶液40.00mL,使Cl-完全沉淀。
III.向其中加入20mL硝基苯,振荡,使沉淀表面被有机物覆盖。
IV.加入指示剂,用cmol/LNH4SCN溶液滴定过量Ag+至终点,记下所用体积VmL。
(已知:Ag3PO4溶于酸,Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2×10-12)
①滴定选用的指示剂是
a.酚酞 b.淀粉 c.NH4Fe(SO4)2 d.甲基橙
②步骤III若不加入硝基苯,所测元素Cl含量将会
您最近一年使用:0次
2020-12-30更新
|
307次组卷
|
4卷引用:湖北山东部分重点中学2021届高三12月教学质量联合检测化学试题
解答题-工业流程题
|
适中(0.65)
名校
解题方法
12. 利用软锰矿和方铅矿(主要成分为PbS,含有FeS2,等杂质)制备PbSO4的工艺流程如图:
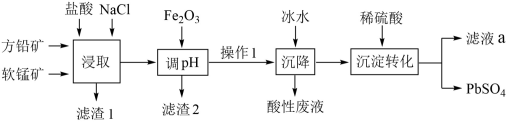
已知: PbCl2(s)+2Cl- (aq) PbCl
PbCl (aq)
(aq)  H>0; Ksp(PbSO4)=1.08x10-8, Ksp (PbCl2)= 1.6x10-5;PbCl2易溶于热水。
H>0; Ksp(PbSO4)=1.08x10-8, Ksp (PbCl2)= 1.6x10-5;PbCl2易溶于热水。
(1)“滤渣1”的成分是S(硫),“浸取”时被氧化的元素是___________ 。
(2)“滤渣2的成分是___________ 。
(3)加入冰水“沉降”的离子方程式为___________ 。
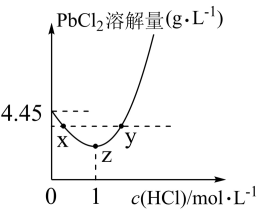
(4)20°C时,PbCl2(s) 在不同浓度的盐酸中的最大溶解量(g L-1 )如图所示。下列叙述正确的是___________ (填字母代号
A.z y,发生了沉淀溶解反应
y,发生了沉淀溶解反应
B.x、y两点对应的溶液中c(Pb2+)相等
C.x z c(Cl- )增大使PbCl2,溶解平衡逆向移动。
z c(Cl- )增大使PbCl2,溶解平衡逆向移动。
D.盐酸浓度越小Ksp (PbCl2)越小
(5)“滤液a”经过处理后可以返回到___________ 工序循环使用; PbCl2经“沉淀转化”后得到PbSO4.,当c(Cl- )=0.1 mol·L-1时,c(SO )=
)=___________ mol·L-1。 (保留三位有效数据)

已知: PbCl2(s)+2Cl- (aq)
 PbCl
PbCl (aq)
(aq)  H>0; Ksp(PbSO4)=1.08x10-8, Ksp (PbCl2)= 1.6x10-5;PbCl2易溶于热水。
H>0; Ksp(PbSO4)=1.08x10-8, Ksp (PbCl2)= 1.6x10-5;PbCl2易溶于热水。(1)“滤渣1”的成分是S(硫),“浸取”时被氧化的元素是
(2)“滤渣2的成分是
(3)加入冰水“沉降”的离子方程式为
(4)20°C时,PbCl2(s) 在不同浓度的盐酸中的最大溶解量(g L-1 )如图所示。下列叙述正确的是

A.z
 y,发生了沉淀溶解反应
y,发生了沉淀溶解反应B.x、y两点对应的溶液中c(Pb2+)相等
C.x
 z c(Cl- )增大使PbCl2,溶解平衡逆向移动。
z c(Cl- )增大使PbCl2,溶解平衡逆向移动。D.盐酸浓度越小Ksp (PbCl2)越小
(5)“滤液a”经过处理后可以返回到
 )=
)=
您最近一年使用:0次
13. CO2是主要的温室气体,以CO2和H2为原料制造更高价值的化学产品是用来缓解温室效应的研究方向,回答下列问题:
(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应I:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1=—51kJ·mol-1
CH3OH(g)+H2O(g) △H1=—51kJ·mol-1
反应II:CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.17kJ·mol-1
CO(g)+H2O(g) △H2=+41.17kJ·mol-1
①已知:键能指断开1mol气态键所吸收的能量或形成1mol气态键所释放的能量。几种化学键的键能如下表所示:
则a=___________ kJ·mol-1;
②若反应II逆反应活化能Ea(逆)为124kJ·mol-1,则该反应的Ea(正)活化能为___________ kJ· mol-1。
(2)向2L容器中充入1molCO2和2molH2,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中CH3OH体积分数如图1所示,测得反应时逆反应速率与容器中c(CH3OH)关系如图II所示:
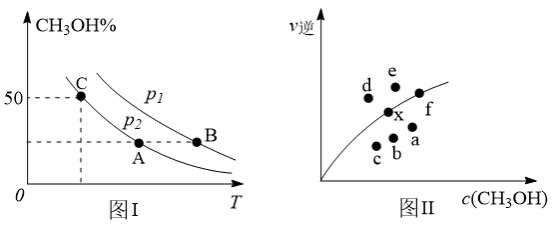
①图I中A、B、C三点对应的平衡常数K(A)、K(B)、K(C)由大到小的顺序排列为___________ ,图I中C点CO2的转化率为___________ 。
②图II中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是___________ 。
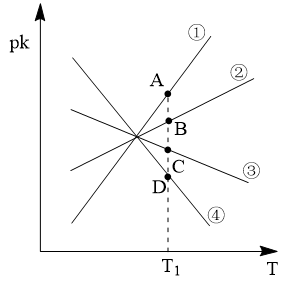
(3)若反应IIICO(g)+H2O(g) CO2(g)+H2(g)的正、逆反应速率分别可表示为v正=k正c(CO)·c(H2O)、v逆=k逆c(CO2)·c(H2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。则下图(pk=-lgk:T表示温度)所示①、②、③、④四条斜线中,能表示以pk正随T变化关系的是斜线
CO2(g)+H2(g)的正、逆反应速率分别可表示为v正=k正c(CO)·c(H2O)、v逆=k逆c(CO2)·c(H2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。则下图(pk=-lgk:T表示温度)所示①、②、③、④四条斜线中,能表示以pk正随T变化关系的是斜线___________ ,能表示pk逆随T变化关系的是斜线___________ ,图中A、B、C、D点的纵坐标分别为a+3、a+1、a-1、a-3,则温度T1时化学平衡常数K=___________ mol-1·L。
(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应I:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H1=—51kJ·mol-1
CH3OH(g)+H2O(g) △H1=—51kJ·mol-1反应II:CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.17kJ·mol-1
CO(g)+H2O(g) △H2=+41.17kJ·mol-1①已知:键能指断开1mol气态键所吸收的能量或形成1mol气态键所释放的能量。几种化学键的键能如下表所示:
| 化学键 | C-H | C-O | H-O(H2O中) | H-O(CH3OH中) | H-H | C=O |
| 键能/kJ· mol-1 | 406 | 351 | 462.5 | 465 | 436 | a |
②若反应II逆反应活化能Ea(逆)为124kJ·mol-1,则该反应的Ea(正)活化能为
(2)向2L容器中充入1molCO2和2molH2,若只发生反应I,测得反应在不同压强、不同温度下,平衡混合物中CH3OH体积分数如图1所示,测得反应时逆反应速率与容器中c(CH3OH)关系如图II所示:

①图I中A、B、C三点对应的平衡常数K(A)、K(B)、K(C)由大到小的顺序排列为
②图II中当x点平衡体系升高至某一温度时,反应可重新达平衡状态,新平衡点可能是
(3)若反应IIICO(g)+H2O(g)
 CO2(g)+H2(g)的正、逆反应速率分别可表示为v正=k正c(CO)·c(H2O)、v逆=k逆c(CO2)·c(H2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。则下图(pk=-lgk:T表示温度)所示①、②、③、④四条斜线中,能表示以pk正随T变化关系的是斜线
CO2(g)+H2(g)的正、逆反应速率分别可表示为v正=k正c(CO)·c(H2O)、v逆=k逆c(CO2)·c(H2),k正、k逆分别为正、逆反应速率常数,c为物质的量浓度。则下图(pk=-lgk:T表示温度)所示①、②、③、④四条斜线中,能表示以pk正随T变化关系的是斜线
【知识点】 化学反应热的计算 化学平衡的有关计算 温度对化学平衡移动的影响解读
您最近一年使用:0次
2020-12-30更新
|
649次组卷
|
5卷引用:山东省2021届高三12月大联考化学试题
山东省2021届高三12月大联考化学试题(已下线)练习6 化学平衡(一)-2020-2021学年【补习教材·寒假作业】高二化学(人教版)福建省福州市第三中学2021届高三下学期第八次质量检测化学试题(已下线)大题07 化学反应原理综合题(二)-【考前抓大题】备战2021年高考化学(全国通用)吉林省松原市实验高级中学2021届高三5月月考化学试题
解答题-结构与性质
|
适中(0.65)
名校
解题方法
14. N、F、Cu及其化合物在化工、医药、材料等方面应用十分广泛。回答下列有关问题:
(1)写出N基态原子核外电子的空间运动状态有___________ 种,与Cu同周期且基态原子核外单电子数与Cu相同的元素还有___________ 种。
(2)常见含氮化合物CH3NH2、(CH3)2NH常温下均为气体,已知甲基的供电子能力强于氢原子,沸点较高的是___________ ,原因是___________ ;NF3中F—N—F键角___________ 比NH3中H—N—H键角。(填大于、小于或等于)
(3)将无水硫酸铜溶解在一定量的水中,再加入过量氨水,溶液变为深蓝色,1mol深蓝色离子[Cu(NH3)4(H2O)2]2+中所含 键为
键为___________ mol(包括配位键)。
(4)氮、铜形成的一种化合物,为立方晶系晶体,晶胞参数为a pm,沿面对角线投影如图所示:

该晶胞中原子的分数坐标为:
Cu:( );(
);( ),(
),( );(
);( );(
);( );(
);( )……
)……
N:(0,0,0):(0,1,1):(1,0,0);(1,1,1);……
则该晶胞中,与Cu原子紧邻的Cu原子有___________ 个,令阿伏加德罗常数的值为NA,该晶体的密度为___________ g/cm3.(列出计算式)
(1)写出N基态原子核外电子的空间运动状态有
(2)常见含氮化合物CH3NH2、(CH3)2NH常温下均为气体,已知甲基的供电子能力强于氢原子,沸点较高的是
(3)将无水硫酸铜溶解在一定量的水中,再加入过量氨水,溶液变为深蓝色,1mol深蓝色离子[Cu(NH3)4(H2O)2]2+中所含
 键为
键为(4)氮、铜形成的一种化合物,为立方晶系晶体,晶胞参数为a pm,沿面对角线投影如图所示:

该晶胞中原子的分数坐标为:
Cu:(
 );(
);( ),(
),( );(
);( );(
);( );(
);( )……
)……N:(0,0,0):(0,1,1):(1,0,0);(1,1,1);……
则该晶胞中,与Cu原子紧邻的Cu原子有
您最近一年使用:0次
2020-12-30更新
|
227次组卷
|
2卷引用:山东省2021届高三12月大联考化学试题
解答题-有机推断题
|
较难(0.4)
名校
解题方法
15. 药物瑞德西韦( )对2019年新型冠状病毒(NCP)有明显抑制作用;K为药物合成的中间体,其合成路线如下:
)对2019年新型冠状病毒(NCP)有明显抑制作用;K为药物合成的中间体,其合成路线如下:
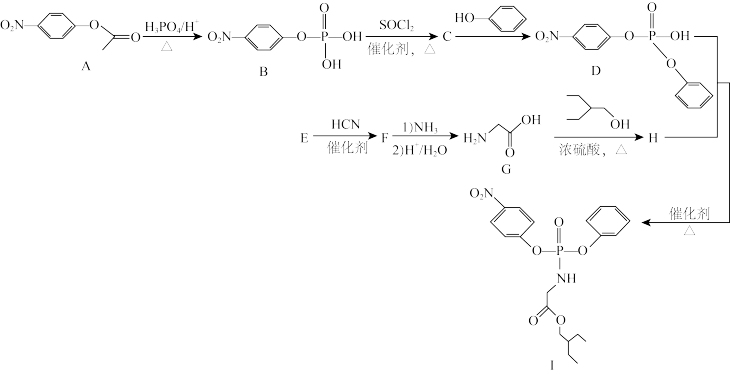
已知:
①
②
回答下列问题:
(1)H中官能团的名称为_______ 。
(2)E→F的反应类型为_______ 。
(3)由C生成D的过程中可能存在的副产物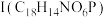 的结构简式为
的结构简式为_______ 。
(4)X是A同分异构体,写出满足下列条件的X的结构简式:_______ 。
①含有硝基的芳香族化合物;
②既能发生水解反应,又能发生银镜反应;
③核磁共振氢谱有四组峰。
(5)设计由苯甲醛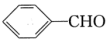 为原料制备化合物
为原料制备化合物 的合成路线
的合成路线_______ (无机试剂任选)。
 )对2019年新型冠状病毒(NCP)有明显抑制作用;K为药物合成的中间体,其合成路线如下:
)对2019年新型冠状病毒(NCP)有明显抑制作用;K为药物合成的中间体,其合成路线如下:
已知:
①

②

回答下列问题:
(1)H中官能团的名称为
(2)E→F的反应类型为
(3)由C生成D的过程中可能存在的副产物
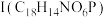 的结构简式为
的结构简式为(4)X是A同分异构体,写出满足下列条件的X的结构简式:
①含有硝基的芳香族化合物;
②既能发生水解反应,又能发生银镜反应;
③核磁共振氢谱有四组峰。
(5)设计由苯甲醛
 为原料制备化合物
为原料制备化合物 的合成路线
的合成路线
您最近一年使用:0次
2020-12-17更新
|
510次组卷
|
3卷引用:江苏省2021届高三百校第二次联考化学试题
试卷分析
整体难度:适中
考查范围:化学与STSE、认识化学科学、常见无机物及其应用、化学反应原理、有机化学基础、物质结构与性质、化学实验基础
试卷题型(共 15题)
题型
数量
单选题
10
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 化学科学对人类文明发展的意义 化学对材料制造和应用的作用 光导纤维与硅芯片 | |
| 2 | 0.65 | 阿伏加德罗常数的应用 氯气的实验室制法 电解池有关计算 | |
| 3 | 0.65 | 同系物 | |
| 4 | 0.85 | 沉淀转化 元素金属性、非金属性强弱探究实验 化学实验方案的设计与评价 | |
| 5 | 0.65 | 盐类水解的原理 根据物质性质进行元素种类推断 | |
| 6 | 0.65 | 原电池电极反应式书写 燃料电池原理及优点 原电池有关计算 | |
| 7 | 0.65 | 一氧化氮的化学性质 硝酸的强氧化性 | |
| 8 | 0.65 | 氧化还原反应有关计算 物质制备的探究 | |
| 9 | 0.65 | 化学平衡图像分析 转化率的相关计算及判断 溶度积常数相关计算 | |
| 10 | 0.65 | 弱电解质的电离平衡 盐溶液中离子浓度大小的比较 | |
| 二、解答题 | |||
| 11 | 0.65 | 氯气的实验室制法 铁盐的检验 探究物质组成或测量物质的含量 物质制备的探究 | 实验探究题 |
| 12 | 0.65 | 溶度积常数相关计算 物质制备的探究 | 工业流程题 |
| 13 | 0.4 | 化学反应热的计算 化学平衡的有关计算 温度对化学平衡移动的影响 | 原理综合题 |
| 14 | 0.65 | 核外电子排布的表示形式 共价键对分子构型、性质的影响 配合物 晶胞的有关计算 | 结构与性质 |
| 15 | 0.4 | 逆合成分析法 根据题给物质选择合适合成路线 有机合成综合考查 信息给予的有机合成 | 有机推断题 |



