某温度下,向10mL0.1mol/LCuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中溶液中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示,已知:lg2=0.3,Ksp(ZnS)=3×10-25mol2/L2,下列有关说法正确的是( )
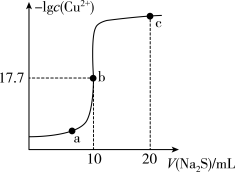

| A.a、b、c三点中,水的电离程度最大的为b点 |
| B.如不考虑CuS的溶解,则c点溶液有:2[c(S2-)+c(HS-)+c(H2S)]═c(Cl-) |
| C.该温度下Ksp(CuS)=2×10-18mol2/L2 |
D.该温度下,反应: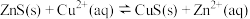 的平衡常数为 的平衡常数为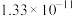 |
更新时间:2020-06-18 21:17:38
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】25℃时,某物质的溶液中,由水电离出的c(H+)=1×10-5 mol/L,下列说法正确的是
| A.该溶液的溶质可能是NaOH | B.该溶液溶质可能是NaHSO4 |
| C.该溶液的溶质可能是HNO3 | D.该溶液的溶质可能是CH3COONa |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃时,向 溶液中加入KOH固体,混合溶液的pH随
溶液中加入KOH固体,混合溶液的pH随 以及
以及  的关系如图所示(忽略溶液体积变化和
的关系如图所示(忽略溶液体积变化和 的挥发)。下列有关叙述错误的是
的挥发)。下列有关叙述错误的是

 溶液中加入KOH固体,混合溶液的pH随
溶液中加入KOH固体,混合溶液的pH随 以及
以及  的关系如图所示(忽略溶液体积变化和
的关系如图所示(忽略溶液体积变化和 的挥发)。下列有关叙述错误的是
的挥发)。下列有关叙述错误的是
A. 是一种二元弱酸,其 是一种二元弱酸,其 约为 约为 |
B.从a点到c点,水电离的 先减小后增大 先减小后增大 |
C.b点有关微粒浓度大小关系为  |
D. 时, 时,  |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】将标准状况下1.12LCO2 通入含有3gNaOH的水溶液中,完全反应并得到1L碱性溶液,则对于该溶液表述正确的是( )
| A.2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)] |
| B.c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
| C.HCO3-的电离程度大于HCO3-的水解程度 |
| D.该溶液中存在的平衡体系只有:HCO3-+H2O ⇋ H2CO3+OH-,HCO3-⇋H++CO32- |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】电位滴定法是靠电极电位的突变来指示滴定终点。在滴定过程中,计算机对数据自动采集、处理,并利用滴定反应化学计量点前后电位突变的特性,自动寻找滴定终点。室温时,用0.1000mol/L的NaOH标准溶液滴定同浓度的NH4HSO4溶液,计算机呈现的滴定曲线如图所示(稀溶液中不考虑氨水的分解导致氨的逸出),已知Kb(NH3·H2O)=1.8×10-5,下列说法不正确的是


A.a点溶液中n( )=3.0×10-4mol )=3.0×10-4mol |
B.b点溶液中:c( )+c(H+)—c(Na+)=c(OH—) )+c(H+)—c(Na+)=c(OH—) |
| C.常温时,c点溶液中pH<7 |
| D.b、d点水的电离程度:b>d |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度下,分别向10.00 mL0.1 mol·L-1的KCl和K2CrO4溶液中滴加0.1 mol·L-1AgNO3溶液,滴加过程中-lgc(M)(M为Cl-或 )与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。已知铬酸银是深红色晶体,下列说法正确的是
)与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。已知铬酸银是深红色晶体,下列说法正确的是
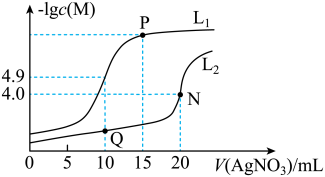
 )与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。已知铬酸银是深红色晶体,下列说法正确的是
)与AgNO3溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。已知铬酸银是深红色晶体,下列说法正确的是
| A.该温度下,Ksp(Ag2CrO4)=4.0×10-9.8 |
| B.曲线L2表示-lgc(Cl- )与V(AgNO3)的变化关系 |
C.P点溶液中:c(K+ )>c( )>c(Ag+ )>c(H+ )>c(OH-) )>c(Ag+ )>c(H+ )>c(OH-) |
| D.若向等浓度的KCl和K2CrO4的混合溶液中滴加硝酸银溶液,则先出现白色沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度下,CuS和 饱和溶液中pS和pM的关系如图所示,其中
饱和溶液中pS和pM的关系如图所示,其中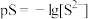 ,
, ,
,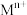 为
为 或
或 ,下列说法错误的是
,下列说法错误的是

 饱和溶液中pS和pM的关系如图所示,其中
饱和溶液中pS和pM的关系如图所示,其中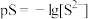 ,
, ,
,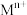 为
为 或
或 ,下列说法错误的是
,下列说法错误的是
A.曲线Ⅱ代表的是 | B.a=48 |
C.此温度下CuS的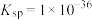 | D.此温度下的饱和溶液中 |
您最近一年使用:0次

 作为沉淀剂除去工业废水中的
作为沉淀剂除去工业废水中的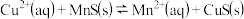 。已知
。已知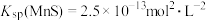 ,
,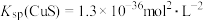 。下列叙述错误的是
。下列叙述错误的是 的溶解度
的溶解度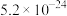
 、
、 也可以用作沉淀剂
也可以用作沉淀剂 固体,
固体,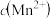 变大
变大

