T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C的变化如图所示。
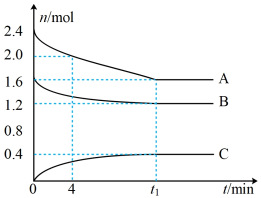
(1)写出反应的化学方程式______ 。
(2)0~4min时,A的平均反应速率为______ 。
(3)已知:K(300℃)>K(350℃),该反应是______ (填“吸热”或“放热”)反应。
(4)T℃时,反应的平衡常数为______ (保留到小数点后2位)。
(5)到达平衡时B的转化率为______ 。
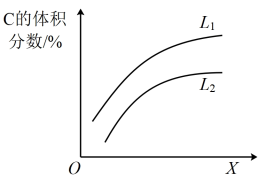
(6)如图是上述反应平衡混合气中C的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是______ (填“温度”或“压强”)。判断L1_____ L2(填“>”或“<”),理由是_____ 。

(1)写出反应的化学方程式
(2)0~4min时,A的平均反应速率为
(3)已知:K(300℃)>K(350℃),该反应是
(4)T℃时,反应的平衡常数为
(5)到达平衡时B的转化率为
(6)如图是上述反应平衡混合气中C的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。其中X代表的是

更新时间:2020-11-09 17:11:16
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】t℃时,将3mol A和1mol B气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g) xC(g),△H<0;在2min时反应达到平衡状态(温度不变)剩余了0.8molB,并测得C的浓度为0.4mol·L—1,请填写下列空白:
xC(g),△H<0;在2min时反应达到平衡状态(温度不变)剩余了0.8molB,并测得C的浓度为0.4mol·L—1,请填写下列空白:
(1)从开始反应至达到平衡状态,生成B的平均反应速率为_____________ 。
(2)x=__________ ,平衡常数K=_________ ,A的转化率为_____________ 。
(3)若继续向原平衡混合物的容器中通入少量氦气(假设氦气和A、B、C都不反应)后,化学平衡(填字母)________________ 。
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(4)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应该满足的关系式为______________ 。
 xC(g),△H<0;在2min时反应达到平衡状态(温度不变)剩余了0.8molB,并测得C的浓度为0.4mol·L—1,请填写下列空白:
xC(g),△H<0;在2min时反应达到平衡状态(温度不变)剩余了0.8molB,并测得C的浓度为0.4mol·L—1,请填写下列空白:(1)从开始反应至达到平衡状态,生成B的平均反应速率为
(2)x=
(3)若继续向原平衡混合物的容器中通入少量氦气(假设氦气和A、B、C都不反应)后,化学平衡(填字母)
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(4)如果上述反应在相同温度和容器中进行,欲使反应达到平衡时C的物质的量分数与原平衡相等,起始加入的三种物质的物质的量n(A)、n(B)、n(C)之间应该满足的关系式为
您最近一年使用:0次
【推荐2】甲醇是重要的化工原料,可用于制备丙烯、氢气等。
(1)MTO法由甲醇制备丙烯时的反应原理是:甲醇先脱水生成二甲醚,然后二甲醚与甲醇的平衡混合物脱水转化为含丙烯较多的低聚烯烃。某温度下,在密闭容器中加入CH3OH气体,发生脱水反应:2CH3OH(g) CH3OCH3(g)+H2O(g),一段时间后测得各组分的浓度如表所示。
CH3OCH3(g)+H2O(g),一段时间后测得各组分的浓度如表所示。
该温度下,反应的平衡常数数值是___ ,CH3OH的平衡转化率是___ 。
(2)利用甲醇水蒸气重整制氢法是获得氢气的重要方法。反应原理如下:
反应i(主反应):CH3OH(g)+H2O(g) CO2(g)+3H2(g)△H=+49kJ•mol-1
CO2(g)+3H2(g)△H=+49kJ•mol-1
反应ii(副反应):H2(g)+CO2(g) CO(g)+H2O(g)△H=+41kJ•mol-1
CO(g)+H2O(g)△H=+41kJ•mol-1
①温度高于300℃则会同时发生CH3OH转化为CO和H2的副反应,该反应的热化学方程式是___ 。
②反应中,经常使用催化剂提高化学反应速率,但催化剂对反应具有选择性。一定条件下,测得CH3OH转化率及CO、CO2选择性随温度变化情况分别如图所示(CO、CO2的选择性:转化的CH3OH中生成CO、CO2的百分比)。
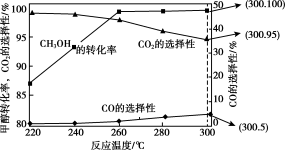
从图中可知,反应的适宜温度为___ ,随着温度的升高,催化剂对___ (填“反应i”或“反应ii”)的选择性越低。
③TiO2纳米电极电化学还原法可将副产物CO2在酸性水溶液中电解生成甲醇,生成甲醇的电极反应式是___ 。
(1)MTO法由甲醇制备丙烯时的反应原理是:甲醇先脱水生成二甲醚,然后二甲醚与甲醇的平衡混合物脱水转化为含丙烯较多的低聚烯烃。某温度下,在密闭容器中加入CH3OH气体,发生脱水反应:2CH3OH(g)
 CH3OCH3(g)+H2O(g),一段时间后测得各组分的浓度如表所示。
CH3OCH3(g)+H2O(g),一段时间后测得各组分的浓度如表所示。| 物质 | CH3OH | CH3OCH3 | H2O |
| 5min浓度(mol·L-1) | 0.44 | 0.6 | 0.6 |
| 10min浓度mol·L-1) | 0.04 | 0.8 | 0.8 |
| 15min浓度(mol•L-1) | 0.04 | 0.8 | 0.8 |
该温度下,反应的平衡常数数值是
(2)利用甲醇水蒸气重整制氢法是获得氢气的重要方法。反应原理如下:
反应i(主反应):CH3OH(g)+H2O(g)
 CO2(g)+3H2(g)△H=+49kJ•mol-1
CO2(g)+3H2(g)△H=+49kJ•mol-1反应ii(副反应):H2(g)+CO2(g)
 CO(g)+H2O(g)△H=+41kJ•mol-1
CO(g)+H2O(g)△H=+41kJ•mol-1①温度高于300℃则会同时发生CH3OH转化为CO和H2的副反应,该反应的热化学方程式是
②反应中,经常使用催化剂提高化学反应速率,但催化剂对反应具有选择性。一定条件下,测得CH3OH转化率及CO、CO2选择性随温度变化情况分别如图所示(CO、CO2的选择性:转化的CH3OH中生成CO、CO2的百分比)。

从图中可知,反应的适宜温度为
③TiO2纳米电极电化学还原法可将副产物CO2在酸性水溶液中电解生成甲醇,生成甲醇的电极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中发生反应:N2O4(g)  2NO2(g),反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示。
2NO2(g),反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示。
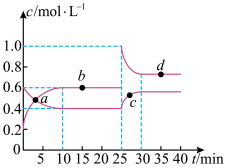
(1)该反应的平衡常数表达式为______________ ,若温度升高K值增大,则该反应的正反应为__________ 反应(填吸热或放热)。
(2)a、b、c、d四个点中,化学反应处于平衡状态的是______________ 点。从起点开始首次达到平衡时以NO2表示的平均反应速率为___________________________ 。
(3)25 min时,增加了______ mol______ (填物质的化学式)使平衡发生了移动。
(4)变化过程中a、b、c、d四个时刻体系的颜色由深到浅的顺序是______ (填字母)。
 2NO2(g),反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示。
2NO2(g),反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示。
(1)该反应的平衡常数表达式为
(2)a、b、c、d四个点中,化学反应处于平衡状态的是
(3)25 min时,增加了
(4)变化过程中a、b、c、d四个时刻体系的颜色由深到浅的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】由CO2与H2制备甲醇是当今研究的热点之一,也是我国科学家2021年发布的由CO2人工合成淀粉(节选途径见图)中的重要反应之一、已知:
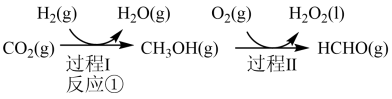
反应②:CO2(g)+H2(g) CO(g)+H2O(g) △H=+40.9kJ•mol-1
CO(g)+H2O(g) △H=+40.9kJ•mol-1
反应③:CH3OH(g) CO(g)+2H2(g) △H=+90.4kJ•mol-1
CO(g)+2H2(g) △H=+90.4kJ•mol-1
某研究小组采用上述催化剂,向密闭容器中通入3molH2和1molCO2,只发生反应①和反应②,在不同条件下达到平衡,在T=300℃下甲醇的物质的量分数φ(CH3OH)随压强P的变化、在p=600kPa下φ(CH3OH)随温度T的变化,如图所示。
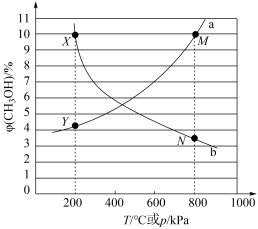
图中M点的φ(CH3OH)高于N点的原因是_____ 。
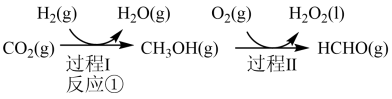
反应②:CO2(g)+H2(g)
 CO(g)+H2O(g) △H=+40.9kJ•mol-1
CO(g)+H2O(g) △H=+40.9kJ•mol-1反应③:CH3OH(g)
 CO(g)+2H2(g) △H=+90.4kJ•mol-1
CO(g)+2H2(g) △H=+90.4kJ•mol-1某研究小组采用上述催化剂,向密闭容器中通入3molH2和1molCO2,只发生反应①和反应②,在不同条件下达到平衡,在T=300℃下甲醇的物质的量分数φ(CH3OH)随压强P的变化、在p=600kPa下φ(CH3OH)随温度T的变化,如图所示。

图中M点的φ(CH3OH)高于N点的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氨是化肥工业和化工生产的主要原料,工业合成氨使用的氢气主要来自合成气( ,
, 混合气体)。回答下列问题:
混合气体)。回答下列问题:
(1)合成氨的热化学方程式为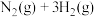


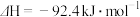 ,升高温度,合成氨反应的平衡常数
,升高温度,合成氨反应的平衡常数_______ (填“增大”“不变”或“减小”)。理论上,为了增大平衡时 的转化率,可采取的措施是
的转化率,可采取的措施是_____ (填字母)。
a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物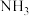
(2)合成氨的原料 可通过反应
可通过反应

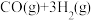
 来获取,已知该反应中,当初始混合气中的
来获取,已知该反应中,当初始混合气中的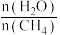 恒定时,温度、压强对平衡混合气中
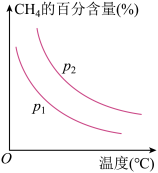
恒定时,温度、压强对平衡混合气中 的百分含量的影响如图所示:
的百分含量的影响如图所示:
图中两条曲线表示压强的关系是:
________  (填“>”“<”或“=”下同),
(填“>”“<”或“=”下同),
________ 0。
(3) 的另外一个反应为
的另外一个反应为

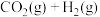
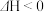 ,一定条件下,反应达到平衡后,采取
,一定条件下,反应达到平衡后,采取______________ 措施可提高 的转化率。
的转化率。
 ,
, 混合气体)。回答下列问题:
混合气体)。回答下列问题:(1)合成氨的热化学方程式为
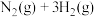


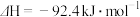 ,升高温度,合成氨反应的平衡常数
,升高温度,合成氨反应的平衡常数 的转化率,可采取的措施是
的转化率,可采取的措施是a.增大压强 b.使用合适的催化剂
c.升高温度 d.及时分离出产物
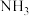
(2)合成氨的原料
 可通过反应
可通过反应

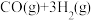
 来获取,已知该反应中,当初始混合气中的
来获取,已知该反应中,当初始混合气中的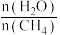 恒定时,温度、压强对平衡混合气中
恒定时,温度、压强对平衡混合气中 的百分含量的影响如图所示:
的百分含量的影响如图所示:图中两条曲线表示压强的关系是:

 (填“>”“<”或“=”下同),
(填“>”“<”或“=”下同),

(3)
 的另外一个反应为
的另外一个反应为

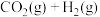
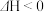 ,一定条件下,反应达到平衡后,采取
,一定条件下,反应达到平衡后,采取 的转化率。
的转化率。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
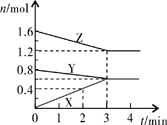
【推荐3】某温度时,在一个2L的密闭容器中,X、Y、Z三种气态物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
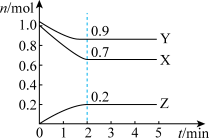
(1)该反应的化学方程式为____
(2)反应开始至2min,以Z表示的平均反应速率为____
(3)该反应为放热反应,能使该反应的反应速率增大的是____
A.及时分离出Z气体 B.适当降低温度 C.增大Y的浓度 D.选择高效催化剂
(4)2min后反应达到平衡,此时容器内混合气体的平均相对分子质量比起始投料时____ (填“增大”“减小”或“相等”)
(5)可以判断上述反应已经达到平衡的是____
A.密闭容器中总压强不变
B.密闭容器中混合气体的密度不变
C.混合气体的平均相对分子质量不再改变
D.n(A):n(B):n(C)等于化学计量系数之比

(1)该反应的化学方程式为
(2)反应开始至2min,以Z表示的平均反应速率为
(3)该反应为放热反应,能使该反应的反应速率增大的是
A.及时分离出Z气体 B.适当降低温度 C.增大Y的浓度 D.选择高效催化剂
(4)2min后反应达到平衡,此时容器内混合气体的平均相对分子质量比起始投料时
(5)可以判断上述反应已经达到平衡的是
A.密闭容器中总压强不变
B.密闭容器中混合气体的密度不变
C.混合气体的平均相对分子质量不再改变
D.n(A):n(B):n(C)等于化学计量系数之比
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】硝酸氯(ClNO)是有机合成中的重要试剂。亚硝酸氯可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+Cl2(g) 2ClNO(g)。
2ClNO(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酸氯,涉及如下反应:
①4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)K1
2NaNO3(s)+2NO(g)+Cl2(g)K1
②2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g)K2
NaNO3(s)+ClNO(g)K2
③2NO(g)+Cl2(g) 2ClNO(g)K3
2ClNO(g)K3
则K1,K2,K3之间的关系为K3=______________ 。
(2)T℃时,2NO(g)+Cl2(g) 2ClNO(g)的正反应速率表达式为v正=kcn(ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为v正=kcn(ClNO),测得速率和浓度的关系如下表:
n=____________ ;k=____________ (注明单位)。
(3)在2L的恒容密闭容器中充入4molNO(g)和2molCl2(g),在不同温度下测得c(ClNO)与时间的关系如图A
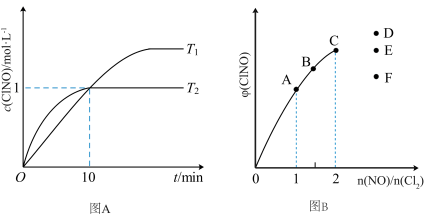
①温度为T1时,能作为该反应达到平衡的标志的有__________ ;
a容器体积保持不变
b容器压强保持不变
c平衡常数K保持不变
d气体颜色保持不变
ev(ClNO)=v(NO)
fNO与ClNO的物质的量比值保持不变
②反应开始到10min时Cl2的平均反应速率v(Cl2)=____________ ;
③温度为T2时,10min已经达到平衡,该反应的平衡常数K=____________ (注明单位)。
(4)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数φ随n(NO)/n(Cl2)的变化图象如图B,则A、B、C三状态中,NO的转化率最小的是__________ 点,当n(NO)/n(Cl2)=2.8时,达到平衡状态ClNO的体积分数φ可能是D、E、F三点中的__________ 点。
 2ClNO(g)。
2ClNO(g)。(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酸氯,涉及如下反应:
①4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+Cl2(g)K1
2NaNO3(s)+2NO(g)+Cl2(g)K1②2NO2(g)+NaCl(s)
 NaNO3(s)+ClNO(g)K2
NaNO3(s)+ClNO(g)K2③2NO(g)+Cl2(g)
 2ClNO(g)K3
2ClNO(g)K3则K1,K2,K3之间的关系为K3=
(2)T℃时,2NO(g)+Cl2(g)
 2ClNO(g)的正反应速率表达式为v正=kcn(ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为v正=kcn(ClNO),测得速率和浓度的关系如下表:| 序号 | c(ClNO)/mol L-1 L-1 | v/mol L-1 L-1 s-1 s-1 |
 | 0.30 | 3.6 10-8 10-8 |
 | 0.60 | 1.44 10-7 10-7 |
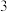 | 0.90 | 3.24 10-7 10-7 |
n=
(3)在2L的恒容密闭容器中充入4molNO(g)和2molCl2(g),在不同温度下测得c(ClNO)与时间的关系如图A

①温度为T1时,能作为该反应达到平衡的标志的有
a容器体积保持不变
b容器压强保持不变
c平衡常数K保持不变
d气体颜色保持不变
ev(ClNO)=v(NO)
fNO与ClNO的物质的量比值保持不变
②反应开始到10min时Cl2的平均反应速率v(Cl2)=
③温度为T2时,10min已经达到平衡,该反应的平衡常数K=
(4)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数φ随n(NO)/n(Cl2)的变化图象如图B,则A、B、C三状态中,NO的转化率最小的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在恒温恒容条件下,将一定量NO2和N2O4的混合气体通入容积为2L的密闭容器中发生反应:N2O4(g)  2NO2(g),反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示。
2NO2(g),反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示。

(1)该反应的平衡常数表达式为______________ ,若温度升高K值增大,则该反应的正反应为__________ 反应(填吸热或放热)。
(2)a、b、c、d四个点中,化学反应处于平衡状态的是______________ 点。从起点开始首次达到平衡时以NO2表示的平均反应速率为___________________________ 。
(3)25 min时,增加了______ mol______ (填物质的化学式)使平衡发生了移动。
(4)变化过程中a、b、c、d四个时刻体系的颜色由深到浅的顺序是______ (填字母)。
 2NO2(g),反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示。
2NO2(g),反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示。
(1)该反应的平衡常数表达式为
(2)a、b、c、d四个点中,化学反应处于平衡状态的是
(3)25 min时,增加了
(4)变化过程中a、b、c、d四个时刻体系的颜色由深到浅的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】现将0.4 mol A气体和0.2 mol B气体充入10 L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量的变化如图:

(1)若t1=10 min,则0至t1时间内C物质的平均反应速率为________ ;该反应在t1时达到平衡,其化学方程式为____________________________________ 。
(2)据图中曲线变化情况分析,t1时刻改变的反应条件可能是________ 。
A.加入了催化剂 B.降低了反应温度
C.向容器中充入了C D.缩小了容器体积

(1)若t1=10 min,则0至t1时间内C物质的平均反应速率为
(2)据图中曲线变化情况分析,t1时刻改变的反应条件可能是
A.加入了催化剂 B.降低了反应温度
C.向容器中充入了C D.缩小了容器体积
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】一定温度下,向1.0L的密闭容器中加入0.60molX(g),发生反应X(g) Y(s)+2Z(g),测得反应物X的浓度与反应时间的关系如表所示:
Y(s)+2Z(g),测得反应物X的浓度与反应时间的关系如表所示:
(1)0~3min内用Z表示的平均反应速度v(Z)=___ 。
(2)分析该反应中反应物的浓度与时间的关系,得出的结论是___ 。由此规律推出在6min时反应物X的浓度为___ mol·L-1。
(3)该反应的逆反应速率随时间变化的曲线如图所示,t2时改变的条件可能是___ 、___ 。

 Y(s)+2Z(g),测得反应物X的浓度与反应时间的关系如表所示:
Y(s)+2Z(g),测得反应物X的浓度与反应时间的关系如表所示:| 反应时间t/min | 0 | 1 | 2 | 3 | 4 | 6 | 8 |
| c(X)/(mol·L-1) | 0.60 | 0.42 | 0.30 | 0.21 | 0.15 | a | 0.0375 |
(1)0~3min内用Z表示的平均反应速度v(Z)=
(2)分析该反应中反应物的浓度与时间的关系,得出的结论是
(3)该反应的逆反应速率随时间变化的曲线如图所示,t2时改变的条件可能是

您最近一年使用:0次

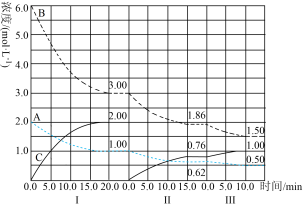
 cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示:
cC(g)(ΔH<0)在等容条件下进行。改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示: