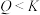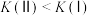下列有关反应M(g)+2N(g) 3G(g)+H(s)的说法正确的是
3G(g)+H(s)的说法正确的是
 3G(g)+H(s)的说法正确的是
3G(g)+H(s)的说法正确的是| A.在体积可变的密闭容器中,该反应达到平衡后,若加压,则平衡不移动、混合气体平均相对分子质量变大、混合气体密度变大 |
| B.若T℃时该反应的平衡常数K=1.0,则在T ℃时在使用催化剂后该反应的K值将大于1.0 |
| C.某温度下,若向已达平衡的该反应体系中加入1molM(g)和2molN(g),则平衡不移动 |
| D.如果该反应在容积不变的密闭容器中进行,当反应达到平衡时v正(N)∶v逆(G)=2∶3 |
2021·上海嘉定·一模 查看更多[1]
更新时间:2020-12-29 08:56:39
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】可逆反应 ,反应过程中,当其它条件不变时,C的百分含量(C%)与温度和压强的关系如下图,下列叙述正确的是
,反应过程中,当其它条件不变时,C的百分含量(C%)与温度和压强的关系如下图,下列叙述正确的是
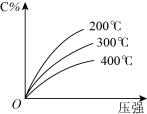
 ,反应过程中,当其它条件不变时,C的百分含量(C%)与温度和压强的关系如下图,下列叙述正确的是
,反应过程中,当其它条件不变时,C的百分含量(C%)与温度和压强的关系如下图,下列叙述正确的是
| A.达平衡后,加入催化剂后C%增大 |
| B.达平衡后,若升温,平衡右移 |
| C.达平衡后,增加A的量有利于平衡向右移动 |
| D.化学方程式中n>e+f |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】在恒容密闭容器中进行的反应:2CO2(g)+6H2(g)⇌C2H5OH(g)+3H2O(g) △H。起始时按不同氢碳比[n(H2)/n(CO2)]投料(起始时加入CO2的物质的量相同,见图中曲线①②③),测得CO2的平衡转化率与温度关系如图所示。下列说法不正确的是


| A.该反应的焓变△H小于0 |
| B.三种条件下起始的氢碳比:①<②<③ |
| C.其他条件不变,缩小容器的体积可提高CO2的转化率 |
| D.控制温度为400K时,曲线③起始CO2浓度为2mol/L,达到平衡时所需时间为5min,则0~5minʋ(H2O)=0.3mol·L-1·min-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】 N2(g)+3H2(g) 2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
2NH3(g) △H<0,反应达平衡时,下列措施能提高N2转化率的是
①降温 ②恒压通入惰性气体 ③增加N2的浓度 ④加压 ⑤催化剂
| A.①④ | B.①②③⑤ | C.②③⑤ | D.③④⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列各组实验所选玻璃仪器和试剂,不能达到实验目的的是(不考虑存放试剂的容器)
| 实验目的 | 玻璃仪器 | 试剂 | |
| A | 测定某NaOH溶液的浓度 | 酸式滴定管、碱式滴定管、烧杯 |  HCl溶液、酚酞试剂、待测NaOH溶液、蒸馏水 HCl溶液、酚酞试剂、待测NaOH溶液、蒸馏水 |
| B | 探究浓度对化学平衡的影响 | 胶头滴管、试管、量筒 | 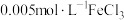 溶液、 溶液、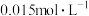 KSCN溶液、 KSCN溶液、 KSCN溶液 KSCN溶液 |
| C | 比较氯、溴、碘的非金属性 | 试管、胶头滴管 | 新制氯水、溴水、NaBr溶液、NaI溶液 |
| D | 验证铁盐的氧化性 | 试管、胶头滴管 |  溶液、KI溶液、淀粉溶液 溶液、KI溶液、淀粉溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】密闭容器中一定量的混合气体发生以下反应: xA(g)+yB(g)⇌zC(g),平衡时测得A的浓度为0.50 mol∙L-1,在温度不变时,把容器容积扩大到原来的2倍,使其重新达到平衡,此时A的浓度为0.30 mol∙L-1,下列叙述正确的是
| A.平衡一定向右移动 | B.B的转化率降低 | C.x+y<z | D.C的体积分数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)  2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
① b<f ② 915℃、2.0 MPa时E的转化率为60% ③ 增大压强平衡左移 ④ K(1000℃)>K(810℃) 上述①~④中正确的有
 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:| 压强/Mpa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
810 | 54.0 | a | b |
915 | c | 75.0 | d |
1000 | e | f | 83.0 |
① b<f ② 915℃、2.0 MPa时E的转化率为60% ③ 增大压强平衡左移 ④ K(1000℃)>K(810℃) 上述①~④中正确的有
| A.4个 | B.3个 | C.2个 | D.1个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在温度一定的条件下,N2(g)+ 3H2(g)  2NH3(g)在密闭容器中反应并达到平衡时,混合气体的平均摩尔质量为M g/mol,N2与NH3的浓度均为c mol·L−1。若将容器的体积压缩为原来的
2NH3(g)在密闭容器中反应并达到平衡时,混合气体的平均摩尔质量为M g/mol,N2与NH3的浓度均为c mol·L−1。若将容器的体积压缩为原来的 ,当达到新的平衡时,下列说法中
,当达到新的平衡时,下列说法中不正确 的是 ( )
 2NH3(g)在密闭容器中反应并达到平衡时,混合气体的平均摩尔质量为M g/mol,N2与NH3的浓度均为c mol·L−1。若将容器的体积压缩为原来的
2NH3(g)在密闭容器中反应并达到平衡时,混合气体的平均摩尔质量为M g/mol,N2与NH3的浓度均为c mol·L−1。若将容器的体积压缩为原来的 ,当达到新的平衡时,下列说法中
,当达到新的平衡时,下列说法中| A.新的平衡体系中,N2的浓度小于2c mol·L−1大于c mol·L−1 |
| B.新的平衡体系中,NH3的浓度小于2c mol·L−1大于cmol·L−1 |
| C.新的平衡体系中,混合体的平均摩尔质量大于M g/mol |
| D.新的平衡体系中,气体密度是原平衡体系的2倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】温度为T时,向容积为2 L的恒容密闭容器中通入NO2,发生反应:2NO2(g) N2O4(g)。实验测得:v正=k正·c2(NO2),v逆=k逆·c(N2O4),k正、k逆为速率常数,受温度的影响,不同时刻测得容器中n(NO2)如图所示。下列说法正确的是
N2O4(g)。实验测得:v正=k正·c2(NO2),v逆=k逆·c(N2O4),k正、k逆为速率常数,受温度的影响,不同时刻测得容器中n(NO2)如图所示。下列说法正确的是

 N2O4(g)。实验测得:v正=k正·c2(NO2),v逆=k逆·c(N2O4),k正、k逆为速率常数,受温度的影响,不同时刻测得容器中n(NO2)如图所示。下列说法正确的是
N2O4(g)。实验测得:v正=k正·c2(NO2),v逆=k逆·c(N2O4),k正、k逆为速率常数,受温度的影响,不同时刻测得容器中n(NO2)如图所示。下列说法正确的是
| A.0~2 s内,该反应的平均速率v(NO2)=0.50 mol·L-1·s-1 |
| B.该温度下,平衡时k正=10k逆 |
| C.其他条件不变,往容器中再通入2 mol NO2,平衡时NO2体积分数增大 |
| D.其他条件不变,移走部分N2O4,则平衡正向移动,平衡常数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
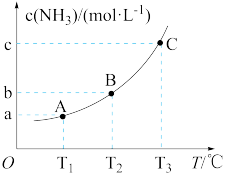
【推荐2】向体积为V1L的密闭容器中充入x mol NH3、x mol NO和y mol O2,x :y=4: 1,模拟SNCR- SCR脱硝技术,主要反应为4NH3(g) +4NO(g) + O2(g)  4N2(g)+ 6H2O(g) △H= -1 632.4 kJ·mol-1,达到平衡时c(NH3)与温度T的关系如下图所示。若T1、T2、T3时的平衡常数分别为K1、K2、K3。下列说法正确的是
4N2(g)+ 6H2O(g) △H= -1 632.4 kJ·mol-1,达到平衡时c(NH3)与温度T的关系如下图所示。若T1、T2、T3时的平衡常数分别为K1、K2、K3。下列说法正确的是
 4N2(g)+ 6H2O(g) △H= -1 632.4 kJ·mol-1,达到平衡时c(NH3)与温度T的关系如下图所示。若T1、T2、T3时的平衡常数分别为K1、K2、K3。下列说法正确的是
4N2(g)+ 6H2O(g) △H= -1 632.4 kJ·mol-1,达到平衡时c(NH3)与温度T的关系如下图所示。若T1、T2、T3时的平衡常数分别为K1、K2、K3。下列说法正确的是
| A.K1<K3 |
B.T2时,若保持温度不变,容器体积由V1 L缩小到V2 L,则平衡后c(N2)小于(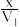 -b)mol·L-1 -b)mol·L-1 |
| C.若保持体系绝热,容积不变,T3时发生反应,平衡后c(NH3)对应的点在C点右下方 |
| D.反应开始后的一段时间内,适当升高温度可提高单位时间内NH3的转化率 |
您最近一年使用:0次


 ,下列叙述正确的是
,下列叙述正确的是 增大
增大
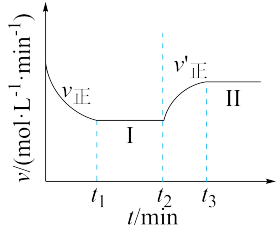
 ,向一恒温恒容的密闭容器中充入1molX和3molY发生反应,
,向一恒温恒容的密闭容器中充入1molX和3molY发生反应, 时达到平衡状态I。在
时达到平衡状态I。在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态II,正反应速率随时间的变化如图所示。下列说法正确的是
时重新达到平衡状态II,正反应速率随时间的变化如图所示。下列说法正确的是