人体血液中存在H2CO3/HCO 等缓冲对。常温下,某水溶液中H2CO3/HCO
等缓冲对。常温下,某水溶液中H2CO3/HCO 缓冲对的微粒浓度之比的对数值
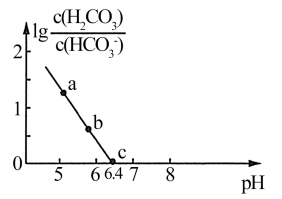
缓冲对的微粒浓度之比的对数值 与pH的关系如图所示。下列说法正确的是
与pH的关系如图所示。下列说法正确的是
 等缓冲对。常温下,某水溶液中H2CO3/HCO
等缓冲对。常温下,某水溶液中H2CO3/HCO 缓冲对的微粒浓度之比的对数值
缓冲对的微粒浓度之比的对数值 与pH的关系如图所示。下列说法正确的是
与pH的关系如图所示。下列说法正确的是
A.H2CO3的电离方程式为H2CO3 2H++CO 2H++CO |
| B.a点→b点的过程中,水的电离程度逐渐减小 |
| C.常温下,H2CO3的第一级电离常数Ka1=1×10-6.4 |
D.c点对应溶液中c(H+)=c(HCO )+c(OH-) )+c(OH-) |
2021·河北·模拟预测 查看更多[3]
2021年河北省高中名校名师原创预测卷化学(第六模拟)(已下线)难点6 水溶液中的四大平衡常数-2021年高考化学专练【热点·重点·难点】(已下线)难点8 水溶液中的四大平衡常数-2021年高考化学【热点·重点·难点】专练(新高考)
更新时间:2021-01-08 16:20:53
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列物质在水溶液中的电离方程式书写正确的是
A.CH3COOH H++CH3COO- H++CH3COO- | B.NaHSO4=Na++HSO |
C.H3PO4 3H++PO 3H++PO | D.NaHCO3 Na++H++CO Na++H++CO |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】柠檬酸是天然防腐剂和食品添加剂,它是一种有机三元弱酸(用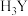 表示),与NaOH溶液反应生成柠檬酸钠。下列说法中正确的是
表示),与NaOH溶液反应生成柠檬酸钠。下列说法中正确的是
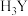 表示),与NaOH溶液反应生成柠檬酸钠。下列说法中正确的是
表示),与NaOH溶液反应生成柠檬酸钠。下列说法中正确的是A.柠檬酸的电离方程式为: |
B.若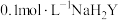 水溶液pH<7,则 水溶液pH<7,则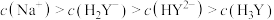 |
C.在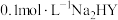 溶液中: 溶液中: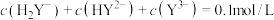 |
D.在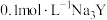 溶液中: 溶液中: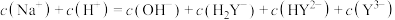 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】NA表示阿伏加 德罗常数的值,下列说法正确的是( )
| A.0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA |
| B.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
| C.1L 0.1mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA |
| D.某电池的总反应为Fe+2Fe3+=3Fe2+,当有5.6gFe溶解时电路中有0.2mol e-通过 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】分子结构修饰是指保持分子的基本结构不变,仅改变分子结构中的某些基团而得到的新分子。分子结构被修饰后,分子的性质发生了改变。已知部分羧酸的分子组成和结构、电离常数如表。下列说法正确的是
| 羧酸 | CH3CH2COOH | CH3COOH | CH2ClCOOH | CF3COOH |
| 电离常数(25℃) | a | b | c | d |
| A.a>b>c>d | B.b>a>c>d | C.c>b>a>d | D.d>c>b>a |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】常温下,向20 mL某浓度的硫酸溶液中滴入0.1 mol·L-1氨水,溶液中水电离的氢离子浓度随加入氨水的体积变化如图。下列分析正确的是
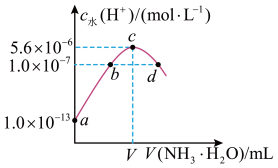

| A.V=40且可用酚酞做指示剂 |
| B.c点所示溶液中:c(H+)-c(OH-)=c(NH3·H2O) |
| C.由图中数据可知NH3·H2O的电离常数K=10-4 |
D.b点溶液呈中性且d点溶液中: |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】常温下取0.1mol/L的NaA和NaB两种盐溶液各1L,分别通入0.02molCO2,发生如下反应:NaA+CO2+H2O=HA+NaHCO3、2NaB+CO2+H2O=2HB+Na2CO3。HA和HB的1L溶液分别加水稀释至体积为VL时可能有如图曲线,则下列说法正确的是


| A.X是HA,M是HB |
| B.常温下pH:NaA溶液>NaB溶液 |
C.常温下,对于 的值(R代表A或B),一定存在HA>HB 的值(R代表A或B),一定存在HA>HB |
| D.若常温下浓度均为0.1mol/L的NaA和HA的混合溶液的pH>7,则c(A-)>c(HA) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】一定温度下,下列溶液的离子浓度关系式正确的是
A.稀释氨水溶液 10 倍后,其 c(OH-)为原来的 |
| B.pH 之和为 14 的 H2C2O4与 NaOH 溶液混合:c(Na+)+c(H+)=c(OH-)+ c(HC2O4-) |
| C.pH=5 的 H2S 溶液中,c(H+)=c(HS-)=1×10-5mol/L |
D.将等物质的量的Na2CO3 和 NaHCO3 混合溶于水中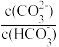 <1 <1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是
 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是A.将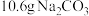 溶于水,溶液中阳离子总数为 溶于水,溶液中阳离子总数为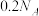 |
B.将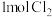 与足量的甲烷在光照条件下充分反应,直至混合气体变为无色,生成 与足量的甲烷在光照条件下充分反应,直至混合气体变为无色,生成 的数目为 的数目为 |
C.向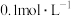 的 的 溶液中通入适量氨气至中性,此时溶液中 溶液中通入适量氨气至中性,此时溶液中 的数目为 的数目为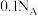 |
D.标准状况下,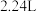 由 由 和 和 组成的混合气体中分子总数为 组成的混合气体中分子总数为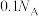 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列说法错误的个数有
①NaHCO3溶液加水稀释,c(Na+)/c( )的比值保持增大
)的比值保持增大
②浓度均为0.1mol·L1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c( )+c(
)+c( )]
)]
③在0.1mol·L1NaOH溶液中滴加0.lmol·L1醋酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH-)=l0-amol·L-1
④pH=3.6的0.1mol/LHX与0.1mol/LNaX的混合溶液中,c(H+)-c(OH-)=c(X-)-c(HX)
⑤ 浓度相等的a、NH4HSO4溶液、b、NH4HCO3溶液、c、NH4Cl溶液,溶液的浓度:a>c>b
浓度相等的a、NH4HSO4溶液、b、NH4HCO3溶液、c、NH4Cl溶液,溶液的浓度:a>c>b
⑥常温下,将pH=10.4的NaOH溶液和pH=3.6的醋酸溶液等体积混合,溶液显酸性
⑦常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1mol·L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
①NaHCO3溶液加水稀释,c(Na+)/c(
 )的比值保持增大
)的比值保持增大②浓度均为0.1mol·L1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(
 )+c(
)+c( )]
)]③在0.1mol·L1NaOH溶液中滴加0.lmol·L1醋酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH-)=l0-amol·L-1
④pH=3.6的0.1mol/LHX与0.1mol/LNaX的混合溶液中,c(H+)-c(OH-)=c(X-)-c(HX)
⑤
 浓度相等的a、NH4HSO4溶液、b、NH4HCO3溶液、c、NH4Cl溶液,溶液的浓度:a>c>b
浓度相等的a、NH4HSO4溶液、b、NH4HCO3溶液、c、NH4Cl溶液,溶液的浓度:a>c>b⑥常温下,将pH=10.4的NaOH溶液和pH=3.6的醋酸溶液等体积混合,溶液显酸性
⑦常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1mol·L-1]:c(Na+)=c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-)
| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 时,有
时,有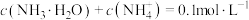 的一组
的一组 、
、 混合溶液,溶液中
混合溶液,溶液中 和
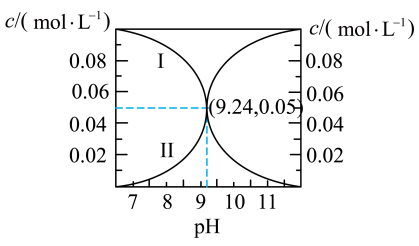
和 与溶液pH的关系如图所示。下列说法错误的是
与溶液pH的关系如图所示。下列说法错误的是
 时,有
时,有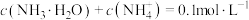 的一组
的一组 、
、 混合溶液,溶液中
混合溶液,溶液中 和
和 与溶液pH的关系如图所示。下列说法错误的是
与溶液pH的关系如图所示。下列说法错误的是
A.曲线Ⅰ表示 |
B. |
C. 时, 时,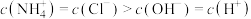 |
D.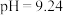 时, 时, |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】室温下,向20mL一定浓度的NaOH溶液中加入一定浓度的HA溶液,溶液的pH、HA和A-的分布分数δ随滴加HA溶液的体积的变化关系如图所示。[δ是组分的平衡浓度占总浓度的分数,如δ(HA)= 。下列说法不正确的是
。下列说法不正确的是

 。下列说法不正确的是
。下列说法不正确的是
| A.水的电离程度a>d |
| B.b点溶液中一定有c(A-)>c(Na+) |
| C.NaOH溶液和HA溶液浓度均约为0.1 mol·L-1 |
| D.该温度下,HA的电离平衡常数K=1.0×10-7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
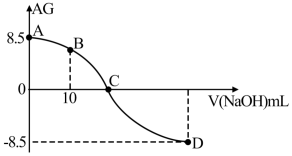
【推荐3】化学上常用AG表示溶液中的 。25℃时,用0.100mol/L的NaOH溶液滴定20.00mL0.100mol/L的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
。25℃时,用0.100mol/L的NaOH溶液滴定20.00mL0.100mol/L的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
 。25℃时,用0.100mol/L的NaOH溶液滴定20.00mL0.100mol/L的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
。25℃时,用0.100mol/L的NaOH溶液滴定20.00mL0.100mol/L的HNO2溶液,AG与所加NaOH溶液的体积(V)的关系如图所示,下列说法不正确的是
| A.HNO2为一元弱酸 |
B.D点溶液的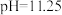 |
| C.C点之前溶液显碱性,C点之后溶液显酸性 |
D.25℃时,HNO2的电离常数 |
您最近一年使用:0次



