化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种。且均符合勒夏特列原理。请回答下列问题。
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g) 4C(g)∆H >0 达到平衡时,c(A)=2mol/L、c(B)=7mol/L、c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是
4C(g)∆H >0 达到平衡时,c(A)=2mol/L、c(B)=7mol/L、c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是_______ ;若改变条件重新达到平衡后,体系中C的质量分数增大,下列措施可行的是_______ 。
A.增加C的物质的量 B.加压 C.升温 D.使用催化剂
(2)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色。分析该溶液遇酚酞呈红色原因(用离子方程式表示)_______ 。
(3)关于小苏打(NaHCO3)溶液的表述错误的是( )
A. c(Na+)=c(HCO )+ c(CO
)+ c(CO )+c(H2CO3)
)+c(H2CO3)
B. c(Na+)+c(H+)=c(HCO )+ 2c(CO
)+ 2c(CO )+c(OH-)
)+c(OH-)
C. HCO 的电离程度大于其水解程度
的电离程度大于其水解程度
D. c(Na+)>c(HCO ) >c(OH-)>c(CO
) >c(OH-)>c(CO )
)
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应A(g)+2B(g)
 4C(g)∆H >0 达到平衡时,c(A)=2mol/L、c(B)=7mol/L、c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是
4C(g)∆H >0 达到平衡时,c(A)=2mol/L、c(B)=7mol/L、c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是A.增加C的物质的量 B.加压 C.升温 D.使用催化剂
(2)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色。分析该溶液遇酚酞呈红色原因(用离子方程式表示)
(3)关于小苏打(NaHCO3)溶液的表述错误的是
A. c(Na+)=c(HCO
 )+ c(CO
)+ c(CO )+c(H2CO3)
)+c(H2CO3)B. c(Na+)+c(H+)=c(HCO
 )+ 2c(CO
)+ 2c(CO )+c(OH-)
)+c(OH-)C. HCO
 的电离程度大于其水解程度
的电离程度大于其水解程度D. c(Na+)>c(HCO
 ) >c(OH-)>c(CO
) >c(OH-)>c(CO )
)
更新时间:2021-01-29 10:04:44
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】二甲醚是一种清洁能源,用水煤气制取甲醚的原理如下:
I、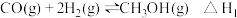
II、
(1)则 的
的
_____ (用 、
、 表示)
表示)
(2)300℃和500℃时,反应I的平衡常数分别为K1、K2,且K1>K2,则其正反应为______ 反应(填“吸热”或“放热”)。
(3)在恒容密闭容器中发生反应I:
①下图能正确反映体系中甲醇体积分数随温度变化情况的曲线是___________ (填“a”或“b”)。
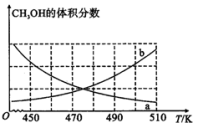
②下列说法能表明反应已达平衡状态的是___________ (填标号)。
A、容器中气体的压强不再变化
B、混合气体的密度不再变化
C、混合气体的平均相对分子质量不再变化
D、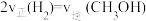
(4)500K时,在2L密闭容器中充入4molCO和8molH2,4min达到平衡,平衡时CO的转化率为80%,且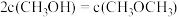 ,则:
,则:
①0~4min,反应I的v(H2)=___________ ,反应I的平衡常数K=___________ 。
②反应II中CH3OH的转化率α=___________ 。
I、
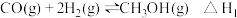
II、

(1)则
 的
的
 、
、 表示)
表示)(2)300℃和500℃时,反应I的平衡常数分别为K1、K2,且K1>K2,则其正反应为
(3)在恒容密闭容器中发生反应I:
①下图能正确反映体系中甲醇体积分数随温度变化情况的曲线是

②下列说法能表明反应已达平衡状态的是
A、容器中气体的压强不再变化
B、混合气体的密度不再变化
C、混合气体的平均相对分子质量不再变化
D、
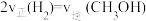
(4)500K时,在2L密闭容器中充入4molCO和8molH2,4min达到平衡,平衡时CO的转化率为80%,且
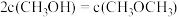 ,则:
,则:①0~4min,反应I的v(H2)=
②反应II中CH3OH的转化率α=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】如何降低大气中CO2的含量及有效地开发利用碳资源的研究越来越紧迫。请运用化学反应原理的相关知识研究碳及其化合物的性质.
(1)工业上在恒容密闭容器中用下列反应合成甲醇:CO(g)+2H2(g)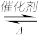 CH3OH(g) △H
CH3OH(g) △H
如表所列数据是反应在不同温度下的化学平衡常数(K)。
①由表中数据判断△H________ 0 ( 填“>”、 “ < “ 或 “ = ”) ;
②判断反应达到平衡状态的依据是________ .
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的平均相对分子质量不变
C.混合气体的密度不变
D.CH3OH、CO、H2的浓度都不再发生变化
③借助上表数据判断,要提高CO的转化率,可采取的措施是________ .
A.升温 B.充入更多H2 C.分离出甲醇 D.加入催化剂
(2)CH3OH可以用做燃料电池的燃料,以甲醇与氧气的反应为原理设计,现有电解质溶液是KOH溶液的燃料电池。请写出该电池负极的电极反应式:____________________ .
(3)向BaSO4沉淀中加入饱和碳酸钠溶液,充分搅拌,弃去上层清液,如此处理多次,可使BaSO4全部转化为BaCO3,发生反应:BaSO4(s)+CO32-(aq)⇌BaCO3(s)+SO42-(aq)。已知某温度下该反应的平衡常数K=4.0×10-2,BaSO4的Ksp=1.0×10-10,则 BaCO3的溶度积Ksp=________________ 。
(1)工业上在恒容密闭容器中用下列反应合成甲醇:CO(g)+2H2(g)
 CH3OH(g) △H
CH3OH(g) △H如表所列数据是反应在不同温度下的化学平衡常数(K)。
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
①由表中数据判断△H
②判断反应达到平衡状态的依据是
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的平均相对分子质量不变
C.混合气体的密度不变
D.CH3OH、CO、H2的浓度都不再发生变化
③借助上表数据判断,要提高CO的转化率,可采取的措施是
A.升温 B.充入更多H2 C.分离出甲醇 D.加入催化剂
(2)CH3OH可以用做燃料电池的燃料,以甲醇与氧气的反应为原理设计,现有电解质溶液是KOH溶液的燃料电池。请写出该电池负极的电极反应式:
(3)向BaSO4沉淀中加入饱和碳酸钠溶液,充分搅拌,弃去上层清液,如此处理多次,可使BaSO4全部转化为BaCO3,发生反应:BaSO4(s)+CO32-(aq)⇌BaCO3(s)+SO42-(aq)。已知某温度下该反应的平衡常数K=4.0×10-2,BaSO4的Ksp=1.0×10-10,则 BaCO3的溶度积Ksp=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】氮的氧化物是大气污染物之一,研究氮氧化物的反应机理对缓解环境污染有重要意义,回答下列问题。
(1)碘蒸气的存在能大幅度提高N2O的分解速率,反应历程为:
第一步:I2(g)→2I(g) (快反应)
第二步:I(g)+N2O(g)→N2(g)+IO(g) (慢反应)
第三步:IO(g)+N2O(g)→N2(g)+O2(g)+I2(g) (快反应)
实验表明:含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是___________
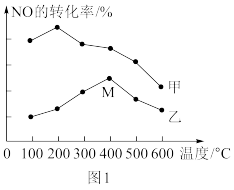
(2)为探究温度及不同催化剂对反应2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH=-746.5kJ/mol的影响,分别在不同温度、不同催化剂下,保持其它初始条件不变重复实验,在相同时间内测得NO转化率与温度的关系如图1所示。在催化剂乙作用下,图中M点对应的速率(对应温度400°C)v(正)
N2(g)+2CO2(g) ΔH=-746.5kJ/mol的影响,分别在不同温度、不同催化剂下,保持其它初始条件不变重复实验,在相同时间内测得NO转化率与温度的关系如图1所示。在催化剂乙作用下,图中M点对应的速率(对应温度400°C)v(正)___________ v(逆)(填“>”、“<”或“=”),温度升高后,两种催化剂条件下NO转化效率均明显降低,原因可能是___________ 。
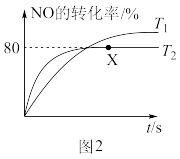
(3)实验发现,NO易发生二聚反应2NO(g) N2O2(g)。向某恒容的容器中充入一定量的NO进行反应,测得温度分别为T1和T2时NO的转化率随时间变化的结果如图2所示。则T1
N2O2(g)。向某恒容的容器中充入一定量的NO进行反应,测得温度分别为T1和T2时NO的转化率随时间变化的结果如图2所示。则T1___________ T2(填“>”、“<”或“=”)。温度为T2时,达到平衡时体系的总压强为200kPa,X点对应的平衡常数Kp=___________ kPa-1(用分压表示);提高NO平衡转化率的条件为___________ (写出其中一点)。
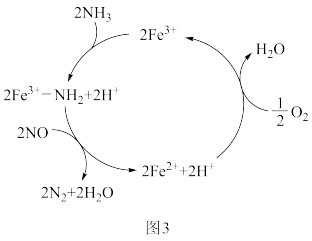
(4)NH3催化还原NO是重要的烟气脱硝技术,研究发现以Fe3+为主体催化剂时可能发生的反应过程如图3,写出脱硝过程总反应的化学方程式:___________ 。
(1)碘蒸气的存在能大幅度提高N2O的分解速率,反应历程为:
第一步:I2(g)→2I(g) (快反应)
第二步:I(g)+N2O(g)→N2(g)+IO(g) (慢反应)
第三步:IO(g)+N2O(g)→N2(g)+O2(g)+I2(g) (快反应)
实验表明:含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是___________
| A.升高温度,第一步向右进行的程度变大 |
| B.第二步的活化能比第三步小 |
| C.IO为反应的催化剂 |
| D.N2O分解反应的速率与是否含碘蒸气有关 |
 N2(g)+2CO2(g) ΔH=-746.5kJ/mol的影响,分别在不同温度、不同催化剂下,保持其它初始条件不变重复实验,在相同时间内测得NO转化率与温度的关系如图1所示。在催化剂乙作用下,图中M点对应的速率(对应温度400°C)v(正)
N2(g)+2CO2(g) ΔH=-746.5kJ/mol的影响,分别在不同温度、不同催化剂下,保持其它初始条件不变重复实验,在相同时间内测得NO转化率与温度的关系如图1所示。在催化剂乙作用下,图中M点对应的速率(对应温度400°C)v(正)
(3)实验发现,NO易发生二聚反应2NO(g)
 N2O2(g)。向某恒容的容器中充入一定量的NO进行反应,测得温度分别为T1和T2时NO的转化率随时间变化的结果如图2所示。则T1
N2O2(g)。向某恒容的容器中充入一定量的NO进行反应,测得温度分别为T1和T2时NO的转化率随时间变化的结果如图2所示。则T1
(4)NH3催化还原NO是重要的烟气脱硝技术,研究发现以Fe3+为主体催化剂时可能发生的反应过程如图3,写出脱硝过程总反应的化学方程式:

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】I.工业上用丙烯与 加成制备1,2-二氯丙烷,主要副产物为3-氯丙烯,反应原理为:
加成制备1,2-二氯丙烷,主要副产物为3-氯丙烯,反应原理为:
①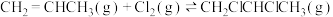
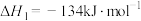
②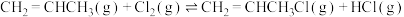
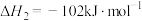
(1)已知 的活化能
的活化能 (逆)为
(逆)为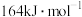 ,则该反应的
,则该反应的 (正)活化能为
(正)活化能为_______  。
。
(2)一定温度下,向恒容密闭容器中充入等物质的量的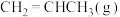 和
和 ,在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
,在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
用单位时间内气体分压的变化来表示反应速率,即 ,则反应①前180min内平均反应速率
,则反应①前180min内平均反应速率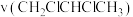 =
=_______ 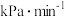
 (保留小数点后2位)。
(保留小数点后2位)。
II.丙烯的制备方法
方法一:丙烷无氧脱氢法制备丙烯反应如下: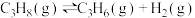
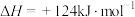
(3)①某温度下,在刚性容器中充入 ,起始压强为10kPa,平衡时总压为14kPa,
,起始压强为10kPa,平衡时总压为14kPa, 的平衡转化率为
的平衡转化率为_______ 。用平衡分压代替平衡浓度,则该反应的平衡常数
_______ kPa
②总压分别为100kPa、10kPa时发生该反应,平衡体系中 和
和 的物质的量分数随温度变化关系如图所示:
的物质的量分数随温度变化关系如图所示:
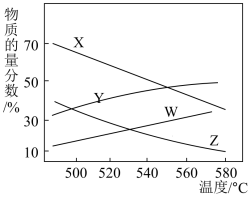
10kPa时, 和
和 的物质的量分数随温度变化关系的曲线分别是
的物质的量分数随温度变化关系的曲线分别是____ 、___ 。
方法二:丙烷氧化脱氢法制备丙烯还生成CO、 等副产物,制备丙烯的反应如下:
等副产物,制备丙烯的反应如下: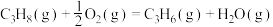
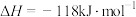 。在催化剂作用下的转化率和
。在催化剂作用下的转化率和 的产率随温度变化关系如图所示。
的产率随温度变化关系如图所示。
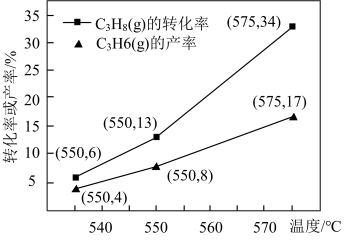
(4)①图中 的转化率随温度升高而上升的原因是
的转化率随温度升高而上升的原因是_______ 。
②575℃时, 的选择性为
的选择性为_______ 。( 的选择性=
的选择性=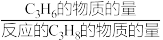 ×100%)
×100%)
 加成制备1,2-二氯丙烷,主要副产物为3-氯丙烯,反应原理为:
加成制备1,2-二氯丙烷,主要副产物为3-氯丙烯,反应原理为:①
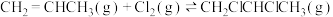
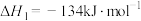
②
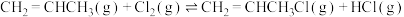
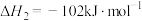
(1)已知
 的活化能
的活化能 (逆)为
(逆)为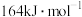 ,则该反应的
,则该反应的 (正)活化能为
(正)活化能为 。
。(2)一定温度下,向恒容密闭容器中充入等物质的量的
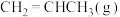 和
和 ,在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。
,在催化剂作用下发生反应①②,容器内气体的压强随时间的变化如下表所示。| 时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
| 压强/kPa | 80 | 74.2 | 69.4 | 65.2 | 61.6 | 57.6 | 57.6 |
 ,则反应①前180min内平均反应速率
,则反应①前180min内平均反应速率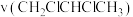 =
=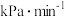
 (保留小数点后2位)。
(保留小数点后2位)。II.丙烯的制备方法
方法一:丙烷无氧脱氢法制备丙烯反应如下:
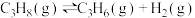
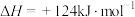
(3)①某温度下,在刚性容器中充入
 ,起始压强为10kPa,平衡时总压为14kPa,
,起始压强为10kPa,平衡时总压为14kPa, 的平衡转化率为
的平衡转化率为
②总压分别为100kPa、10kPa时发生该反应,平衡体系中
 和
和 的物质的量分数随温度变化关系如图所示:
的物质的量分数随温度变化关系如图所示:
10kPa时,
 和
和 的物质的量分数随温度变化关系的曲线分别是
的物质的量分数随温度变化关系的曲线分别是方法二:丙烷氧化脱氢法制备丙烯还生成CO、
 等副产物,制备丙烯的反应如下:
等副产物,制备丙烯的反应如下: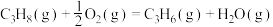
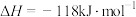 。在催化剂作用下的转化率和
。在催化剂作用下的转化率和 的产率随温度变化关系如图所示。
的产率随温度变化关系如图所示。
(4)①图中
 的转化率随温度升高而上升的原因是
的转化率随温度升高而上升的原因是②575℃时,
 的选择性为
的选择性为 的选择性=
的选择性=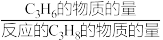 ×100%)
×100%)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】甲醇、乙烯都是重要的有机化工原料,工业上可利用 和
和 在催化剂作用下合成,发生的主要反应有:
在催化剂作用下合成,发生的主要反应有:
ⅰ.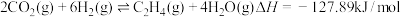
ⅱ.
ⅲ.
(1)上述反应ⅲ中的活化能
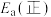
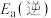 (填“>”或“<”),该反应应选择
(填“>”或“<”),该反应应选择(2)不同压强下
 的平衡转化率与温度的关系如图:
的平衡转化率与温度的关系如图: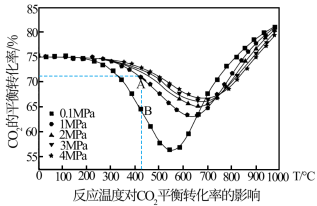
①如图B点
 (填“>”“<”或“=”),在B点给定的温度和压强下,提高
(填“>”“<”或“=”),在B点给定的温度和压强下,提高 平衡转化率的方法有
平衡转化率的方法有
②在恒定压强下,随着温度的升高, 的平衡转化率先降低后升高。表明在较低温度下体系中合成低碳烯烃时
的平衡转化率先降低后升高。表明在较低温度下体系中合成低碳烯烃时
③在较高温度如850℃时, 的平衡转化率随着压强的升高而减小的原因是
的平衡转化率随着压强的升高而减小的原因是
a.温度300~400℃ b.温度900~1000℃ c压强0.1~1.0MPa d.压强2.0~3.0MPa
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】一定温度下,将气体A、B置于固定容积为4L的密闭容器中,发生反应:3A(g)+B(g)  2C(g)+D(g) △H<0。反应进行到10s末,达到平衡,测得A的物质的量为1.6 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+D(g) △H<0。反应进行到10s末,达到平衡,测得A的物质的量为1.6 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示的前10s内正反应的平均反应速率为__________ 。
(2)反应前A的物质的量浓度是__________ 。
(3)10s末,生成物D的物质的量浓度为_______________ ;该温度下,上述反应的平衡常数Kc=_________ (用分数表示),其他条件不变,升高温度,Kc将__________ (填“增大”“减小”或“不变”,下同)。
(4)平衡后,若改变下列条件,生成D的速率将如何变化?
 2C(g)+D(g) △H<0。反应进行到10s末,达到平衡,测得A的物质的量为1.6 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+D(g) △H<0。反应进行到10s末,达到平衡,测得A的物质的量为1.6 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。(1)用C表示的前10s内正反应的平均反应速率为
(2)反应前A的物质的量浓度是
(3)10s末,生成物D的物质的量浓度为
(4)平衡后,若改变下列条件,生成D的速率将如何变化?
| 编号 | 改变的条件 | 生成D的速率 |
| ① | 压缩容器体积 | |
| ② | 恒压下充He(不参与体系反应) | |
| ③ | 恒容下充入Ne(不参与体系反应) |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】某温度下,容积同为2L的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下
(已知某温度下2HI(g) H2 (g)+I2 (g)
H2 (g)+I2 (g)  =+A kJ·mol-1 K=4.0)
=+A kJ·mol-1 K=4.0)
(1)根据上表回答问题
①c1、c3的关系式为_______
②a、b的关系式为__________
③p2、p3的关系式为__________
④a1与a2的关系式为__________
(2)甲容器中:该反应的平衡常数表达式为__________ ;
(3)乙容器中:反应在开始2分钟后达平衡状态,则该反应在这2分钟内用HI表示的平均反应速率为___ mol•L-1•min-1;
(4)丙容器中:反应开始时进行的方向是_____ (填“向左”、“向右”或“不动”)
(5)乙容器中:当反应达到平衡状态后,向容器中再充入1 mol H2,则1分钟后,正反应速率与原平衡时相比___________ 填“增大”、“不变”或“减小”)
(已知某温度下2HI(g)
 H2 (g)+I2 (g)
H2 (g)+I2 (g)  =+A kJ·mol-1 K=4.0)
=+A kJ·mol-1 K=4.0)| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2 mol HI | 1 mol H2 + 1 1mol I2 | 2 mol HI + 1 mol H2 + 1 mol I2 |
HI的浓度(mol·L ) ) | c1 | c2 | c3 |
| 反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 |  |  |  |
(1)根据上表回答问题
①c1、c3的关系式为
②a、b的关系式为
③p2、p3的关系式为
④a1与a2的关系式为
(2)甲容器中:该反应的平衡常数表达式为
(3)乙容器中:反应在开始2分钟后达平衡状态,则该反应在这2分钟内用HI表示的平均反应速率为
(4)丙容器中:反应开始时进行的方向是
(5)乙容器中:当反应达到平衡状态后,向容器中再充入1 mol H2,则1分钟后,正反应速率与原平衡时相比
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】I 用Cl2生产某些含氯有机物时会产生副产物HCl,利用反应A可实现氯的循环利用。反应A:4HCl+O2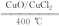 2Cl2+2H2O。
2Cl2+2H2O。
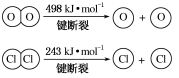
已知:ⅰ反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.
(1)H2O的电子式是______________________ 。
(2)反应A的热化学方程式是_________________________________________________ 。
(3)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为________ kJ,H2O中H—O键比HCl中H—Cl键________ (填“强”或“弱”)。
II 在一定条件下,可逆反应A2(g) + B2(g) 2C(g)达到平衡时,各物质的平衡浓度c(A2)=0.5 mol·L-1、c(B2)=0.1 mol·L-1、c(C)=1.6 mol·L-1,若用a、b、c分别表示A2、B2、C的初始浓度(mol·L-1),则:
2C(g)达到平衡时,各物质的平衡浓度c(A2)=0.5 mol·L-1、c(B2)=0.1 mol·L-1、c(C)=1.6 mol·L-1,若用a、b、c分别表示A2、B2、C的初始浓度(mol·L-1),则:
(1)a、b应满足的关系是________________________________ ;
(2)a的取值范围是________________________________ 。
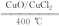 2Cl2+2H2O。
2Cl2+2H2O。已知:ⅰ反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ⅱ.

(1)H2O的电子式是
(2)反应A的热化学方程式是
(3)断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为
II 在一定条件下,可逆反应A2(g) + B2(g)
 2C(g)达到平衡时,各物质的平衡浓度c(A2)=0.5 mol·L-1、c(B2)=0.1 mol·L-1、c(C)=1.6 mol·L-1,若用a、b、c分别表示A2、B2、C的初始浓度(mol·L-1),则:
2C(g)达到平衡时,各物质的平衡浓度c(A2)=0.5 mol·L-1、c(B2)=0.1 mol·L-1、c(C)=1.6 mol·L-1,若用a、b、c分别表示A2、B2、C的初始浓度(mol·L-1),则:(1)a、b应满足的关系是
(2)a的取值范围是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】将2 mol I2(g)和1 mol H2置于某2 L密闭容器中,在一定温度下发生反应:I2(g)+H2(g) 2HI(g) ΔH<0,并达平衡,HI的体积分数φ(HI)随时间变化如图曲线(Ⅱ)所示。
2HI(g) ΔH<0,并达平衡,HI的体积分数φ(HI)随时间变化如图曲线(Ⅱ)所示。
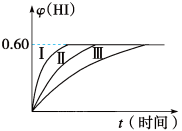
(1)达平衡时,I2(g)的物质的量浓度为_______ 。
(2)若保持温度不变,在另一相同的2 L的密闭容器中加入a mol I2(g)、b mol H2和c mol HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.60,则a、b、c的关系是______ 。
 2HI(g) ΔH<0,并达平衡,HI的体积分数φ(HI)随时间变化如图曲线(Ⅱ)所示。
2HI(g) ΔH<0,并达平衡,HI的体积分数φ(HI)随时间变化如图曲线(Ⅱ)所示。
(1)达平衡时,I2(g)的物质的量浓度为
(2)若保持温度不变,在另一相同的2 L的密闭容器中加入a mol I2(g)、b mol H2和c mol HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.60,则a、b、c的关系是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有A、B、C、D四种强电解质,它们在水中电离时可产生下列离子(每种物质只含一种阳离子和一种阴离子且互不重复)。
已知:①A、C溶液的pH均大于7,B溶液的pH小于7,A、B溶液中水的电离程度相同;D物质的焰色反应呈黄色;②C溶液和D溶液相遇时只生成白色沉淀,B溶液和C溶液相遇时只生成有刺激性气味的气体,A溶液和D溶液混合时无明显现象。
(1)A的名称是_______ B的化学式_______
(2)写出C溶液和D溶液反应的化学方程式___________
(3)25 ℃时,pH=9的A溶液和pH=9的C溶液中水的电离程度小的是___ (填A或C)。
(4) A溶液的pH大于7,用离子方程式表示原因______ 。
| 阳离子 | K+、Na+、Ba2+、NH |
| 阴离子 | CH3COO-、Cl-、OH-、SO |
(1)A的名称是
(2)写出C溶液和D溶液反应的化学方程式
(3)25 ℃时,pH=9的A溶液和pH=9的C溶液中水的电离程度小的是
(4) A溶液的pH大于7,用离子方程式表示原因
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】回答下列问题
(1)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
①写出该混合溶液中存在的电荷守恒关系式_______ 。
现将 溶液和
溶液和 溶液等体积混合,得到缓冲溶液。
溶液等体积混合,得到缓冲溶液。
②若HA为HCN,该溶液显碱性,则溶液中c(Na+)_______ c(CN-) (填“<”、“=”或“>”)。
③若HA为 ,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是
,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是_______ 。
(2)常温下,向 溶液中逐滴加入
溶液中逐滴加入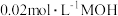 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:

常温下一定浓度的MCl稀溶液的pH_______ (填“>”“<”或“=”)7,K点对应的溶液中,c(M+)+c(MOH) _______ (填“>”“<”或“=”)2c(Cl-)
(1)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
①写出该混合溶液中存在的电荷守恒关系式
现将
 溶液和
溶液和 溶液等体积混合,得到缓冲溶液。
溶液等体积混合,得到缓冲溶液。②若HA为HCN,该溶液显碱性,则溶液中c(Na+)
③若HA为
 ,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是
,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是(2)常温下,向
 溶液中逐滴加入
溶液中逐滴加入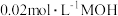 溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
常温下一定浓度的MCl稀溶液的pH
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】活性炭吸附法是工业 提碘的主要方法之一,其流程如下:
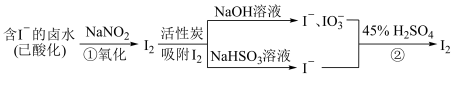
完成下列填空:
(1)酸性条件下,NaNO2溶液只能将I-氧化为I2,同时生成NO。写出反应①的离子方程式并标出电子转移的方向和数目___________________________________________________ 。
(2)氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,但工业上氧化卤水中的I-选择了价格并不便宜的亚硝酸钠,可能的原因是____________________________________ 。
(3)反应②发生时,溶液底部有紫黑色固体生成,有时溶液上方产生紫色气体,产生这种现象的原因是_______________________________________ 。
(4)流程中,碘元素经过了I-→I2→I-、IO3-→I2的变化过程,这样反复操作的目的是___________ 。
(5)流程中所用的NaHSO3溶液显弱酸性,源于NaHSO3存在两种程度不同的平衡体系:水解_______________________________ 和电离_______________________________ (用离子方程式表示)
(6)如向0.1mol/L的NaHSO3溶液中分别加入以下物质,回答问题:
①加入少量Ba(OH)2固体,水解平衡向_________ 移动。
②加入少量NaClO固体,溶液的pH_________ (选填:增大、减小、不变)。

完成下列填空:
(1)酸性条件下,NaNO2溶液只能将I-氧化为I2,同时生成NO。写出反应①的离子方程式并标出电子转移的方向和数目
(2)氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,但工业上氧化卤水中的I-选择了价格并不便宜的亚硝酸钠,可能的原因是
(3)反应②发生时,溶液底部有紫黑色固体生成,有时溶液上方产生紫色气体,产生这种现象的原因是
(4)流程中,碘元素经过了I-→I2→I-、IO3-→I2的变化过程,这样反复操作的目的是
(5)流程中所用的NaHSO3溶液显弱酸性,源于NaHSO3存在两种程度不同的平衡体系:水解
(6)如向0.1mol/L的NaHSO3溶液中分别加入以下物质,回答问题:
①加入少量Ba(OH)2固体,水解平衡向
②加入少量NaClO固体,溶液的pH
您最近一年使用:0次



