工业上在一定条件下可由水煤气合成甲醇,同时有副反应,反应如下:
主反应: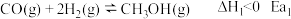
副反应: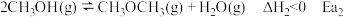
已知: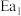 和
和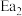 为正反应活化能,且
为正反应活化能,且 。
。
请回答:
(1)有利于主反应平衡正向移动的适宜条件___________ 。
A.高温高压 B.低温高压 C.高温低压 D.低温低压
(2)反应: 的
的
___________ (用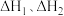 表示)
表示)
(3)若主反应在恒温恒容下进行,下列说法正确的是___________
A.当容器压强不变,反应处于平衡状态
B.K值越大,反应速率一定越快
C. 越小,放热越多,反应速率就越快
越小,放热越多,反应速率就越快
D.使用合适催化剂,可快速提高反应平衡前的转化率
E.正反应活化能越大, 就越大
就越大
(4)在 时,
时, 和
和 在体积为
在体积为 的恒温密闭容器中反应,测得2小时和5小时
的恒温密闭容器中反应,测得2小时和5小时 的选择性为80%和60%(
的选择性为80%和60%( 的选择性是指转化的
的选择性是指转化的 中生成
中生成 的百分比)。
的百分比)。 的转化率与时间的关系如图1所示:(不考虑其它副反应)
的转化率与时间的关系如图1所示:(不考虑其它副反应)
则:①2小时 的产率
的产率___________ 。
②副反应的平衡常数___________ 。
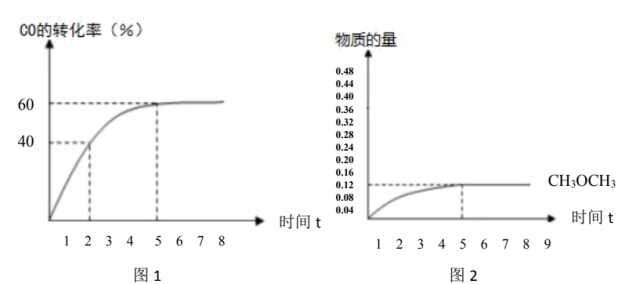
(5) 的物质的量随时间变化如图2所示,请在图2上画出
的物质的量随时间变化如图2所示,请在图2上画出 的物质的量随时间变化曲线
的物质的量随时间变化曲线___________ 。
主反应:
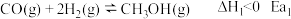
副反应:
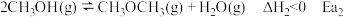
已知:
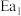 和
和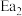 为正反应活化能,且
为正反应活化能,且 。
。请回答:
(1)有利于主反应平衡正向移动的适宜条件
A.高温高压 B.低温高压 C.高温低压 D.低温低压
(2)反应:
 的
的
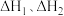 表示)
表示)(3)若主反应在恒温恒容下进行,下列说法正确的是
A.当容器压强不变,反应处于平衡状态
B.K值越大,反应速率一定越快
C.
 越小,放热越多,反应速率就越快
越小,放热越多,反应速率就越快D.使用合适催化剂,可快速提高反应平衡前的转化率
E.正反应活化能越大,
 就越大
就越大(4)在
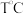 时,
时, 和
和 在体积为
在体积为 的恒温密闭容器中反应,测得2小时和5小时
的恒温密闭容器中反应,测得2小时和5小时 的选择性为80%和60%(
的选择性为80%和60%( 的选择性是指转化的
的选择性是指转化的 中生成
中生成 的百分比)。
的百分比)。 的转化率与时间的关系如图1所示:(不考虑其它副反应)
的转化率与时间的关系如图1所示:(不考虑其它副反应)则:①2小时
 的产率
的产率②副反应的平衡常数

(5)
 的物质的量随时间变化如图2所示,请在图2上画出
的物质的量随时间变化如图2所示,请在图2上画出 的物质的量随时间变化曲线
的物质的量随时间变化曲线
更新时间:2021-04-14 08:43:08
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】I.如图列出了①~⑧八种元素在周期表中的位置:
请回答下列问题:
(1)②和③能形成一种淡黄色的固体,请写出该物质的电子式:______ 。
(2)写出实验室制取①的最简单氢化物的化学方程式______ 。
(3)比较⑥和⑦最高价氧化物对应水化物酸性的强弱:______ (用化学式表示)。
(4)⑤的最高价氧化物对应的水化物与⑧的最高价氧化物对应的水化物反应的化学方程式是______ 。
(5)下列可以比较③、④两元素金属性强弱的实验是______(填字母)。
Ⅱ. 催化重整反应为
催化重整反应为 。已知上述反应中相关的化学键键能数据如下:
。已知上述反应中相关的化学键键能数据如下:
(6)则该反应的
______ 。
(7)已知:
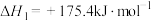

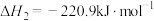
 加碳氯化生成
加碳氯化生成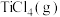 和
和 的热化学方程式:
的热化学方程式:______ 。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 4 | ⑧ |
(1)②和③能形成一种淡黄色的固体,请写出该物质的电子式:
(2)写出实验室制取①的最简单氢化物的化学方程式
(3)比较⑥和⑦最高价氧化物对应水化物酸性的强弱:
(4)⑤的最高价氧化物对应的水化物与⑧的最高价氧化物对应的水化物反应的化学方程式是
(5)下列可以比较③、④两元素金属性强弱的实验是______(填字母)。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将③的单质投入到④的盐溶液中 |
| C.将形状、大小相同的这两种元素的单质分别与等体积20℃的水反应 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
Ⅱ.
 催化重整反应为
催化重整反应为 。已知上述反应中相关的化学键键能数据如下:
。已知上述反应中相关的化学键键能数据如下:| 化学键 |  |  |  | 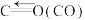 |
键能 | 413 | 745 | 436 | 1075 |
(6)则该反应的

(7)已知:

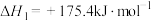

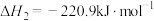
 加碳氯化生成
加碳氯化生成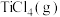 和
和 的热化学方程式:
的热化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】十三届全国人民代表大会第四次会议上作政府工作报告时指出:优化产业结构和能源结构,扎实做好碳达峰、碳中和各项工作。
(1)利用工业废气中的CO2可制取甲醇,其反应为:CO2+3H2 CH3OH+H2O。
CH3OH+H2O。
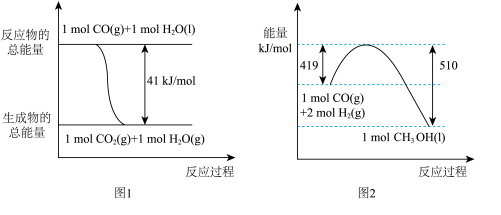
①常温常压下,已知反应的能量变化如图1、图2所示, 由二氧化碳和氢气制备甲醇的热化学方程式为CO2(g)+3H2(g) CH3OH(l)+H2O(l) ΔH= a kJ·mol-1,则a=
CH3OH(l)+H2O(l) ΔH= a kJ·mol-1,则a=___________ 。
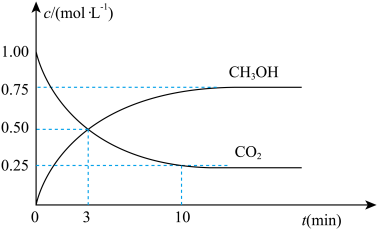
②为探究用CO2生产燃料甲醇的反应原理,现进行如下实验:在一恒温恒容密闭容器中,充入lmolCO2和3molH2,进行上述反应。 测得CO2和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,v(H2)=___________ ;能使平衡体系中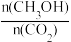 增大的措施有
增大的措施有___________ (任写一条)。
(2)CO2加氢还可制备甲酸(HCOOH)。其反应原理为CO2(g)+H2(g) HCOOH(g) △H= -31.4 kJ·mol-1。
HCOOH(g) △H= -31.4 kJ·mol-1。
①温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g) HCOOH(g) K=2。实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=
HCOOH(g) K=2。实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=___________ k正。
②温度为T2℃时,k正=1.9k逆,则T2℃时平衡压强___________ (填“>”“<”或“=”)T1℃时平衡压强,理由是___________ 。
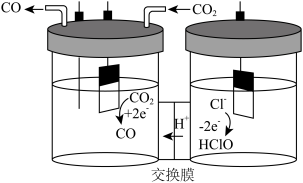
(3)我国科学家设计了一种将电解饱和食盐水与电催化还原CO2相耦合的电解装置(如图)。阴极上的电极反应式为:___________
(1)利用工业废气中的CO2可制取甲醇,其反应为:CO2+3H2
 CH3OH+H2O。
CH3OH+H2O。①常温常压下,已知反应的能量变化如图1、图2所示, 由二氧化碳和氢气制备甲醇的热化学方程式为CO2(g)+3H2(g)
 CH3OH(l)+H2O(l) ΔH= a kJ·mol-1,则a=
CH3OH(l)+H2O(l) ΔH= a kJ·mol-1,则a=
②为探究用CO2生产燃料甲醇的反应原理,现进行如下实验:在一恒温恒容密闭容器中,充入lmolCO2和3molH2,进行上述反应。 测得CO2和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,v(H2)=
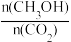 增大的措施有
增大的措施有
(2)CO2加氢还可制备甲酸(HCOOH)。其反应原理为CO2(g)+H2(g)
 HCOOH(g) △H= -31.4 kJ·mol-1。
HCOOH(g) △H= -31.4 kJ·mol-1。①温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应:CO2(g)+H2(g)
 HCOOH(g) K=2。实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=
HCOOH(g) K=2。实验测得:v正=k正c(CO2)·c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。T1℃时,k逆=②温度为T2℃时,k正=1.9k逆,则T2℃时平衡压强
(3)我国科学家设计了一种将电解饱和食盐水与电催化还原CO2相耦合的电解装置(如图)。阴极上的电极反应式为:

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】乙烯是重要的化工原料,在化工合成与生产中具有极其重要的地位,回答下列问题:
(1)C2H4(g)+3O2=2CO2(g)+2H2O(l) ΔH1
C(s,石墨)+O2(g)=CO2(g) ΔH2
2H2(g)+O2(g)=2H2O(l) ΔH3
写出乙烯气体分解得到石墨和氢气的热化学方程式___________ 。
(2)乙烯可由甲烷制得:2CH4(g) C2H4(g)+2H2(g)。T℃时在2L恒容密闭容器中充入0.6mol甲烷气体,若5分钟时达到平衡,测得c(C2H4)=2c(CH4),则v(H2)=
C2H4(g)+2H2(g)。T℃时在2L恒容密闭容器中充入0.6mol甲烷气体,若5分钟时达到平衡,测得c(C2H4)=2c(CH4),则v(H2)=___________ mol·L-1·min-1,该反应的平衡常数为___________ 。保持温度不变,若再向平衡后的容器中各充入0.12mol的三种气体,充人后v正___________ v逆(填“>”、“<”或“=”)。
(3)工业上以煤为主要原料制乙烯首先需要制备合成气,生产合成气的反应为:C(s)+H2O(g)=CO(g)+H2(g),理论上该反应能自发进行的条件是___________ 。 制得合成气后需用合成气制备甲醇CO(g)+2H2(g) CH3OH(g),现设置以下三个容器进行该反应(恒温)
CH3OH(g),现设置以下三个容器进行该反应(恒温)
达平衡时,三个容器中甲醇体积分数的大小关系为___________ (填编号)。
(4)已知反应2CO2(g)+6H2(g) C2H4(g)+4H2O(g)可用于制备乙烯,现向一刚性容器中按物质的量之比1:1充入CO2和H2,在温度为378K和478K时CO2的转化率随时间变化如图所示:
C2H4(g)+4H2O(g)可用于制备乙烯,现向一刚性容器中按物质的量之比1:1充入CO2和H2,在温度为378K和478K时CO2的转化率随时间变化如图所示:
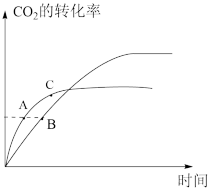
①图中A、B、C三点逆反应速率由大到小的顺序是___________ 。
②如改变影响平衡的某一条件使得CO2的平衡转化率增大,则该反应平衡常数的变化是___________ 。
(1)C2H4(g)+3O2=2CO2(g)+2H2O(l) ΔH1
C(s,石墨)+O2(g)=CO2(g) ΔH2
2H2(g)+O2(g)=2H2O(l) ΔH3
写出乙烯气体分解得到石墨和氢气的热化学方程式
(2)乙烯可由甲烷制得:2CH4(g)
 C2H4(g)+2H2(g)。T℃时在2L恒容密闭容器中充入0.6mol甲烷气体,若5分钟时达到平衡,测得c(C2H4)=2c(CH4),则v(H2)=
C2H4(g)+2H2(g)。T℃时在2L恒容密闭容器中充入0.6mol甲烷气体,若5分钟时达到平衡,测得c(C2H4)=2c(CH4),则v(H2)=(3)工业上以煤为主要原料制乙烯首先需要制备合成气,生产合成气的反应为:C(s)+H2O(g)=CO(g)+H2(g),理论上该反应能自发进行的条件是
 CH3OH(g),现设置以下三个容器进行该反应(恒温)
CH3OH(g),现设置以下三个容器进行该反应(恒温)| 编号 | 条件 | n(CO)/mol | n(H2)/mol | n(CH3OH)/mol |
| ① | 恒容 | 0.2 | 0.4 | 0 |
| ② | 恒容 | 0.4 | 0.8 | 0 |
| ③ | 恒压 | 0.4 | 0.8 | 0 |
达平衡时,三个容器中甲醇体积分数的大小关系为
(4)已知反应2CO2(g)+6H2(g)
 C2H4(g)+4H2O(g)可用于制备乙烯,现向一刚性容器中按物质的量之比1:1充入CO2和H2,在温度为378K和478K时CO2的转化率随时间变化如图所示:
C2H4(g)+4H2O(g)可用于制备乙烯,现向一刚性容器中按物质的量之比1:1充入CO2和H2,在温度为378K和478K时CO2的转化率随时间变化如图所示:
①图中A、B、C三点逆反应速率由大到小的顺序是
②如改变影响平衡的某一条件使得CO2的平衡转化率增大,则该反应平衡常数的变化是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
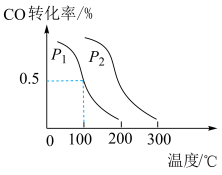
【推荐1】甲醇可作为燃料电池的原料。下列反应制备甲醇:CO(g)+2H2(g) CH3OH(g) △H=﹣90.8 kJ•mol-1,在一容积可变的密闭容器中充入10 mol CO 和20 mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A时,容器的体积为20 L。
CH3OH(g) △H=﹣90.8 kJ•mol-1,在一容积可变的密闭容器中充入10 mol CO 和20 mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A时,容器的体积为20 L。

(1)该反应的平衡常数表达式_______ 。若提高温度到T2,达平衡时,K值_______ (填“增大”“减小”或“不变”)。
(2)图中P1_______ P2(填“>”、“<”或“=”)。
(3)已知CO2(g)+H2(g) CO(g)+H2O(g) △H=+41.3 kJ•mol﹣1,试写出由CO2和H2制取气态甲醇和气态水的热化学方程式
CO(g)+H2O(g) △H=+41.3 kJ•mol﹣1,试写出由CO2和H2制取气态甲醇和气态水的热化学方程式_______ 。
 CH3OH(g) △H=﹣90.8 kJ•mol-1,在一容积可变的密闭容器中充入10 mol CO 和20 mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A时,容器的体积为20 L。
CH3OH(g) △H=﹣90.8 kJ•mol-1,在一容积可变的密闭容器中充入10 mol CO 和20 mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A时,容器的体积为20 L。
(1)该反应的平衡常数表达式
(2)图中P1
(3)已知CO2(g)+H2(g)
 CO(g)+H2O(g) △H=+41.3 kJ•mol﹣1,试写出由CO2和H2制取气态甲醇和气态水的热化学方程式
CO(g)+H2O(g) △H=+41.3 kJ•mol﹣1,试写出由CO2和H2制取气态甲醇和气态水的热化学方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为
_____ 。
(2)该反应为_____ 反应(选填“吸热”、“放热”)。
(3)能判断该反应是否已达到化学平衡状态的依据是_____。
(4)某温度下,平衡浓度符合下式: ,试判断此时的温度为
,试判断此时的温度为_____ ℃。将 的
的 与
与 混合加热到此温度,达到下列平衡时
混合加热到此温度,达到下列平衡时 转化为
转化为 的转化率为
的转化率为_____ (保留1位小数)。
(5)恒温下,一体积固定的密闭容器中存在反应 ,若增大
,若增大 的浓度,则此反应的焓变
的浓度,则此反应的焓变_____ (填“增大”、“减小”、“不变”)。
(6)在催化剂和一定温度、压强条件下, 与
与 可反应生成甲醇:
可反应生成甲醇: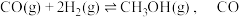 的平衡转化率与温度、压强的关系如图所示,则:
的平衡转化率与温度、压强的关系如图所示,则:
_____  (填“>”、“<”或“=”,下同),该反应的
(填“>”、“<”或“=”,下同),该反应的
_____ 0。
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表: | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为

(2)该反应为
(3)能判断该反应是否已达到化学平衡状态的依据是_____。
| A.容器中压强不变 | B.混合气体中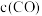 不变 不变 |
C. | D.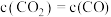 |
(4)某温度下,平衡浓度符合下式:
 ,试判断此时的温度为
,试判断此时的温度为 的
的 与
与 混合加热到此温度,达到下列平衡时
混合加热到此温度,达到下列平衡时 转化为
转化为 的转化率为
的转化率为(5)恒温下,一体积固定的密闭容器中存在反应
 ,若增大
,若增大 的浓度,则此反应的焓变
的浓度,则此反应的焓变(6)在催化剂和一定温度、压强条件下,
 与
与 可反应生成甲醇:
可反应生成甲醇: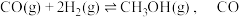 的平衡转化率与温度、压强的关系如图所示,则:
的平衡转化率与温度、压强的关系如图所示,则:
 (填“>”、“<”或“=”,下同),该反应的
(填“>”、“<”或“=”,下同),该反应的

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】 资源化能有效应对全球的气候变化,并且能充分利用碳资源。
资源化能有效应对全球的气候变化,并且能充分利用碳资源。
(1) 催化加氢合成
催化加氢合成 其过程中主要发生下列反应:
其过程中主要发生下列反应:
反应Ⅰ:
反应Ⅱ: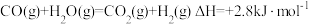
反应Ⅲ: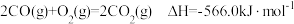
则反应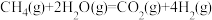 的
的
___________  。
。
(2)电解法转化 可实现
可实现 资源化利用。电解
资源化利用。电解 制
制 的原理示意图如图1。
的原理示意图如图1。
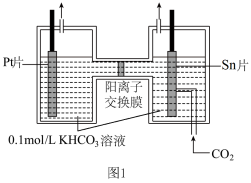
写出阴极 还原为
还原为 的电极反应式:
的电极反应式:___________ ,电解一段时间后,阳极区的 溶液浓度降低,其原因是
溶液浓度降低,其原因是___________ 。
(3) 催化加氢合成二甲醚。
催化加氢合成二甲醚。
反应Ⅰ:
反应Ⅱ:
①反应Ⅱ的平衡常数表达式
___________ 。
②在恒压、 和
和 的起始量一定的条件下,
的起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性(
的选择性( 的选择性
的选择性 )随温度的变化如图2。
)随温度的变化如图2。
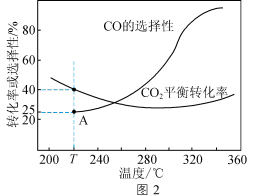
T℃时,起始投入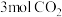 、
、 ,达到平衡时反应I理论上消耗
,达到平衡时反应I理论上消耗 的物质的量为
的物质的量为___________  。合成二甲醚时较适宜的温度为260℃,其原因是
。合成二甲醚时较适宜的温度为260℃,其原因是___________ 。
 资源化能有效应对全球的气候变化,并且能充分利用碳资源。
资源化能有效应对全球的气候变化,并且能充分利用碳资源。(1)
 催化加氢合成
催化加氢合成 其过程中主要发生下列反应:
其过程中主要发生下列反应:反应Ⅰ:

反应Ⅱ:
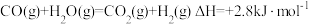
反应Ⅲ:
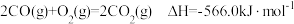
则反应
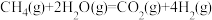 的
的
 。
。(2)电解法转化
 可实现
可实现 资源化利用。电解
资源化利用。电解 制
制 的原理示意图如图1。
的原理示意图如图1。
写出阴极
 还原为
还原为 的电极反应式:
的电极反应式: 溶液浓度降低,其原因是
溶液浓度降低,其原因是(3)
 催化加氢合成二甲醚。
催化加氢合成二甲醚。反应Ⅰ:

反应Ⅱ:

①反应Ⅱ的平衡常数表达式

②在恒压、
 和
和 的起始量一定的条件下,
的起始量一定的条件下, 平衡转化率和平衡时
平衡转化率和平衡时 的选择性(
的选择性( 的选择性
的选择性 )随温度的变化如图2。
)随温度的变化如图2。
T℃时,起始投入
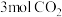 、
、 ,达到平衡时反应I理论上消耗
,达到平衡时反应I理论上消耗 的物质的量为
的物质的量为 。合成二甲醚时较适宜的温度为260℃,其原因是
。合成二甲醚时较适宜的温度为260℃,其原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】燃煤烟气中的SO2是主要的大气污染物之一、氢气可用于还原二氧化硫,其主要反应为: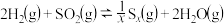 。
。
(1)用氢气进行脱硫的优点是_______ 。
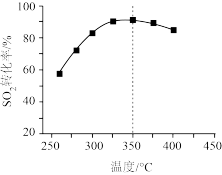
(2)如图表示Co/Al2O3催化下,相同时间内、不同温度下的SO2的转化率。由图可知该反应为放热反应,解释图中温度小于350℃时,转化率随温度升高而增大的原因是_______ 。
(3)以Co/Al2O3作催化剂时氢气脱硫的过程由两步反应组成,过程如图1所示。
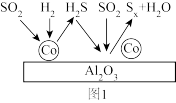
①结合图1中的信息,写出第一步反应的化学方程式:___ 。
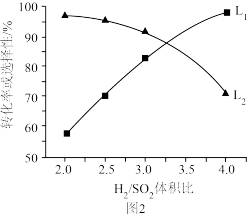
②已知在反应过程中,过量的H2可发生副反应: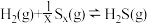 ,图2中的两条曲线分别代表SO2的转化率或SX的选择性随H2/SO2体积比的变化(SX的选择性:SO2的还原产物中SX所占的百分比),可推断曲线
,图2中的两条曲线分别代表SO2的转化率或SX的选择性随H2/SO2体积比的变化(SX的选择性:SO2的还原产物中SX所占的百分比),可推断曲线__ (填“L1“或“L2”)代表SX的选择性,理由是__ 。
(4)下表所示为压强对氢气脱硫反应的影响(已知:p(A)/P总=n(A)/n总)。
下列关于表中数据的分析中,不正确的是___ (填字母)
a要想增大反应速率,增大SO2压强比增大H2压强更为有效
b.保持SO2/H2的比例不变,提高总压,SO2的平衡转化率增加
c.x与y的值都在90.6至96.2之间
 。
。(1)用氢气进行脱硫的优点是
(2)如图表示Co/Al2O3催化下,相同时间内、不同温度下的SO2的转化率。由图可知该反应为放热反应,解释图中温度小于350℃时,转化率随温度升高而增大的原因是

(3)以Co/Al2O3作催化剂时氢气脱硫的过程由两步反应组成,过程如图1所示。
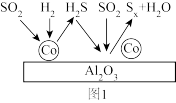

①结合图1中的信息,写出第一步反应的化学方程式:
②已知在反应过程中,过量的H2可发生副反应:
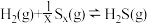 ,图2中的两条曲线分别代表SO2的转化率或SX的选择性随H2/SO2体积比的变化(SX的选择性:SO2的还原产物中SX所占的百分比),可推断曲线
,图2中的两条曲线分别代表SO2的转化率或SX的选择性随H2/SO2体积比的变化(SX的选择性:SO2的还原产物中SX所占的百分比),可推断曲线(4)下表所示为压强对氢气脱硫反应的影响(已知:p(A)/P总=n(A)/n总)。
实验 | P(SO2)/kPa | P(H2) /kPa | SO2起始速率 ×10-4mol·L-1·h-1 | H2起始速率 ×10-4mol·L-1·h-1 | SO2的平衡转化率% |
1 | 13.3 | 26.7 | 1.90 | 3.74 | 90.6 |
2 | 26.6 | 26.7 | 2.26 | 4.43 | x |
3 | 13.3 | 52.3 | 4.06 | 7.94 | y |
4 | 26.6 | 52.3 | 4.83 | 9.41 | 96.2 |
下列关于表中数据的分析中,不正确的是
a要想增大反应速率,增大SO2压强比增大H2压强更为有效
b.保持SO2/H2的比例不变,提高总压,SO2的平衡转化率增加
c.x与y的值都在90.6至96.2之间
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】氢气是清洁能源,工业上用天然气为原料制备氢气的有关反应如下:
I.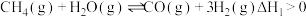
II.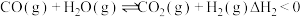
回答下列问题:
(1)在恒温恒容密闭容器中充入 和
和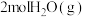 ,发生上述反应。下列叙述正确的是___________(填字母)。
,发生上述反应。下列叙述正确的是___________(填字母)。
(2)写出 和
和 反应生成
反应生成 和
和 的热化学方程式:
的热化学方程式:___________ ( 用
用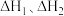 的关系式表示)。
的关系式表示)。
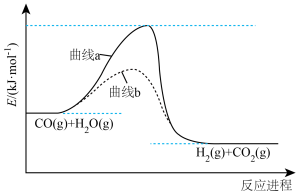
(3) 和水蒸气反应的能量变化如图所示。
和水蒸气反应的能量变化如图所示。
已知:i.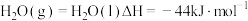 。
。
ii.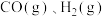 的燃烧热
的燃烧热 分别为
分别为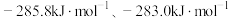 。
。
①启动该反应需要加热,其主要作用是___________ (填字母)。
A.降低活化能 B.改变反应历程
C.增大反应物能量 D.增大产物能量
②图中代表加入催化剂的曲线是___________ (填“a”或“b”)。
③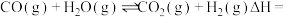
___________  。
。
I.
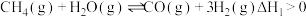
II.
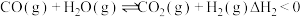
回答下列问题:
(1)在恒温恒容密闭容器中充入
 和
和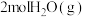 ,发生上述反应。下列叙述正确的是___________(填字母)。
,发生上述反应。下列叙述正确的是___________(填字母)。| A.平衡后,增大压强,反应Ⅰ的平衡常数减小 |
| B.平衡后,升高温度,两个反应都向左移动 |
C.平衡后,充入惰性气体, 的平衡转化率增大 的平衡转化率增大 |
D.其他条件不变,增大 浓度,两个反应的正反应速率均增大 浓度,两个反应的正反应速率均增大 |
(2)写出
 和
和 反应生成
反应生成 和
和 的热化学方程式:
的热化学方程式: 用
用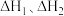 的关系式表示)。
的关系式表示)。(3)
 和水蒸气反应的能量变化如图所示。
和水蒸气反应的能量变化如图所示。
已知:i.
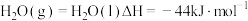 。
。ii.
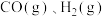 的燃烧热
的燃烧热 分别为
分别为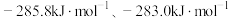 。
。①启动该反应需要加热,其主要作用是
A.降低活化能 B.改变反应历程
C.增大反应物能量 D.增大产物能量
②图中代表加入催化剂的曲线是
③
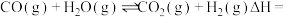
 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】I.300℃时将2molA和2molB两种气体混合于2L密闭容器中,发生如下反应:3A(g)+B(g)⇌2C(g)+2D(g) △H,2min末达到平衡,生成0.8moLD。
(1)300℃时,该反应的平衡常数表达式为K=________ ,已知K300℃<K350℃,则△H________ (填“>”或“<” 0).
(2)在2min末时,B的平衡浓度为________ ,D的平均反应速率为________ 。
(3)若温度不变,缩小容器容积,则A的转化率________  填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。
II.在一定条件下,可逆反应:mA+nB⇌pC达到平衡,若:
(1)A、B、C都是气体,减小压强,平衡向正反应方向移动,则,m+n________ (填“>”“<”或“ ” p)。
” p)。
(2)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是________ 。
(3)加热后,可使C的质量增加,则正反应是________ (填“放热”或“吸热”)反应。
(1)300℃时,该反应的平衡常数表达式为K=
(2)在2min末时,B的平衡浓度为
(3)若温度不变,缩小容器容积,则A的转化率
 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。II.在一定条件下,可逆反应:mA+nB⇌pC达到平衡,若:
(1)A、B、C都是气体,减小压强,平衡向正反应方向移动,则,m+n
 ” p)。
” p)。(2)A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡移动的方向是
(3)加热后,可使C的质量增加,则正反应是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】消除氮氧化物污染对建设美丽家乡,打造宜居环境有重要意义。
(1)炽热的活性炭可以处理NO2,发生的反应为2C(s)+2NO2(g)=2CO2(g)+N2(g) ΔH。
已知:①2NO(g)+O2(g)=2NO2(g) ΔH=-114kJ·mol-1
②C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
③N2(g)+O2(g)=2NO(g) ΔH=+181kJ·mol-1
则ΔH=___________ 。
(2)炽热的活性炭可以处理NO,发生的反应为C(s)+2NO(g) CO2(g)+N2(g) ΔH=-574kJ·mol-1。
CO2(g)+N2(g) ΔH=-574kJ·mol-1。
①该反应任何温度下都能自发进行,则该反应的ΔS___________ 0(填“>”“<”或“=”)
②在恒温恒容下发生上述反应,下列能表示该反应达到平衡状态的是___________ 。
A.混合气体的密度保持不变 B.混合气体的平均相对分子质量保持不变
C.2v(NO)正=v(N2)正 D.容器内压强不再改变
(3)已知:4CO(g)+2NO2(g) 4CO2(g)+N2(g) ΔH=-1200kJ·mol-1。在2L恒容密闭容器中,投入0.2molNO2和0.4molCO,经过一段时间后达到平衡状态,测得CO的转化率为50%。该温度下,反应的平衡常数为
4CO2(g)+N2(g) ΔH=-1200kJ·mol-1。在2L恒容密闭容器中,投入0.2molNO2和0.4molCO,经过一段时间后达到平衡状态,测得CO的转化率为50%。该温度下,反应的平衡常数为___________ 。
(4)将3%NO、6%NH3、21%O2和70%N2的混合气体(N2为平衡气)以一定流速通过装有Cu基催化剂的反应器,NO去除率随反应温度的变化曲线如图所示。
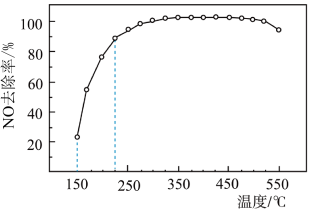
在150-225℃范围内,NO去除率随温度的升高而迅速上升的原因是___________ 。
(5)向恒容密闭容器中充入一定量的CH4(g)和NO(g),发生反应:CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(g) ΔH=-2894kJ·mol-1。在T3K下NO的平衡转化率随
2N2(g)+CO2(g)+2H2O(g) ΔH=-2894kJ·mol-1。在T3K下NO的平衡转化率随 的变化曲线及当
的变化曲线及当 =x时NO的平衡转化率随
=x时NO的平衡转化率随 (温度的倒数)的变化曲线如图所示。
(温度的倒数)的变化曲线如图所示。
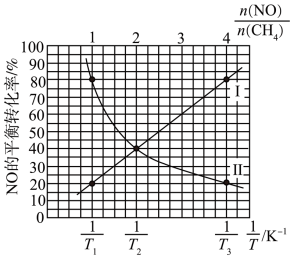
①表示T3K下,NO的平衡转化率随 的变化曲线为曲线
的变化曲线为曲线___________ (填“Ⅰ”或“Ⅱ”),
②x=___________ 。
(1)炽热的活性炭可以处理NO2,发生的反应为2C(s)+2NO2(g)=2CO2(g)+N2(g) ΔH。
已知:①2NO(g)+O2(g)=2NO2(g) ΔH=-114kJ·mol-1
②C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1
③N2(g)+O2(g)=2NO(g) ΔH=+181kJ·mol-1
则ΔH=
(2)炽热的活性炭可以处理NO,发生的反应为C(s)+2NO(g)
 CO2(g)+N2(g) ΔH=-574kJ·mol-1。
CO2(g)+N2(g) ΔH=-574kJ·mol-1。①该反应任何温度下都能自发进行,则该反应的ΔS
②在恒温恒容下发生上述反应,下列能表示该反应达到平衡状态的是
A.混合气体的密度保持不变 B.混合气体的平均相对分子质量保持不变
C.2v(NO)正=v(N2)正 D.容器内压强不再改变
(3)已知:4CO(g)+2NO2(g)
 4CO2(g)+N2(g) ΔH=-1200kJ·mol-1。在2L恒容密闭容器中,投入0.2molNO2和0.4molCO,经过一段时间后达到平衡状态,测得CO的转化率为50%。该温度下,反应的平衡常数为
4CO2(g)+N2(g) ΔH=-1200kJ·mol-1。在2L恒容密闭容器中,投入0.2molNO2和0.4molCO,经过一段时间后达到平衡状态,测得CO的转化率为50%。该温度下,反应的平衡常数为(4)将3%NO、6%NH3、21%O2和70%N2的混合气体(N2为平衡气)以一定流速通过装有Cu基催化剂的反应器,NO去除率随反应温度的变化曲线如图所示。

在150-225℃范围内,NO去除率随温度的升高而迅速上升的原因是
(5)向恒容密闭容器中充入一定量的CH4(g)和NO(g),发生反应:CH4(g)+4NO(g)
 2N2(g)+CO2(g)+2H2O(g) ΔH=-2894kJ·mol-1。在T3K下NO的平衡转化率随
2N2(g)+CO2(g)+2H2O(g) ΔH=-2894kJ·mol-1。在T3K下NO的平衡转化率随 的变化曲线及当
的变化曲线及当 =x时NO的平衡转化率随
=x时NO的平衡转化率随 (温度的倒数)的变化曲线如图所示。
(温度的倒数)的变化曲线如图所示。
①表示T3K下,NO的平衡转化率随
 的变化曲线为曲线
的变化曲线为曲线②x=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氨在工农业及国防工业上有广泛的用途。
(1)已知:
①4NH3(g)+3O2(g) 2N2(g)+6H2O(g) △H=-1266.2k/mol
2N2(g)+6H2O(g) △H=-1266.2k/mol
②2H2(g)+O2(g) 2H2O(g) △H=-483.6kJ/mol
2H2O(g) △H=-483.6kJ/mol
则合成氨反应N2(g)+3H2(g) 2NH3(g) △H=
2NH3(g) △H=___________ kJ/mol,该反应属于___________ 。
A.高温自发 B.低温自发 C.恒自发 D.恒不自发
(2)在甲、乙、丙三个容积均为2L的密闭装置中,均充人4mol合成气,但N2、H2的投料比不同,在400℃时反应,测定N2的体积百分含量,得到下图一。
①乙装置中N2、H2的投料比为___________ 。
②反应达到平衡后,测得乙装置中H2的体积百分含量为25%,则400℃时,合成氨反应的平衡常数为___________ (不须注明单位)。
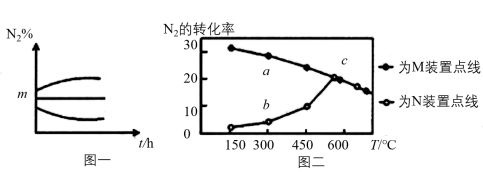
(3)在M、N两个装置中分别充入相同投料比的N2、H2,进行合成氨反应,各反应1小时,测定不同温度下N2的转化率,得到上图二。
①N2、H2在M、N两装置中反应时,不同的条件可能是______________________ 。
②在300℃时,a、b两点转化率差异的原因是______________________ 。
(4)氨法烟气脱硫技术渐趋成熟,回收SO2,并产出氮肥,其流程分两步:
①氨水吸收烟气中的SO2:xNH3+SO2(g)+H2O====(NH4)xH2-xSO3
②加入足量的磷酸得到纯净的SO2。写出该反应的化学方程式:______________________ 。
(1)已知:
①4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) △H=-1266.2k/mol
2N2(g)+6H2O(g) △H=-1266.2k/mol②2H2(g)+O2(g)
 2H2O(g) △H=-483.6kJ/mol
2H2O(g) △H=-483.6kJ/mol则合成氨反应N2(g)+3H2(g)
 2NH3(g) △H=
2NH3(g) △H=A.高温自发 B.低温自发 C.恒自发 D.恒不自发
(2)在甲、乙、丙三个容积均为2L的密闭装置中,均充人4mol合成气,但N2、H2的投料比不同,在400℃时反应,测定N2的体积百分含量,得到下图一。
①乙装置中N2、H2的投料比为
②反应达到平衡后,测得乙装置中H2的体积百分含量为25%,则400℃时,合成氨反应的平衡常数为

(3)在M、N两个装置中分别充入相同投料比的N2、H2,进行合成氨反应,各反应1小时,测定不同温度下N2的转化率,得到上图二。
①N2、H2在M、N两装置中反应时,不同的条件可能是
②在300℃时,a、b两点转化率差异的原因是
(4)氨法烟气脱硫技术渐趋成熟,回收SO2,并产出氮肥,其流程分两步:
①氨水吸收烟气中的SO2:xNH3+SO2(g)+H2O====(NH4)xH2-xSO3
②加入足量的磷酸得到纯净的SO2。写出该反应的化学方程式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1) 和
和 是两种重要的温室气体,通过
是两种重要的温室气体,通过 和
和 的反应,制造更高价值的化学品是目前的研究目标。250℃时,以镍合金为催化剂,发生如下反应:
的反应,制造更高价值的化学品是目前的研究目标。250℃时,以镍合金为催化剂,发生如下反应: 。
。
已知:




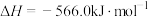
反应 的
的
_______  ;
;
(2)在一定体积的密闭容器中,进行如下化学反应: ,其化学平衡常数
,其化学平衡常数 和温度
和温度 的关系如下表:
的关系如下表:
回答下列问题:
①该反应的化学平衡常数表达式为
_______ 。
②该反应为反应_______ (选填“吸热”“放热”)。
③830℃,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的体积。平衡_______ (填“向正反应方向”“向逆反应方向”或“不”)移动。
④某温度下,平衡浓度符合 ,试判断此时的温度为
,试判断此时的温度为_______ ℃。在此温度下 密闭容器中进行反应
密闭容器中进行反应 ,
, 和
和 的起始量均为
的起始量均为 ,达到平衡时
,达到平衡时 的转化率为
的转化率为_______ 。
⑤若1200℃时,在某时刻,体系中 、
、 、
、 、
、 的浓度分别为
的浓度分别为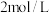 、
、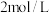 、
、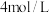 、
、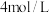 ,则此时上述反应的平衡移动方向为
,则此时上述反应的平衡移动方向为_______ (填“正反应方向”“逆反应方向”或“不移动”)。
(1)
 和
和 是两种重要的温室气体,通过
是两种重要的温室气体,通过 和
和 的反应,制造更高价值的化学品是目前的研究目标。250℃时,以镍合金为催化剂,发生如下反应:
的反应,制造更高价值的化学品是目前的研究目标。250℃时,以镍合金为催化剂,发生如下反应: 。
。已知:





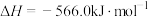
反应
 的
的
 ;
;(2)在一定体积的密闭容器中,进行如下化学反应:
 ,其化学平衡常数
,其化学平衡常数 和温度
和温度 的关系如下表:
的关系如下表: ℃ ℃ | 700 | 800 | 830 | 1000 | 1200 |
 | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①该反应的化学平衡常数表达式为

②该反应为反应
③830℃,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的体积。平衡
④某温度下,平衡浓度符合
 ,试判断此时的温度为
,试判断此时的温度为 密闭容器中进行反应
密闭容器中进行反应 ,
, 和
和 的起始量均为
的起始量均为 ,达到平衡时
,达到平衡时 的转化率为
的转化率为⑤若1200℃时,在某时刻,体系中
 、
、 、
、 、
、 的浓度分别为
的浓度分别为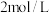 、
、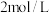 、
、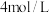 、
、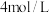 ,则此时上述反应的平衡移动方向为
,则此时上述反应的平衡移动方向为
您最近一年使用:0次



