室温下,向10mL 0.1mol·L-1H2C2O4溶液中滴加0.1mol·L-1NaOH溶液,混合溶液中含碳组分的物质的量分数δ(X)[δ(X)=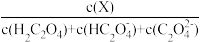 ]与pH关系如图所示。下列说法不正确的是
]与pH关系如图所示。下列说法不正确的是

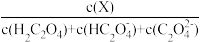 ]与pH关系如图所示。下列说法不正确的是
]与pH关系如图所示。下列说法不正确的是
A.曲线②代表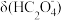 与pH关系 与pH关系 |
| B.将0.2mol·L-1NaHC2O4和0.2mol·L-1Na2C2O4等体积混合所得溶液pH=4.29 |
C.0.1mol·L-1NaHC2O4溶液中c(Na+)>c(HC2O )>c(H+)>c(C2O )>c(H+)>c(C2O )>c(OH-) )>c(OH-) |
| D.H2C2O4的第二步电离常数K2的数量级为10-5 |
2021·安徽安庆·模拟预测 查看更多[2]
更新时间:2021-04-17 16:33:42
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】将 盐酸和
盐酸和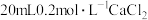 溶液混合后,用
溶液混合后,用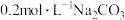 溶液滴定,滴定过程中溶液
溶液滴定,滴定过程中溶液 随加入
随加入 溶液体积变化如图。[
溶液体积变化如图。[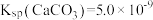 ,忽略溶液混合过程中体积变化]下列说法错误的是
,忽略溶液混合过程中体积变化]下列说法错误的是
 盐酸和
盐酸和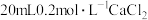 溶液混合后,用
溶液混合后,用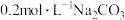 溶液滴定,滴定过程中溶液
溶液滴定,滴定过程中溶液 随加入
随加入 溶液体积变化如图。[
溶液体积变化如图。[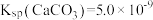 ,忽略溶液混合过程中体积变化]下列说法错误的是
,忽略溶液混合过程中体积变化]下列说法错误的是
A.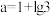 |
B. 、 、 、 、 三点的溶液中水电离程度依次增大 三点的溶液中水电离程度依次增大 |
C. 点溶液中存在: 点溶液中存在:  |
D. 点 点 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g)⇌Cl2(aq) K1=10-1.2
Cl2(aq)+H2O⇌HClO+H++Cl- K2=10-3.4
HClO⇌H++ClO- Ka=?
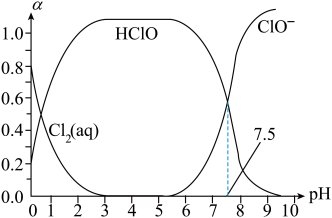
其中Cl2(aq)、HClO和ClO-分别在三者中占分数(α)随pH变化的关系如图所示。下列表述正确的是
Cl2(g)⇌Cl2(aq) K1=10-1.2
Cl2(aq)+H2O⇌HClO+H++Cl- K2=10-3.4
HClO⇌H++ClO- Ka=?
其中Cl2(aq)、HClO和ClO-分别在三者中占分数(α)随pH变化的关系如图所示。下列表述正确的是

| A.Cl2(g)+H2O⇌2H++ClO-+Cl- K=10-10.9 |
| B.在氯处理水体系中,c(HClO)+c(ClO-)<c(H+)-c(OH-) |
| C.用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时强 |
| D.氯处理饮用水时,在夏季的杀菌效果比在冬季好 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,两种钠盐 、
、 溶液的物质的量浓度均为
溶液的物质的量浓度均为 ,加水稀释时溶液的
,加水稀释时溶液的 与稀释倍数的对数
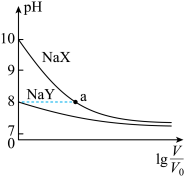
与稀释倍数的对数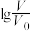 的关系如图所示。下列判断错误的是( )
的关系如图所示。下列判断错误的是( )
 、
、 溶液的物质的量浓度均为
溶液的物质的量浓度均为 ,加水稀释时溶液的
,加水稀释时溶液的 与稀释倍数的对数
与稀释倍数的对数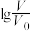 的关系如图所示。下列判断错误的是( )
的关系如图所示。下列判断错误的是( )
A. 、 、 均为弱酸,且 均为弱酸,且 的酸性比 的酸性比 的强 的强 |
B. 的 的 、 、 溶液中,前者对水的电离促进作用较大 溶液中,前者对水的电离促进作用较大 |
C. 点 点 溶液中存在: 溶液中存在: |
D.随着溶液的稀释, 溶液中 溶液中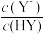 逐渐减小 逐渐减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时, 的
的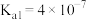 ,
,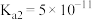 ,已知
,已知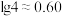 ,下列有关说法
,下列有关说法不正确 的是
 的
的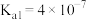 ,
,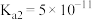 ,已知
,已知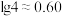 ,下列有关说法
,下列有关说法A.向饱和碳酸钠溶液通入过量 的离子方程式: 的离子方程式: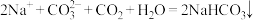 |
B. 的 的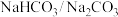 缓冲体系: 缓冲体系: |
C. 溶液中存在如下平衡: 溶液中存在如下平衡: ,则该平衡常数 ,则该平衡常数 |
D.常温下,某 溶液的浓度为 溶液的浓度为 ,该溶液 ,该溶液 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,用NaOH溶液调节H3PO4溶液的pH,溶液中含磷微粒的物质的量分数与pH的关系如下图所示:

下列说法正确的是

下列说法正确的是
A.H3PO4的电离方程式为:H3PO4⇌3H++ |
| B.溶液pH越大,H3PO4的电离程度越小 |
| C.H3PO4的Ka2=1×10-7.25 |
D.pH=5时,c( )<c( )<c( )<c(Na+) )<c(Na+) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
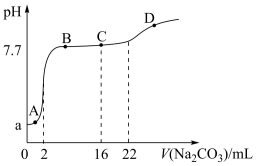
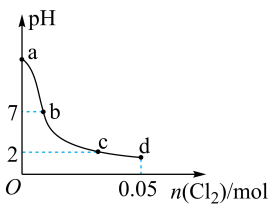
【推荐2】常温下,向 溶液(不考虑空气的影响)中缓慢通入
溶液(不考虑空气的影响)中缓慢通入 ,整个过程中无气体逸出,忽略溶液中体积和温度的变化,测得溶液的pH与通入
,整个过程中无气体逸出,忽略溶液中体积和温度的变化,测得溶液的pH与通入 的物质的量之间的变化曲线如图所示。下列说法错误的是。(不考虑与
的物质的量之间的变化曲线如图所示。下列说法错误的是。(不考虑与 发生的其他反应)
发生的其他反应)
已知:常温下,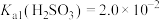 ,
, 。
。
 溶液(不考虑空气的影响)中缓慢通入
溶液(不考虑空气的影响)中缓慢通入 ,整个过程中无气体逸出,忽略溶液中体积和温度的变化,测得溶液的pH与通入
,整个过程中无气体逸出,忽略溶液中体积和温度的变化,测得溶液的pH与通入 的物质的量之间的变化曲线如图所示。下列说法错误的是。(不考虑与
的物质的量之间的变化曲线如图所示。下列说法错误的是。(不考虑与 发生的其他反应)
发生的其他反应)已知:常温下,
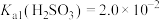 ,
, 。
。
A.a点溶液中,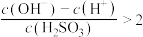 |
B.b点溶液中,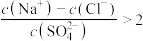 |
C.c点溶液中,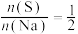 |
D.d点溶液中,水电离出的 和水电离出的 和水电离出的 之积为 之积为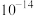 |
您最近半年使用:0次


 溶液中:
溶液中: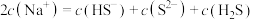
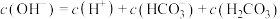
 溶液与pH=11的NaOH溶液等体积混合后:
溶液与pH=11的NaOH溶液等体积混合后:
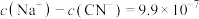

 )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)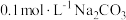 溶液中:
溶液中:


