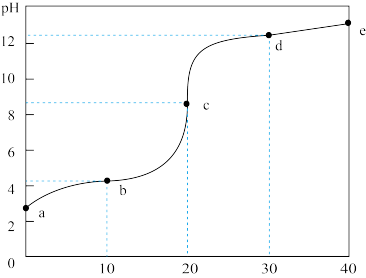
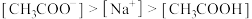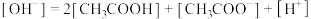常温下,往20mL0.1mol·L-1CH3COOH溶液中滴加等浓度的NaOH溶液,由水电离出的氢氧根离子浓度随滴入NaOH溶液的体积变化如下图所示,下列说法正确的是
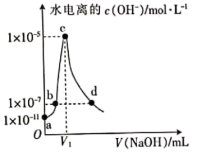

| A.该CH3COOH溶液的电离度为10% | B.c点对应溶液的pH为9 |
| C.V1>20 | D.b、d两点溶液的pH相等 |
更新时间:2021-07-13 13:56:44
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】实验测得0.10
 溶液的pH随温度变化如图:
溶液的pH随温度变化如图:
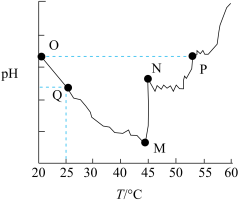
下列说法正确的是

 溶液的pH随温度变化如图:
溶液的pH随温度变化如图:
下列说法正确的是
A.OM段随温度升高溶液的pH减小,原因是 水解被抑制 水解被抑制 |
B.O点溶液和P点溶液中 相等 相等 |
| C.将N点溶液恢复到25℃,pH可能大于Q点 |
D.Q点、M点溶液中均有: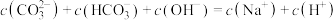 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温下,向20.00mL 的
的 溶液中滴加
溶液中滴加 的
的 溶液,溶液中
溶液,溶液中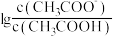 随pH的变化关系如图所示(取
随pH的变化关系如图所示(取 )。
)。

下列说法错误的是
 的
的 溶液中滴加
溶液中滴加 的
的 溶液,溶液中
溶液,溶液中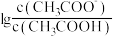 随pH的变化关系如图所示(取
随pH的变化关系如图所示(取 )。
)。
下列说法错误的是
A.常温下, 的电离常数为 的电离常数为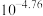 |
B.当溶液的 时、消耗 时、消耗 溶液的体积小于20.00mL 溶液的体积小于20.00mL |
C.a、b、c三点对应的溶液中,水的电离程度大小: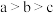 |
D.c点溶液中: |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温下,向VmL0.1mol·L−1的MOH溶液中加入等浓度的盐酸溶液,溶液中由水电离产生的氢离子的−lgc(H+)水随加入盐酸体积的变化如图所示。下列说法正确的是(已知lg2=0.3)
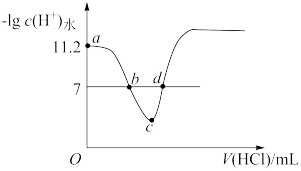

| A.常温下,0.1mol·L−1的MOH溶液溶液的电离平衡常数数量级为10-6 |
B.b点加入盐酸的体积大于 mL mL |
| C.c点溶质为MCl和HCl |
| D.d点溶液中c(M+)=c(Cl−) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】类比是重要的学习方法,类比pH的定义可定义pOH和pKW。在某弱酸HX及其盐NaX的混合溶液中(HX和NaX的含量不确定),c(H+)和c(OH-)存在如图所示的关系,则下列说法不正确的是


| A.图中温度T2>25℃ |
| B.若此混合溶液呈酸性且c(HX)=c(NaX),则HX电离能力大于NaX的水解能力 |
C.位于AB线段上任意点的溶液均有pH=pOH=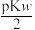 |
| D.图中D点处溶液中离子浓度:c(Na+)>c(X-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知: pH=-lgc(H+), pOH=-lgc(OH-)。 常温下,向某浓度的盐酸溶液中滴加氢氧化钠溶液,所得溶液pOH和pH变化如图所示。 下列说法正确的是
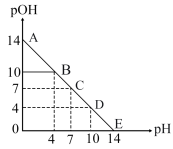

| A.盐酸与NaOH溶液的浓度相等 |
| B.B点和D点水的电离程度相同 |
| C.滴加NaOH溶液改为滴加氨水溶液,该图曲线不变 |
| D.升高温度,滴定过程中pOH+pH>14 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】常温下,Ka(CH3COOH) =2×10-5,Ka(HCOOH)=2×10-4,Kb(NH3·H2O)=2×10-5,下列说法不正确的是
| A.向0.1mol/L HCOOH溶液中加入少量水,溶液中c(H+)/c(HCOOH)增大 |
| B.浓度均为0.1mol/L的HCOOH和NH4Cl溶液,由水电高出的c(OH-)前者小于后者 |
| C.用0.1mol/L的NaOH溶液分别中和等体积等pH的HCOOH和CH3COOH溶液,消耗NaOH溶液的体积相等 |
| D.0.05mol/L的CH3COOH溶液中pH=3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】用亚硫酸盐(X)吸收烟气中的SO2。已知吸收过程中含硫组分物质的量分数(δ)与溶液pH的变化关系如图所示。下列说法中不正确 的是( )


A.若X为(NH4)2SO3,图中b点溶液中n(HSO )∶n(NH )∶n(NH )=1∶3 )=1∶3 |
B.若X为Na2SO3,当吸收液呈中性时:lgc(HSO )-lgc(H2SO3)=5.15 )-lgc(H2SO3)=5.15 |
C.若X为(NH4)2SO3,(NH4)2SO3溶液呈碱性,说明水解程度:SO >NH >NH |
D.若X为Na2SO3,当吸收液pH=1.85时:c(Na+)=2c(HSO )+c(SO )+c(SO ) ) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】乙二胺(H2NCH2CH2NH2)是二元弱碱,在水中的电离原理类似于氨。常温下,向乙二胺溶液中滴加稀盐酸,溶液的pH随离子浓度变化关系如图所示。下列叙述不正确的是


| A.Kb2[H2NCH2CH2NH2]的数量级为10-8 |
B.曲线G代表pH与lg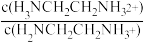 的变化关系 的变化关系 |
| C.H3NCH2CH2NH2Cl溶液中c(H+)>c(OH-) |
| D.0.01mol·L-1H2NCH2CH2NH2电离度约为10% |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】25℃时, H3A 水溶液(一种酸溶液)中含 A 的各种粒子的分布分数(平衡时某种粒子的浓度占各种粒子浓度之和的分数(α)与 pH 的关系如图所示。下列叙述正确的是


| A.根据图,可得 Ka1(H3A )≈10-7 |
| B.将等物质的量的 NaH2A 和 Na2HA 混合物溶于水,所得的溶液中 α(H2Aˉ)=α(HA2-) |
| C.以酚酞为指示剂(变色范围 pH 8.2~10.0),将 NaOH 溶液逐滴加入到 H3A 溶液中,当溶液由无色变为浅红色时停止滴加,则生成 NaH2A |
| D.在上述含 A 的各种粒子的体系中,若 c(H2Aˉ)+5c(A3ˉ)+c(OHˉ)=c(H+),则溶液pH为11.5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】常温下,下列溶液的离子浓度关系正确的是
A. 的 的 溶液中, 溶液中,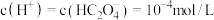 |
B.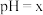 的 的 溶液100mL,稀释10倍后 溶液100mL,稀释10倍后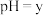 , ,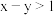 |
C. 的 的 溶液与 溶液与 的NaOH溶液以任意比混合,混合液中: 的NaOH溶液以任意比混合,混合液中: |
D.pH相同的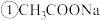 、 、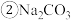 、 、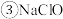 三种溶液中 三种溶液中 : :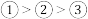 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】常温下,用0.10mol·L-1盐酸分别滴定20.00mL浓度均为0.1mol· L-1 CH3COONa溶液和NaCN溶液,所得滴定曲线如图所示。下列说法正确的是
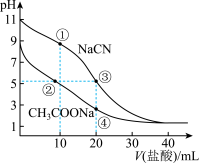

| A.①所示溶液中:c(Cl-)>c(HCN)>c(CN-)>c(OH-) |
| B.②所示溶液中:c(Na+)>c(Cl-)>c(CH3COO-)>c(CH3COOH) |
| C.阳离子物质的量浓度之和:②与③所示溶液中相等 |
| D.④所示溶液中:c(CH3COOH)+ c(H+)-c(OH-)=0.05 mol·L-1 |
您最近一年使用:0次

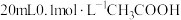 溶液中不断滴入等浓度的
溶液中不断滴入等浓度的 变化如图所示。下列分析
变化如图所示。下列分析