已知: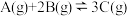
 ,向恒温恒容的密闭容器中充入1molA和2molB发生反应,t1时达到平衡状态Ⅰ,在t2时改变某一条件,t3时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
,向恒温恒容的密闭容器中充入1molA和2molB发生反应,t1时达到平衡状态Ⅰ,在t2时改变某一条件,t3时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
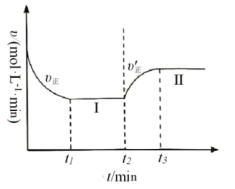
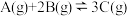
 ,向恒温恒容的密闭容器中充入1molA和2molB发生反应,t1时达到平衡状态Ⅰ,在t2时改变某一条件,t3时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
,向恒温恒容的密闭容器中充入1molA和2molB发生反应,t1时达到平衡状态Ⅰ,在t2时改变某一条件,t3时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。下列说法正确的是
| A.容器内压强不变,表明反应达到平衡 |
| B.t2时改变的条件:向容器中加入C |
C.平衡常数K: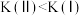 |
D.平衡时A的体积分数 : : |
20-21高二下·山东淄博·期末 查看更多[6]
(已下线)第二单元培优练-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)江西省赣州市赣县第三中学2021-2022学年高二上学期9月考试化学试题山东省济宁市邹城第一中学2021-2022学年高二上学期10月月考化学试卷(已下线)高中化学《新教材变化解读与考法剖析》第二章 化学反应速率与化学平衡(人教版2019选择性必修1)(已下线)专题2.4 化学反应的调控(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)山东省淄博市2020-2021学年高二下学期期末考试化学试题
更新时间:2021-08-07 20:27:36
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】一定温度下容积不变的密闭容器中,对于可逆反应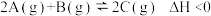 下列说法中正确的是
下列说法中正确的是
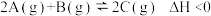 下列说法中正确的是
下列说法中正确的是A.达到化学平衡时, |
B.达到化学平衡后,减小体系压强,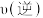 增大, 增大,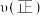 减小,平衡逆向移动 减小,平衡逆向移动 |
| C.当体系压强不随时间变化时,C的物质的量浓度保持不变 |
D. 不变时,反应达到化学平衡状态 不变时,反应达到化学平衡状态 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】200℃、101kPa时,在密闭容器中充入1molH2和1molI2,发生反应I2(g)+H2(g) 2HI(g) ΔH=-14.9 kJ/mol。反应一段时间后,能说明反应已经达到化学平衡状态的是
2HI(g) ΔH=-14.9 kJ/mol。反应一段时间后,能说明反应已经达到化学平衡状态的是
 2HI(g) ΔH=-14.9 kJ/mol。反应一段时间后,能说明反应已经达到化学平衡状态的是
2HI(g) ΔH=-14.9 kJ/mol。反应一段时间后,能说明反应已经达到化学平衡状态的是| A.放出的热量小于14.9 kJ |
| B.反应容器内压强不再变化 |
| C.HI生成的速率与HI分解的速率相等 |
| D.单位时间内消耗a mol H2,同时生成2a mol HI |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】不能 用平衡移动原理解释的事实是
| A.压缩盛有I2和H2混合气体的针筒,气体颜色变深 |
| B.升高温度,NO2和N2O4混合气体的颜色加深 |
| C.打开汽水瓶盖,即有大量气泡逸出 |
| D.用排饱和食盐水的方法收集氯气 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】在一定条件下,恒容密闭容器中反应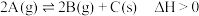 达到平衡后,能使A的浓度增大的措施是
达到平衡后,能使A的浓度增大的措施是
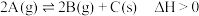 达到平衡后,能使A的浓度增大的措施是
达到平衡后,能使A的浓度增大的措施是| A.降温 | B.增加C的物质的量 |
| C.使用催化剂 | D.减少B的物质的量 |
您最近一年使用:0次
【推荐1】一定温度下,将2molA和2molB两种气体混合放入体积为2L的密闭刚性容器中,发生反应3A(g)+B(g) xC(g)+2D(g),2min末反应达到平衡,生成0.8molD,并测得C的物质的量浓度为0.4mol·L-1,下列说法正确的是( )
xC(g)+2D(g),2min末反应达到平衡,生成0.8molD,并测得C的物质的量浓度为0.4mol·L-1,下列说法正确的是( )
| A.此温度下该反应的平衡常数K等于0.5 |
| B.A的平衡转化率为40% |
| C.x的值为1 |
| D.A和B的平衡转化率相等 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知下列反应的平衡常数:①S(s)+O2(g) SO2(g) K1;②H2(g)+S(s)
SO2(g) K1;②H2(g)+S(s) H2S(g) K2。则反应H2(g)+SO2(g)
H2S(g) K2。则反应H2(g)+SO2(g) O2(g)+H2S(g)的平衡常数是
O2(g)+H2S(g)的平衡常数是
 SO2(g) K1;②H2(g)+S(s)
SO2(g) K1;②H2(g)+S(s) H2S(g) K2。则反应H2(g)+SO2(g)
H2S(g) K2。则反应H2(g)+SO2(g) O2(g)+H2S(g)的平衡常数是
O2(g)+H2S(g)的平衡常数是| A.K1-K2 | B.K2-K1 | C. | D.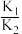 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】下列选项中的图象与其解释或得出的结论对应关系正确的是
| A | B | C | D | |
| 图象 | 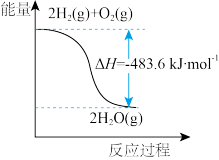 | 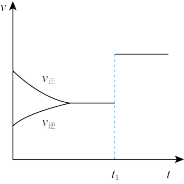 | 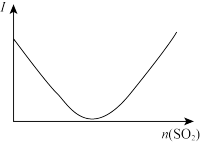 | 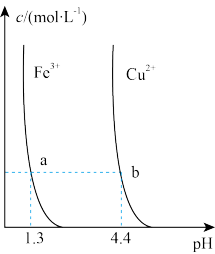 |
| 解释或结论 | 热化学方程式是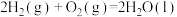 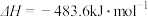 | 某恒容容器中发生反应:X(g)+Y(g)  2Z(g), 2Z(g), 时刻改变的反应条件可能为增大压强 时刻改变的反应条件可能为增大压强 | 向NaOH溶液中通入 至过量,溶液导电性I的变化 至过量,溶液导电性I的变化 | T℃时, 、 、 的溶解平衡曲线, 的溶解平衡曲线,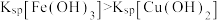 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】某化学科研小组研究在其他条件不变时,改变某一条件对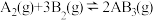 化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是
化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是
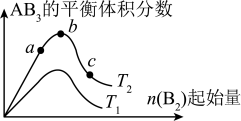
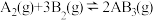 化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是
化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据如图可得出的判断结论正确的是
| A.反应速率:b>a>c |
| B.达到平衡时,AB3的物质的量大小为:b>c>a |
| C.若T2>T1,则正反应一定是吸热反应 |
| D.达到平衡时A2的转化率大小为:b>a>c |
您最近一年使用:0次

 Fe(s)+CO2(g)的平衡常数K=0.25。若在2L密闭容器中加入0.02mol FeO(s),并通入xmol CO,t℃时反应达到平衡.此时FeO(s)转化率为50%,则x的值为( )
Fe(s)+CO2(g)的平衡常数K=0.25。若在2L密闭容器中加入0.02mol FeO(s),并通入xmol CO,t℃时反应达到平衡.此时FeO(s)转化率为50%,则x的值为( )