25°C时,将100mL0.1mol·L-1CH3COOH溶液与0.005molNaOH固体混合,使之充分反应。然后向该混合溶液中通入HCl或加入NaOH固体(忽略体积和温度的变化),溶液pH变化如图所示。下列说法不正确的是


| A.b点溶液中阴离子总数>2倍d点溶液中阴离子总数 |
| B.a→b→c的过程中,始终存在c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| C.a→d→e的过程中,始终存在c+CH3COO-)+c(CH3COOH)≥c(Cl-) |
| D.a→b→c和a→d→e过程中,共只能找出两个点,该点处由水电离出来的c(H+)=10-7mol·L-1 |
21-22高三上·浙江·阶段练习 查看更多[3]
浙江省名校新高考研究联盟(Z20联盟)2022届高三上学期第一次联考化学试题(已下线)解密10 水溶液中的离子平衡(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)2022年浙江省6月高考真题变式题21-25
更新时间:2021-09-17 08:44:48
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,关于下列溶液的说法正确的是
A.pH=7.8的NH4HCO3溶液中:c( )>c( )>c( )>c(NH3•H2O)>c(H2CO3) )>c(NH3•H2O)>c(H2CO3) |
| B.某溶液中由水电离出的c(H+)=1×10-a mol·L-1,则该溶液的pH=a |
C.H2C2O4溶液中c( )=c(H2C2O4)时pH=1.12,则H2C2O4的Ka2=10-1.12 )=c(H2C2O4)时pH=1.12,则H2C2O4的Ka2=10-1.12 |
| D.0.1 mol·L-1的硫酸钾溶液导电能力比同浓度的氯化钾溶液强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各选项所述的两个量中,前者一定大于后者的是
| A.相同温度下,pH相同的NaOH溶液和Na2CO3溶液中由水电离出的c(OH-) |
B.NH4Cl溶液中NH 和Cl-的数目 和Cl-的数目 |
| C.用0.1 mol/L的盐酸中和pH、体积均相同的氨水和NaOH溶液消耗盐酸体积 |
| D.纯水在100℃和25℃时pH |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】用0.1000mol/LNaOH溶液滴定20.00mL未知浓度的盐酸(酚酞作指示剂)的滴定曲线如图所示。下列说法正确的是( )


| A.水的电离程度:a<b |
| B.盐酸的物质的量浓度为0.010mol/L |
| C.指示剂刚变色时,说明盐酸与NaOH恰好完全反应 |
| D.当滴加NaOH溶液30.00mL时(忽略反应前后体积变化),该混合液的pH=1+lg5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】有①NaOH 溶液 ②Na2CO3 溶液 ③CH3COONa 溶液各 10mL,物质的量浓度均为0.1mol·L-1,下列说法正确的是
| A.三种溶液 pH 的大小顺序是①>③>② |
| B.三种溶液中由水电离出的 OH-浓度大小顺序是②>③>① |
| C.若将三种溶液稀释相同倍数,pH 变化最大的是③ |
| D.若分别加入 10mL0.1mol·L-1 盐酸后,pH 最大的是① |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,向0.1mol/L的HA溶液中滴加NaOH溶液,溶液中1gc(HA)、1gc(A–)、lgc(H+) 和 1gc(OH-)随 pH 变化的关系如下图所示(假设整个过程中溶液体积不变)。Ka为HA 的电离常数,下列说法错误的是
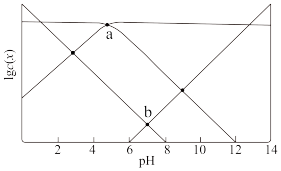

| A.b点时,c(A–)= c(Na+) |
| B.a点时,pH=-lgKa |
C.溶液中存在 mol/L的关系 mol/L的关系 |
| D.溶液pH由2到6的变化过程中,水的电离程度逐渐增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】部分弱电解质的电离常数如下表:
下列说法错误的是
| 弱电解质 | HCOOH | CH3COOH |  |  |
| 电离常数(25℃) | 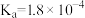 | Ka=1.8×10-5 |  |   |
A. 、 、 、 、 、 、 在溶液中不可以大量共存 在溶液中不可以大量共存 |
B.向 溶液中加NaOH至 溶液中加NaOH至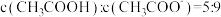 ,此时溶液的pH=5 ,此时溶液的pH=5 |
| C.中和等体积、等pH的HCOOH和HClO消耗NaOH的量前者小于后者 |
D.等体积、等浓度的 和 和 中离子总数: 中离子总数: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下联氨(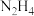 )的水溶液中有:① N2H4+H2O⇌N2H5++OH- K1
)的水溶液中有:① N2H4+H2O⇌N2H5++OH- K1
② N2H5++H2O⇌N2H62++OH- K2,该溶液中微粒的物质的量分数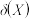 随
随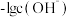 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是

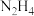 )的水溶液中有:① N2H4+H2O⇌N2H5++OH- K1
)的水溶液中有:① N2H4+H2O⇌N2H5++OH- K1② N2H5++H2O⇌N2H62++OH- K2,该溶液中微粒的物质的量分数
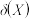 随
随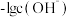 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是
A.图中Ⅲ对应的液粒为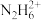 |
B.由图可知, |
C.若 点为 点为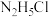 溶液,则存在: 溶液,则存在: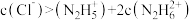 |
D.反应②为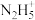 的水解方程式 的水解方程式 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】氯在饮用水处理中常用作杀菌剂,且 HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g)⇌Cl2(aq) K1=10-1.2
Cl2(aq)+ H2O⇌HClO+H++Cl-K2=10-3.4
HClO⇌H++ClO-Ka=?
其中Cl2(aq)、HClO 和 ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。下列表述正确的是

Cl2(g)⇌Cl2(aq) K1=10-1.2
Cl2(aq)+ H2O⇌HClO+H++Cl-K2=10-3.4
HClO⇌H++ClO-Ka=?
其中Cl2(aq)、HClO 和 ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。下列表述正确的是

A.Cl2(g)+H2O 2H++ClO-+Cl-K=10-10.9 2H++ClO-+Cl-K=10-10.9 |
| B.在氯处理水体系中,c(HClO)+c(ClO-)=c(H+)-c(OH-) |
| C.用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时差 |
| D.氯处理饮用水时,在夏季的杀菌效果比在冬季好 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法中,正确的是
| A.向盐酸中加入氨水至中性,溶液中c(NH4+)/ c(C l- )=1 |
| B.25℃时,Mg(OH)2固体在20 mL 0.01mol•L-1氨水中的Ksp比在20mL0.01mol•L-1 NH4Cl溶液中的Ksp小 |
| C.pH试纸测得新制氯水的pH为4.5 |
| D.FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,浓度均为0.1 mol/L的4种溶液pH如下表:
下列说法正确的是
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 4.0 |
| A.0.1 mol/L Na2CO3溶液加水,稀释后溶液中所有离子的浓度均减少 |
| B.NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-) |
| C.NaHSO3溶液中:c(Na+)>c(HSO3-) > c(H2SO3)>c(SO32-) > c(H+)>c(OH-) |
| D.向NaClO溶液中滴加硫酸至中性时,2c(SO42-)= c(HClO) |
您最近一年使用:0次