合成氨技术的创立开辟了人工固氮的重要途径。回答下列问题:
(1)德国化学家F.Haber从1902年开始研究N2和H2直接合成NH3。在1.01×105Pa、250℃时,将1molN2和1molH2加入刚性容器中充分反应,测得NH3的物质的量分数为4%,其他条件不变,温度升高至450℃,测得NH3的物质的量分数为2.5%,则可判断合成氨反应△H___ 0(填“ ”或“
”或“ ”)。
”)。
(2)在2L密闭容器中,投入4molN2和6molH2,在一定条件下生成NH3,测得不同温度下,平衡时NH3的物质的量数据如表:
①温度T1___ (填“>”“<”或“=”)T3。
②在T2温度下,达到平衡时N2的转化率为__ 。
(3)T℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g) 2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
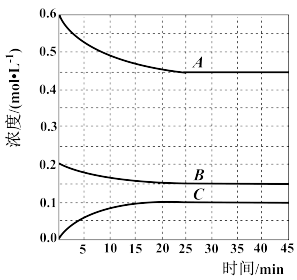
①表示H2浓度变化的曲线是___ (填“A”、“B”或“C”。与(1)中的实验条件(1.01×105Pa、450℃)相比,改变的条件可能是___ 。
②在0~25min内N2的平均反应速率为___ 。在该条件下反应的平衡常数为___ (保留两位有效数字)。
(1)德国化学家F.Haber从1902年开始研究N2和H2直接合成NH3。在1.01×105Pa、250℃时,将1molN2和1molH2加入刚性容器中充分反应,测得NH3的物质的量分数为4%,其他条件不变,温度升高至450℃,测得NH3的物质的量分数为2.5%,则可判断合成氨反应△H
 ”或“
”或“ ”)。
”)。(2)在2L密闭容器中,投入4molN2和6molH2,在一定条件下生成NH3,测得不同温度下,平衡时NH3的物质的量数据如表:
| 温度/K | T1 | T2 | T3 | T4 |
| n(NH3)/mol | 3.6 | 3.2 | 2.8 | 2.0 |
①温度T1
②在T2温度下,达到平衡时N2的转化率为
(3)T℃时,在恒温恒容的密闭条件下发生反应:N2(g)+3H2(g)
 2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
2NH3(g),反应过程中各物质浓度的变化曲线如图所示:
①表示H2浓度变化的曲线是
②在0~25min内N2的平均反应速率为
更新时间:2021-10-14 13:17:02
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】化学在生产生活中无处不在。
(1)某汽车安全气囊的气体发生剂主要含有叠氮化钠( )、
)、 、
、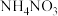 等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
① 是气体发生剂,是
是气体发生剂,是_______ (填“离子”或“共价”)化合物。
②汽车受到猛烈碰撞时,点火器点火引发 迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是_______ (填字母)。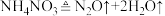 ,推测安全气囊中
,推测安全气囊中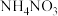 的作用有
的作用有_______ 。
(2)以 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。_______ 转化为化学能;
②根据数据计算,分解1mol 需
需_______ (填“吸收”或“释放”)_______ kJ的能量。
(3)一定条件下,在2L密闭容器内,反应 ,
,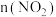 时间变化如表:
时间变化如表:
①0~2s内用 表示该反应的平均速率为
表示该反应的平均速率为_______ 。
②在第5s时, 的转化率为
的转化率为_______ 。(转化率是指某一反应物转化的百分率。)
(4)氮气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和 ,在一定条件下发生反应:
,在一定条件下发生反应: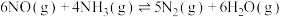 。
。
①能说明该反应已达到平衡状态的标志是_______ (填标号)
A.反应速率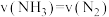
B.容器内压强不再随时间而发生变化
C.容器内 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化
D.容器内
②某次实验中测得容器内NO及 的物质的量随时间变化如图。
的物质的量随时间变化如图。
_______  (填>“<”或“=”),d点对应的速率关系是
(填>“<”或“=”),d点对应的速率关系是
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(1)某汽车安全气囊的气体发生剂主要含有叠氮化钠(
 )、
)、 、
、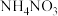 等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。
等物质。当汽车发生碰撞时,气体发生剂产生大量气体使气囊迅速膨胀,从而起到保护作用。①
 是气体发生剂,是
是气体发生剂,是②汽车受到猛烈碰撞时,点火器点火引发
 迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是
迅速分解,生成氢气和金属钠,同时释放大量的热,关于该反应过程中的能量变化示意图正确的是A.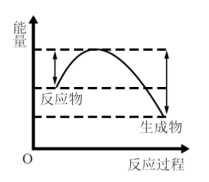 B.
B. C.
C.
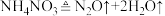 ,推测安全气囊中
,推测安全气囊中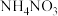 的作用有
的作用有(2)以
 为催化剂的光热化学循环分解
为催化剂的光热化学循环分解 反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。
反应为温室气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示。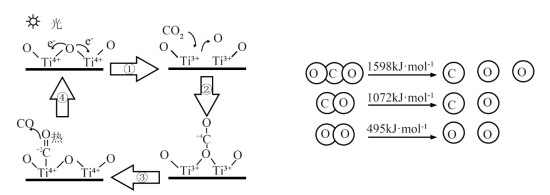
②根据数据计算,分解1mol
 需
需(3)一定条件下,在2L密闭容器内,反应
 ,
,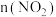 时间变化如表:
时间变化如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
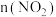 /mol /mol | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
 表示该反应的平均速率为
表示该反应的平均速率为②在第5s时,
 的转化率为
的转化率为(4)氮气可作为脱硝剂,在恒温恒容密闭容器中充入一定量的NO和
 ,在一定条件下发生反应:
,在一定条件下发生反应: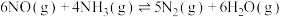 。
。①能说明该反应已达到平衡状态的标志是
A.反应速率
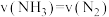
B.容器内压强不再随时间而发生变化
C.容器内
 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化D.容器内

②某次实验中测得容器内NO及
 的物质的量随时间变化如图。
的物质的量随时间变化如图。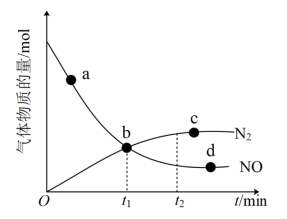

 (填>“<”或“=”),d点对应的速率关系是
(填>“<”或“=”),d点对应的速率关系是
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】近年我国汽车拥有量呈较快增长趋势,汽车尾气已成为重要的空气污染物。回答下列问题:
(l)汽车发动机工作时会引起反应:N2(g)+O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。2000K时,向容积为2L的密闭容器中充入2molN2与2molO2,发生上述反应,经过5min达到平衡,此时容器内NO的体积分数为0.75% .则该反应在5min内的平均反应速率v(O2)=
2NO(g),是导致汽车尾气中含有NO的原因之一。2000K时,向容积为2L的密闭容器中充入2molN2与2molO2,发生上述反应,经过5min达到平衡,此时容器内NO的体积分数为0.75% .则该反应在5min内的平均反应速率v(O2)=_______ mol/(Lmin),N2的平衡转化率为_______ ,2000K时该反应的平衡常数K=_____ 。
(2)一定量NO发生分解的过程中,NO的转化率随时间变化的关系如右图所示。
① 反应2NO(g) N2(g)+O2(g)为
N2(g)+O2(g)为______ 反应(填“吸热”或“放热”) ;
②一定温度下,能够说明反应2NO(g) N2(g)+O2(g)已达到平衡的是
N2(g)+O2(g)已达到平衡的是_____ (填序号);
a.容器内的压强不发生变化
b.混合气体的密度不发生变化
c. 2NO、N2、O2的浓度保持不变
d.单位时间内分解4molNO,同时生成2molN2
③ 在四个容积和温度均完全相同的密闭容器中分别加入下列物质,相应物质的量(mol)如下表所示。相同条件下达到平衡后,N2的体积分数最大的是_______ (填容器代号);
(3)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx。可用CH4催化还原NOx以消除氮氧化物污染。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ·mol-1
①写出CH4与NO反应生成N2、CO2、H2O(g)的热化学方程式:___________ ;
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为___________________ 。
(l)汽车发动机工作时会引起反应:N2(g)+O2(g)
 2NO(g),是导致汽车尾气中含有NO的原因之一。2000K时,向容积为2L的密闭容器中充入2molN2与2molO2,发生上述反应,经过5min达到平衡,此时容器内NO的体积分数为0.75% .则该反应在5min内的平均反应速率v(O2)=
2NO(g),是导致汽车尾气中含有NO的原因之一。2000K时,向容积为2L的密闭容器中充入2molN2与2molO2,发生上述反应,经过5min达到平衡,此时容器内NO的体积分数为0.75% .则该反应在5min内的平均反应速率v(O2)=(2)一定量NO发生分解的过程中,NO的转化率随时间变化的关系如右图所示。
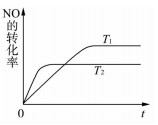
① 反应2NO(g)
 N2(g)+O2(g)为
N2(g)+O2(g)为②一定温度下,能够说明反应2NO(g)
 N2(g)+O2(g)已达到平衡的是
N2(g)+O2(g)已达到平衡的是a.容器内的压强不发生变化
b.混合气体的密度不发生变化
c. 2NO、N2、O2的浓度保持不变
d.单位时间内分解4molNO,同时生成2molN2
③ 在四个容积和温度均完全相同的密闭容器中分别加入下列物质,相应物质的量(mol)如下表所示。相同条件下达到平衡后,N2的体积分数最大的是
容器代号 | NO | N2 | O2 |
A | 2 | 0 | 0 |
B | 0 | l | l |
C | 0.4 | 0.6 | 0.8 |
D | l | 0.5 | 0.4 |
(3)当发动机采用稀薄燃烧时,尾气中的主要污染物为NOx。可用CH4催化还原NOx以消除氮氧化物污染。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867kJ·mol-1
①写出CH4与NO反应生成N2、CO2、H2O(g)的热化学方程式:
②使用催化剂可以将汽车尾气的主要有害成分一氧化碳(CO)和氮氧化物(NOx)转化为无毒气体,该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某校课外活动小组利用草酸( )溶液和酸性
)溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,该反应的离子方程式为
溶液之间的反应来探究外界条件改变对化学反应速率的影响,该反应的离子方程式为 ,实验记录如表。
,实验记录如表。
回答下列问题:
(1)通过实验①、②可探究草酸浓度的改变对反应速率的影响,则
_______ ;通过实验_______ 可探究温度变化对化学反应速率的影响。由实验②③可推断
_______ (填“>”“<”或“=”)10s。
(2)若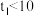 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是_______ ;利用实验②中数据,用 的浓度变化表示的反应平均速率为
的浓度变化表示的反应平均速率为_______  (保留2位有效数字)。
(保留2位有效数字)。
(3)某同学取1支试管加入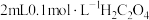 溶液,另取1支试管加入
溶液,另取1支试管加入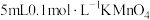 酸性溶液,将两支试管中溶液混合,该同学始终没有看到溶液完全褪色,其原因是
酸性溶液,将两支试管中溶液混合,该同学始终没有看到溶液完全褪色,其原因是_______ 。
(4)已知一定条件下40℃时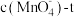 的变化曲线如图。若保持其他条件不变,请在图中用虚线画出20℃时
的变化曲线如图。若保持其他条件不变,请在图中用虚线画出20℃时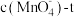 的变化曲线示意图
的变化曲线示意图_______ 。

 )溶液和酸性
)溶液和酸性 溶液之间的反应来探究外界条件改变对化学反应速率的影响,该反应的离子方程式为
溶液之间的反应来探究外界条件改变对化学反应速率的影响,该反应的离子方程式为 ,实验记录如表。
,实验记录如表。| 实验序号 | 实验温度/℃ |  溶液(含硫酸) 溶液(含硫酸) |  溶液 溶液 |  | 溶液颜色褪至无色时所需时间/s | ||
| V/mL | 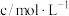 | V/mL | 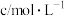 | V/mL | |||
| ① | 20 | 2 | 0.02 | 5 | 0.1 | 5 |  |
| ② | 20 | 2 | 0.02 | 4 | 0.1 |  | 10 |
| ③ | 40 | 2 | 0.02 | 4 | 0.1 | 6 |  |
(1)通过实验①、②可探究草酸浓度的改变对反应速率的影响,则


(2)若
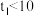 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是 的浓度变化表示的反应平均速率为
的浓度变化表示的反应平均速率为 (保留2位有效数字)。
(保留2位有效数字)。(3)某同学取1支试管加入
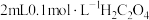 溶液,另取1支试管加入
溶液,另取1支试管加入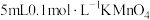 酸性溶液,将两支试管中溶液混合,该同学始终没有看到溶液完全褪色,其原因是
酸性溶液,将两支试管中溶液混合,该同学始终没有看到溶液完全褪色,其原因是(4)已知一定条件下40℃时
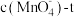 的变化曲线如图。若保持其他条件不变,请在图中用虚线画出20℃时
的变化曲线如图。若保持其他条件不变,请在图中用虚线画出20℃时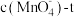 的变化曲线示意图
的变化曲线示意图
您最近一年使用:0次
【推荐1】含碳物质的转化,有利于“减碳”和可持续性发展,有重要的研究价值.回答下列问题:
(1)已知CO(g)+H2O(g) CO2(g)+H2(g) △H=﹣41 kJ•mol-1,下列措施中有利于提高CO平衡转化率的是
CO2(g)+H2(g) △H=﹣41 kJ•mol-1,下列措施中有利于提高CO平衡转化率的是______ (填标号)。
A.增大压强 B.降低温度
C.提高原料气中H2O(g)的比例 D.使用高效催化剂
(2)用惰性电极电解KHCO3溶液可将空气中的CO2转化为甲酸根(HCOO-)和 ,其电极反应式为
,其电极反应式为______________ ;若电解过程中转移1 mol电子,则阳极生成气体的体积为______ L(标准状况)。
(3)乙苯催化脱氢制取苯乙烯的反应为:
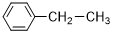 (g)+CO2(g)
(g)+CO2(g)
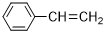 (g)+CO(g)+H2O(g),其反应历程如下:
(g)+CO(g)+H2O(g),其反应历程如下:
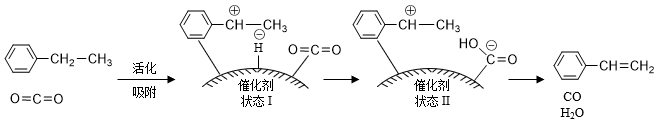
①由原料到状态Ⅰ的过程能量______ (填“放出”或“吸收”)。
②一定温度下,向恒容密闭容器中充入2 mol乙苯和2 mol CO2,起始压强为P0,平衡时容器内气体总物质的量为5 mol,则乙苯的转化率为_____ ,用平衡分压代替平衡浓度表示的化学平衡常数Kp=______ 。
(1)已知CO(g)+H2O(g)
 CO2(g)+H2(g) △H=﹣41 kJ•mol-1,下列措施中有利于提高CO平衡转化率的是
CO2(g)+H2(g) △H=﹣41 kJ•mol-1,下列措施中有利于提高CO平衡转化率的是A.增大压强 B.降低温度
C.提高原料气中H2O(g)的比例 D.使用高效催化剂
(2)用惰性电极电解KHCO3溶液可将空气中的CO2转化为甲酸根(HCOO-)和
 ,其电极反应式为
,其电极反应式为(3)乙苯催化脱氢制取苯乙烯的反应为:
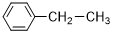 (g)+CO2(g)
(g)+CO2(g)
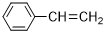 (g)+CO(g)+H2O(g),其反应历程如下:
(g)+CO(g)+H2O(g),其反应历程如下:
①由原料到状态Ⅰ的过程能量
②一定温度下,向恒容密闭容器中充入2 mol乙苯和2 mol CO2,起始压强为P0,平衡时容器内气体总物质的量为5 mol,则乙苯的转化率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】用下图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是16.8℃,沸点是44.8℃。已知发生装置中所涉及反应的化学方程式为:Na2SO3(s) + H2SO4(85%)→ Na2SO4 + H2O + SO2↑

(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合装置并将其序号填入下面的空格中。Ⅰ、Ⅱ、Ⅲ处连接的装置分别是___________ 、___________ 、___________ 。

(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在:① 加热催化剂;② 滴加浓硫酸的顺序中,应采取的操作是先___________ 后___________ (填编号)。在制取SO3的过程中,若温度过高,SO2的转化率会___________ (填“升高”、“不变”或“降低”)。
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你根据以下推测的原因说明相应的验证方法。
① Na2SO3已变质。验证方法___________ 。
② 甲中用稀H2SO4代替浓H2SO4。验证方法___________ 。
(4)用a mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了b g,则实验中SO2的转化率为___________ %(用含a、b的代数式填写)。

(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合装置并将其序号填入下面的空格中。Ⅰ、Ⅱ、Ⅲ处连接的装置分别是

(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在:① 加热催化剂;② 滴加浓硫酸的顺序中,应采取的操作是先
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你根据以下推测的原因说明相应的验证方法。
① Na2SO3已变质。验证方法
② 甲中用稀H2SO4代替浓H2SO4。验证方法
(4)用a mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了b g,则实验中SO2的转化率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】铬铁矿的主要成分的化学式为 FeO ·Cr2O3,还含有 SiO2、Al2O3等杂质。工业上常采用固体碱熔氧法用铬铁矿粉制备重铬酸钾,流程为

(1)铬铁矿经粉碎处理的目的是__ (填“加快”或“减慢”)反应速率。
(2)灼烧是中学化学中常用的操作方法,如在实验室中将铬铁矿和碳酸钠固体混合物灼烧,该过程不需要的仪器是___ (填序号)。
A.陶瓷坩埚 B.铁坩埚 C.三脚架 D.泥三角 E.酒精灯 F.蒸发皿
(3)铬铁矿中的 SiO2和 Al2O3 在反应器中与纯碱共热反应转变为可溶性盐,故 Al2O3与碳酸钠反应生成的可溶性盐的名称 为:________________ 。
(4)化合物 NaFeO2中 Fe 的化合价为______ (填序号)。
A.+2 B.+3 C.+6
该价态对应的简单离子与该元素常见的另一种简单离子相比 ,更稳定的是______ (填序号)。
A.Fe3+ B .Fe2+
(5)通过途径 1 从 Na2CrO4溶液获得 K2Cr2O7晶体,操作步骤有:酸化→加 KCl 固体→操作 a→过滤→洗涤 →干燥
①操作 a 的名称____________________ (填序号)。
A.蒸发结晶 B.蒸发浓缩,冷却结晶 C.蒸馏 D. 萃取
②“酸化”调节溶液 pH<5 其主要目的是_____ (填序号)。
A.增大H+浓度,加快反应速率
B.使2CrO +2H+
+2H+ Cr2O
Cr2O +H2O的平衡向正向移动,尽量将CrO
+H2O的平衡向正向移动,尽量将CrO 转化为Cr2O
转化为Cr2O
(6)将最后制得的晶体溶解、酸化就制成了化学实验中常用的氧化剂——酸性重铬酸钾。酸化过程中常用的酸是_________ (选填“盐酸”、“硫酸”或“硝酸”)。

(1)铬铁矿经粉碎处理的目的是
(2)灼烧是中学化学中常用的操作方法,如在实验室中将铬铁矿和碳酸钠固体混合物灼烧,该过程不需要的仪器是
A.陶瓷坩埚 B.铁坩埚 C.三脚架 D.泥三角 E.酒精灯 F.蒸发皿
(3)铬铁矿中的 SiO2和 Al2O3 在反应器中与纯碱共热反应转变为可溶性盐,故 Al2O3与碳酸钠反应生成的可溶性盐的
(4)化合物 NaFeO2中 Fe 的化合价为
A.+2 B.+3 C.+6
该价态对应的简单离子与该元素常见的另一种简单离子相比 ,更稳定的是
A.Fe3+ B .Fe2+
(5)通过途径 1 从 Na2CrO4溶液获得 K2Cr2O7晶体,操作步骤有:酸化→加 KCl 固体→操作 a→过滤→洗涤 →干燥
①操作 a 的名称
A.蒸发结晶 B.蒸发浓缩,冷却结晶 C.蒸馏 D. 萃取
②“酸化”调节溶液 pH<5 其主要目的是
A.增大H+浓度,加快反应速率
B.使2CrO
 +2H+
+2H+ Cr2O
Cr2O +H2O的平衡向正向移动,尽量将CrO
+H2O的平衡向正向移动,尽量将CrO 转化为Cr2O
转化为Cr2O
(6)将最后制得的晶体溶解、酸化就制成了化学实验中常用的氧化剂——酸性重铬酸钾。酸化过程中常用的酸是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】采用催化剂存在下臭氧氧化—碱吸收法同时脱除SO2和NO。氧化过程中反应原理及反应热、活化能数据如下:
反应Ⅰ:NO(g)+O3(g) NO2(g)+O2(g) ΔH1=-200.9 kJ/mol Ea1=3.2 kJ/mol
NO2(g)+O2(g) ΔH1=-200.9 kJ/mol Ea1=3.2 kJ/mol
反应Ⅱ:SO2(g)+O3(g) SO3(g)+O2(g) ΔH2=-241.6 kJ/mol Ea2=56 kJ/mol
SO3(g)+O2(g) ΔH2=-241.6 kJ/mol Ea2=56 kJ/mol
已知该体系中臭氧会发生分解反应2O3(g) 3O2(g)。一定条件下,向容积为2 L的反应器充入2.0 mol NO、2.0 mol SO2的模拟烟气和4.0 mol O3,升高温度,体系中NO和SO2的转化率随温度T变化如图所示。
3O2(g)。一定条件下,向容积为2 L的反应器充入2.0 mol NO、2.0 mol SO2的模拟烟气和4.0 mol O3,升高温度,体系中NO和SO2的转化率随温度T变化如图所示。

(1)由图像可知,相同温度下NO的转化率远高于SO2,结合题中数据分析其可能原因:________ 。
(2)Q点发生分解反应的臭氧占充入臭氧总量的10%,则此时体系中剩余的O3物质的量是________ mol,反应Ⅱ在此温度下的平衡常数为________ (保留小数点后2位)。
反应Ⅰ:NO(g)+O3(g)
 NO2(g)+O2(g) ΔH1=-200.9 kJ/mol Ea1=3.2 kJ/mol
NO2(g)+O2(g) ΔH1=-200.9 kJ/mol Ea1=3.2 kJ/mol反应Ⅱ:SO2(g)+O3(g)
 SO3(g)+O2(g) ΔH2=-241.6 kJ/mol Ea2=56 kJ/mol
SO3(g)+O2(g) ΔH2=-241.6 kJ/mol Ea2=56 kJ/mol已知该体系中臭氧会发生分解反应2O3(g)
 3O2(g)。一定条件下,向容积为2 L的反应器充入2.0 mol NO、2.0 mol SO2的模拟烟气和4.0 mol O3,升高温度,体系中NO和SO2的转化率随温度T变化如图所示。
3O2(g)。一定条件下,向容积为2 L的反应器充入2.0 mol NO、2.0 mol SO2的模拟烟气和4.0 mol O3,升高温度,体系中NO和SO2的转化率随温度T变化如图所示。
(1)由图像可知,相同温度下NO的转化率远高于SO2,结合题中数据分析其可能原因:
(2)Q点发生分解反应的臭氧占充入臭氧总量的10%,则此时体系中剩余的O3物质的量是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】研究表明,氮氧化物(NOx)和二氧化硫在形成雾霾时与大气中的氨有关,其转化关系如下图所示。

(1)NH3的电子式是______ 。
(2)NH4NO3溶液中的离子浓度由大到小顺序是_____ 。
(3)①已知:SO2生成 SO3总反应方程式是:2SO2(g)+O2(g)⇌2SO3(g)。此反应可通过如下两步完成:2NO(g)+O2 (g ) ⇌2NO2(g),写出第二步的化学方程式______ 。
②一定温度下,向 2 L 恒容密闭容器中充入 NO2和 SO2各 1 mol,5min 达到平衡,此时容器中 NO2和
NO 的浓度之比为 1∶3,则 NO2的平衡转化率是_____ 。
(4)利用NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。
①制备少量NaClO2,其装置如下图所示:

装置 I 控制温度在 35~55℃,通入 SO2将 NaClO3还原为 ClO2(沸点:11℃),反应的离子方程式是_____ ,装置 Ⅱ中反应生成NaClO2,此反应中作为氧化剂的是___ ,反应后装置Ⅲ中溶液中阴离子除了  、
、 、Cl-、ClO-、OH-外还可能含有的一种阴离子是
、Cl-、ClO-、OH-外还可能含有的一种阴离子是_____ 。
②用制得的NaClO2/H2O2酸性复合吸收剂同时对 NO、SO2进行氧化得到硝酸和硫酸而除去。在温度一定时,n(H2O2)/n(NaClO2)、溶液 pH 对脱硫脱硝的影响如下图所示:
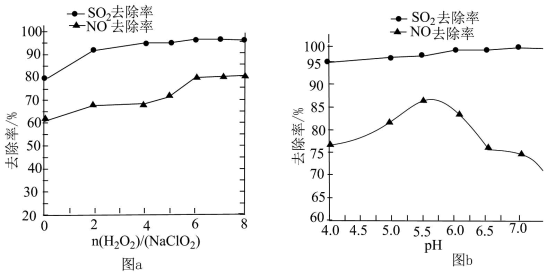
从图 a 和图 b 中可知脱硫脱硝最佳条件是______ 。图 b 中SO2的去除率随 pH 的增大而增大,而NO 的去除率在 pH>5.5 时反而减小,请解释 NO 去除率减小的可能原因是_______ 。

(1)NH3的电子式是
(2)NH4NO3溶液中的离子浓度由大到小顺序是
(3)①已知:SO2生成 SO3总反应方程式是:2SO2(g)+O2(g)⇌2SO3(g)。此反应可通过如下两步完成:2NO(g)+O2 (g ) ⇌2NO2(g),写出第二步的化学方程式
②一定温度下,向 2 L 恒容密闭容器中充入 NO2和 SO2各 1 mol,5min 达到平衡,此时容器中 NO2和
NO 的浓度之比为 1∶3,则 NO2的平衡转化率是
(4)利用NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。
①制备少量NaClO2,其装置如下图所示:

装置 I 控制温度在 35~55℃,通入 SO2将 NaClO3还原为 ClO2(沸点:11℃),反应的离子方程式是
 、
、 、Cl-、ClO-、OH-外还可能含有的一种阴离子是
、Cl-、ClO-、OH-外还可能含有的一种阴离子是②用制得的NaClO2/H2O2酸性复合吸收剂同时对 NO、SO2进行氧化得到硝酸和硫酸而除去。在温度一定时,n(H2O2)/n(NaClO2)、溶液 pH 对脱硫脱硝的影响如下图所示:

从图 a 和图 b 中可知脱硫脱硝最佳条件是
您最近一年使用:0次
【推荐3】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:
(1)若在一个容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2,在一定条件下发生反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则平衡时H2的转化率为
2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则平衡时H2的转化率为____ 。
(2)平衡后,若要提高H2的转化率,可以采取的措施有____ 。
(3)若在2L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g) 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
请完成下列问题:
①试比较K1、K2的大小,K1____ K2(填“<”、“>”或“=”)。
②下列各项能作为判断该反应达到化学平衡状态的依据是____ (填序号字母)。
A.容器内N2、H2、NH3的物质的量浓度之比为1∶3∶2 B.v(N2)正=3v(H2)逆
C.容器内压强保持不变 D.混合气体的密度保持不变
③400℃时,反应2NH3(g) N2(g)+3H2(g)的化学平衡常数为
N2(g)+3H2(g)的化学平衡常数为____ 。若某时刻测得NH3、N2和H2物质的量均 为2mol时,则该时刻反应方向为:____ (填“正反应方向”、“逆反应方向”或“不”)移动。
(1)若在一个容积为2L的密闭容器中加入0.2mol的N2和0.6mol的H2,在一定条件下发生反应:N2(g)+3H2(g)
 2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则平衡时H2的转化率为
2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2mol。则平衡时H2的转化率为(2)平衡后,若要提高H2的转化率,可以采取的措施有
| A.加了催化剂 | B.增大容器体积 | C.降低反应体系的温度 | D.加入一定量N2 |
 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:| T/℃ | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
①试比较K1、K2的大小,K1
②下列各项能作为判断该反应达到化学平衡状态的依据是
A.容器内N2、H2、NH3的物质的量浓度之比为1∶3∶2 B.v(N2)正=3v(H2)逆
C.容器内压强保持不变 D.混合气体的密度保持不变
③400℃时,反应2NH3(g)
 N2(g)+3H2(g)的化学平衡常数为
N2(g)+3H2(g)的化学平衡常数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】某同学对可逆反应2NO2(g)⇌N2O4(g)平衡体系进行探究。回答下列问题:
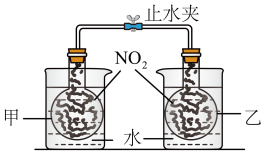
(1)向左侧烧杯中加入NH4NO3晶体,观察甲瓶红棕色变浅,向右侧烧杯中加入CaO固体,乙瓶的红棕色变深。则该反应2NO2(g)⇌N2O4(g) ΔH_____ 0(填“>”“=”或“<”)。
(2)关闭止水夹,维持温度不变,用注射器向甲瓶中充入一定量NO2,则此时反应2NO2(g)⇌N2O4(g)浓度熵Q______ K(填“>”、“=”或“<”),平衡将_______ (填“正向”“逆向”或“不”)移动,颜色比原来______ (填“深”“浅”或“不变”),再次达平衡时,NO2的转化率将______ (填“增大”“减小”或“不变”)。
(3)查阅资料可知,F. Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应:
Ⅰ.2N2O5(g)→4NO2(g)+O2(g) [t=∞时,N2O5(g)完全分解]
Ⅱ.2NO2(g)⇌N2O4(g)
反应体系的总压强p随时间t的变化如图所示:

①研究表明,N2O5(g)分解的反应速率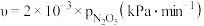 。则此时v(N2O5)=
。则此时v(N2O5)=________ kPa·min−1。
②若提高反应温度至35℃,则N2O5(g)完全分解后体系压强p∞(35℃)____ 65.8 kPa (填“大于”“等于”或“小于”),原因是_________ 。
③25℃时N2O4(g)⇌2NO2(g)反应的平衡常数Kp=_______ kPa(Kp为以分压表示的平衡常数,计算结果保留1位小数)。

(1)向左侧烧杯中加入NH4NO3晶体,观察甲瓶红棕色变浅,向右侧烧杯中加入CaO固体,乙瓶的红棕色变深。则该反应2NO2(g)⇌N2O4(g) ΔH
(2)关闭止水夹,维持温度不变,用注射器向甲瓶中充入一定量NO2,则此时反应2NO2(g)⇌N2O4(g)浓度熵Q
(3)查阅资料可知,F. Daniels等曾利用测压法在刚性反应器中研究了25℃时N2O5(g)分解反应:
Ⅰ.2N2O5(g)→4NO2(g)+O2(g) [t=∞时,N2O5(g)完全分解]
Ⅱ.2NO2(g)⇌N2O4(g)
反应体系的总压强p随时间t的变化如图所示:

①研究表明,N2O5(g)分解的反应速率
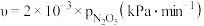 。则此时v(N2O5)=
。则此时v(N2O5)=②若提高反应温度至35℃,则N2O5(g)完全分解后体系压强p∞(35℃)
③25℃时N2O4(g)⇌2NO2(g)反应的平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氨是最重要的氮肥,是产量最大的化工产品之一.德国人哈伯在1905年发明了合成氨的方法,其合成原理为: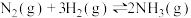
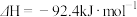 ,他因此获得了1918年诺贝尔化学奖.
,他因此获得了1918年诺贝尔化学奖.
在密闭容器中,使2mol 和6 mol
和6 mol  混合发生下列反应:
混合发生下列反应:
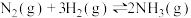 (正反应为放热反应)
(正反应为放热反应)
(1) 和
和 的转化率之比为
的转化率之比为______ .
(2)当达到平衡时,充入氩气,并保持体积不变,平衡将______ (填“正向”“逆向”或“不”)移动.
(3)恒温下,压缩容器体积,混合气体的平均相对分子质量______ ,密度______ .(填“变大”“变小”或“不变”)
(4)若容器恒容、绝热,降温使容器内温度迅速下降至原来的1/2,平衡将______ (填“向左程动”“向右移动”或“不移动”),达到新平衡后,容器内温度______ (填“大于”“小于”或“等于”)原来的1/2.
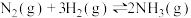
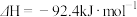 ,他因此获得了1918年诺贝尔化学奖.
,他因此获得了1918年诺贝尔化学奖.在密闭容器中,使2mol
 和6 mol
和6 mol  混合发生下列反应:
混合发生下列反应: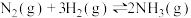 (正反应为放热反应)
(正反应为放热反应)(1)
 和
和 的转化率之比为
的转化率之比为(2)当达到平衡时,充入氩气,并保持体积不变,平衡将
(3)恒温下,压缩容器体积,混合气体的平均相对分子质量
(4)若容器恒容、绝热,降温使容器内温度迅速下降至原来的1/2,平衡将
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】乙炔可用于照明、焊接及切割金属,也是制备乙醛、苯、合成橡胶等的基本原料。甲烷催化裂解是工业上制备乙炔的方法之一、回答下列问题:
(1)已知:2H2(g)+O2(g)=2H2O(l) △H1= - 572 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H2= - 2600 kJ/mol
CH4(g)+2O2(g)=CO2(g)+ 2H2O(l) △H 3= - 885 kJ/mol
则2CH4(g)=C2H2(g)+3H2(g) △H=___________ kJ/mol。
(2)某科研小组利用固体催化工艺进行CH4裂解制备C2H2。
①用 和
和 分别表示 CH4、C2H2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程可表示如下:
分别表示 CH4、C2H2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程可表示如下:
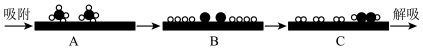
从“吸附”到“解吸”过程中,能量状态最高的是___________ 。 (填标号),理由是___________ 。
②在恒容密闭容器中充入a mol甲烷,测得单位时间内在固体催化剂表面CH4的转化率a(CH4)随温度t0℃/C的关系如图甲所示,t0℃后a(CH4)急剧下降的原因可能是___________ 。

(3)甲烷分解体系中几种气体的平衡分压(p/Pa)与温度(t/℃)的关系如图乙所示。
①在某温度下,向V L恒容密闭容器中充入0.12 mol CH4,若只发生反应:2CH4(g) C2H4(g)+2H2(g),达到平衡时,测得p(H2)=p(CH4),则CH4的平衡转化率为
C2H4(g)+2H2(g),达到平衡时,测得p(H2)=p(CH4),则CH4的平衡转化率为___________ (结果保留两位有效数字)。
②T℃时,反应2CH4(g) C2H2(g)+ 3H2(g)的压强平衡常数Kp=
C2H2(g)+ 3H2(g)的压强平衡常数Kp=___________ Pa2。
(1)已知:2H2(g)+O2(g)=2H2O(l) △H1= - 572 kJ/mol
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H2= - 2600 kJ/mol
CH4(g)+2O2(g)=CO2(g)+ 2H2O(l) △H 3= - 885 kJ/mol
则2CH4(g)=C2H2(g)+3H2(g) △H=
(2)某科研小组利用固体催化工艺进行CH4裂解制备C2H2。
①用
 和
和 分别表示 CH4、C2H2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程可表示如下:
分别表示 CH4、C2H2、H2和固体催化剂,在固体催化剂表面CH4的裂解过程可表示如下:
从“吸附”到“解吸”过程中,能量状态最高的是
②在恒容密闭容器中充入a mol甲烷,测得单位时间内在固体催化剂表面CH4的转化率a(CH4)随温度t0℃/C的关系如图甲所示,t0℃后a(CH4)急剧下降的原因可能是

(3)甲烷分解体系中几种气体的平衡分压(p/Pa)与温度(t/℃)的关系如图乙所示。
①在某温度下,向V L恒容密闭容器中充入0.12 mol CH4,若只发生反应:2CH4(g)
 C2H4(g)+2H2(g),达到平衡时,测得p(H2)=p(CH4),则CH4的平衡转化率为
C2H4(g)+2H2(g),达到平衡时,测得p(H2)=p(CH4),则CH4的平衡转化率为②T℃时,反应2CH4(g)
 C2H2(g)+ 3H2(g)的压强平衡常数Kp=
C2H2(g)+ 3H2(g)的压强平衡常数Kp=
您最近一年使用:0次



