回答下列问题:
(1)用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
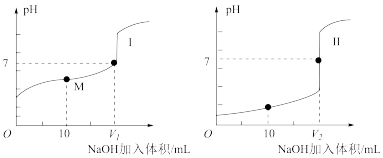
①滴定醋酸的曲线是__ (填“I”或“II”)。
②滴定开始前,三种溶液中由水电离出的c(H+)最大的是__ 。
③V1和V2的关系:V1__ V2(填“>”、“=”或“<”)。
④M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是__ 。
(2)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。
资料:AgSCN是白色沉淀。相同温度下,溶解度:AgSCN>AgI。
①写出步骤2中溶液变红色的离子方程式___ 。
②步骤3中现象a是__ 。
③用化学平衡原理解释步骤4的实验现象__ 。
(1)用0.1mol/LNaOH溶液分别滴定体积均为20.00mL、浓度均为0.1mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。

①滴定醋酸的曲线是
②滴定开始前,三种溶液中由水电离出的c(H+)最大的是
③V1和V2的关系:V1
④M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是
(2)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。
资料:AgSCN是白色沉淀。相同温度下,溶解度:AgSCN>AgI。
| 操作步骤 | 现象 |
| 步骤1:向2mL0.005mol•L-1AgNO3溶液中加入2mL0.005mol•L-1KSCN溶液,静置。 | 出现白色沉淀。 |
| 步骤2:取1mL上层清液于试管中,滴加1滴2mol•L-1Fe(NO3)3溶液。 | 溶液变红色。 |
| 步骤3:向步骤2的溶液中,继续加入5滴3mol•L-1AgNO3溶液。 | 现象a,溶液红色变浅。 |
| 步骤4:向步骤1余下的浊液中加入5滴3mol•L-1KI溶液。 | 浊液中出现黄色沉淀。 |
①写出步骤2中溶液变红色的离子方程式
②步骤3中现象a是
③用化学平衡原理解释步骤4的实验现象
更新时间:2021-12-14 22:40:18
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】运用相关原理,回答下列各小题:
I.已知:NaHSO4在水中的电离方程式为NaHSO4=Na++H++SO .
.
(1)常温下,pH=5的NaHSO4溶液中水的电离程度______________ (填“>”、”=”或“<”)pH=9的氨水中水的电离程度。
(2)等体积等物质的量浓度的NaHSO4与氨水混合后,溶液呈酸性的原因为:______________ (用离子方程式表示);若一定量的NaHSO4溶液与氨水混合后,溶液pH=7,则c(Na+)+c(NH )
)______________ c(SO )(填“>”、“=”或“<”);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO
)(填“>”、“=”或“<”);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO 完全沉淀,则反应后溶液的pH
完全沉淀,则反应后溶液的pH______________ 7(填“>”、”=”或“<”)。
(3)将分别含有MnO 、Fe3+、Fe2+、I- 的四种溶液混合,调节溶液的pH,使pH=1,充分反应后:若I- 离子有剩余,上述四种离子在溶液中还存在的有
、Fe3+、Fe2+、I- 的四种溶液混合,调节溶液的pH,使pH=1,充分反应后:若I- 离子有剩余,上述四种离子在溶液中还存在的有______________ ,一定不存在的是______________ 。
II.在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl−,利用Ag+与CrO42−生成砖红色沉淀,指示到达滴定终点。当溶液中Cl−恰好沉淀完全(浓度等于1.0×10−5 mol·L−1)时,溶液中c(Ag+)为________________ mol·L−1,此时溶液中c(CrO )等于
)等于______________ mol·L−1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10−12和2.0×10−10)。
I.已知:NaHSO4在水中的电离方程式为NaHSO4=Na++H++SO
 .
. (1)常温下,pH=5的NaHSO4溶液中水的电离程度
(2)等体积等物质的量浓度的NaHSO4与氨水混合后,溶液呈酸性的原因为:
 )
) )(填“>”、“=”或“<”);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO
)(填“>”、“=”或“<”);用硫酸氢钠与氢氧化钡溶液制取硫酸钡,若溶液中SO 完全沉淀,则反应后溶液的pH
完全沉淀,则反应后溶液的pH(3)将分别含有MnO
 、Fe3+、Fe2+、I- 的四种溶液混合,调节溶液的pH,使pH=1,充分反应后:若I- 离子有剩余,上述四种离子在溶液中还存在的有
、Fe3+、Fe2+、I- 的四种溶液混合,调节溶液的pH,使pH=1,充分反应后:若I- 离子有剩余,上述四种离子在溶液中还存在的有II.在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl−,利用Ag+与CrO42−生成砖红色沉淀,指示到达滴定终点。当溶液中Cl−恰好沉淀完全(浓度等于1.0×10−5 mol·L−1)时,溶液中c(Ag+)为
 )等于
)等于
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】I.常温下,根据表中的几种物质的电离平衡常数回答下列问题:
(1)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m________ (填“>”“<”或“=”)n。
(2)某温度下纯水的c(H+)=4.0×10-7mol/L,若温度不变,滴入稀盐酸,使c(H+)=2.0×10-4mol/L,则此溶液中由水电离产生的c(H+)=________ 。
(3)常温时,向0.1mol•L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液pH=________ 。
(4)已知NH3•H2O的Kb=1.8×10-5,H2CO3的Ka1=4×10-7,Ka2=4×10-11,则反应NH3•H2O+H2CO3 NH
NH +HCO
+HCO +H2O的平衡常数K=
+H2O的平衡常数K=________ 。
Ⅱ.某实验小组用已知浓度的NaOH溶液滴定未知浓度的盐酸。
(5)①量取待测盐酸20.00mL放入锥形瓶中,向其中滴加2滴酚酞溶液作指示剂。
②用0.1000mol•L-1的NaOH溶液滴定。
如何判断滴定终点________ 。
(6)实验记录如表。计算可得,待测盐酸浓度为________ mol/L。
(7)误差分析:滴定时,若加入待测盐酸前用待测盐酸润洗锥形瓶,将导致测定结果________ (填“偏大”、“偏小”或“不变”)。
(8)常温下,将pH=3的盐酸与pH=11的氨水等体积混合,混合后溶液的pH________ 7(用>、=、<表示)。
| 弱酸 | CH3COOH | NH3•H2O | H2CO3 |
| 电离平衡常数 | Ka=1.8×10-5 | Kb=1.8×10-5 | Ka1=4×10-7 Ka2=4×10-11 |
(1)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m
(2)某温度下纯水的c(H+)=4.0×10-7mol/L,若温度不变,滴入稀盐酸,使c(H+)=2.0×10-4mol/L,则此溶液中由水电离产生的c(H+)=
(3)常温时,向0.1mol•L-1CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液pH=
(4)已知NH3•H2O的Kb=1.8×10-5,H2CO3的Ka1=4×10-7,Ka2=4×10-11,则反应NH3•H2O+H2CO3
 NH
NH +HCO
+HCO +H2O的平衡常数K=
+H2O的平衡常数K=Ⅱ.某实验小组用已知浓度的NaOH溶液滴定未知浓度的盐酸。
(5)①量取待测盐酸20.00mL放入锥形瓶中,向其中滴加2滴酚酞溶液作指示剂。
②用0.1000mol•L-1的NaOH溶液滴定。
如何判断滴定终点
(6)实验记录如表。计算可得,待测盐酸浓度为
| 滴定次数 | 滴定管中液面初始读数/mL | 滴定终点液面读数/mL |
| 1 | 0.00 | 15.04 |
| 2 | 1.20 | 16.26 |
| 3 | 0.02 | 15.10 |
(7)误差分析:滴定时,若加入待测盐酸前用待测盐酸润洗锥形瓶,将导致测定结果
(8)常温下,将pH=3的盐酸与pH=11的氨水等体积混合,混合后溶液的pH
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】溶液中的化学反应大多是离子反应。根据要求回答下列问题:
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,试用化学方程式表示:
盐碱地产生碱性的原因:__________________________________________ ;
(2)已知水存在如下平衡:H2O+H2O H3O++OH-,向水中加入NaHSO4固体,水的电离平衡向
H3O++OH-,向水中加入NaHSO4固体,水的电离平衡向________ 移动,且所得溶液显________ 性。
(3)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m________ (填“>”“<”或“=”)n。
(4)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=________ 。
(5)已知:常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5;则 NH4HCO3溶液呈________ 性,NH4HCO3溶液中物质的量浓度最大的离子是________ (填化学式)。
(1)盐碱地(含较多Na2CO3、NaCl)不利于植物生长,试用化学方程式表示:
盐碱地产生碱性的原因:
(2)已知水存在如下平衡:H2O+H2O
 H3O++OH-,向水中加入NaHSO4固体,水的电离平衡向
H3O++OH-,向水中加入NaHSO4固体,水的电离平衡向(3)若取pH、体积均相等的NaOH溶液和氨水分别用水稀释m倍、n倍,稀释后pH仍相等,则m
(4)常温下,在pH=6的CH3COOH与CH3COONa的混合溶液中水电离出来的c(OH-)=
(5)已知:常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5;则 NH4HCO3溶液呈
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】酸碱中和实验是化学研究中重要的定量实验。
Ⅰ.25℃时,在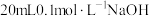 溶液中逐滴加入
溶液中逐滴加入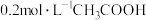 溶液,pH的变化曲线如图所示:
溶液,pH的变化曲线如图所示:
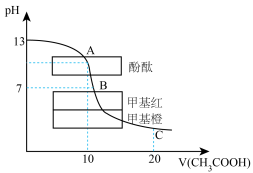
(1)A点溶液中离子浓度由大到小的顺序为___________ [用“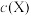 ”表示x的浓度,用“>”连接]。
”表示x的浓度,用“>”连接]。
(2)A→B过程中(不含A点,含B点),下列离子浓度大小关系可能出现的是___________。
(3)图中所示的三种指示剂,误差最大的是___________ 。
(4)滴定过程中水的电离情况如图所示:
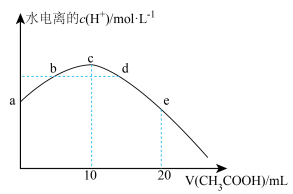
①a点水电离的
___________  。
。
②b点和d点对应的溶液中,pH=7的点是___________ (填“b”或“d”)。
Ⅱ. 的盐酸与
的盐酸与 的NaOH溶液在图所示的装置中进行中和反应,通过测定反应过程中放出的热量可计算中和反应反应热,回答相关问题。
的NaOH溶液在图所示的装置中进行中和反应,通过测定反应过程中放出的热量可计算中和反应反应热,回答相关问题。
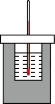
(5)从实验装置上看,图中尚缺少的一种玻璃仪器是___________ 。
(6)若实验过程中,图中内筒未加杯盖,求得的中和反应反应热数值___________ (填“偏大”、“偏小”或“无影响”)。
(7)为了计算中和反应反应热,某学生的实验记录数据如下:
依据上表数据,计算该实验中生成 时放出的热量为
时放出的热量为___________ kJ(结果保留一位小数)。(盐酸和氢氧化钠溶液的密度设为 ,中和反应后生成的溶液的比热容
,中和反应后生成的溶液的比热容 ,忽略量热计的比热容。)
,忽略量热计的比热容。)
Ⅰ.25℃时,在
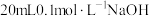 溶液中逐滴加入
溶液中逐滴加入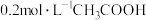 溶液,pH的变化曲线如图所示:
溶液,pH的变化曲线如图所示:
(1)A点溶液中离子浓度由大到小的顺序为
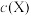 ”表示x的浓度,用“>”连接]。
”表示x的浓度,用“>”连接]。(2)A→B过程中(不含A点,含B点),下列离子浓度大小关系可能出现的是___________。
A.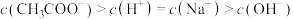 |
B. |
C.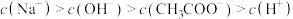 |
D. |
(3)图中所示的三种指示剂,误差最大的是
(4)滴定过程中水的电离情况如图所示:

①a点水电离的

 。
。②b点和d点对应的溶液中,pH=7的点是
Ⅱ.
 的盐酸与
的盐酸与 的NaOH溶液在图所示的装置中进行中和反应,通过测定反应过程中放出的热量可计算中和反应反应热,回答相关问题。
的NaOH溶液在图所示的装置中进行中和反应,通过测定反应过程中放出的热量可计算中和反应反应热,回答相关问题。
(5)从实验装置上看,图中尚缺少的一种玻璃仪器是
(6)若实验过程中,图中内筒未加杯盖,求得的中和反应反应热数值
(7)为了计算中和反应反应热,某学生的实验记录数据如下:
| 实验序号 | 反应物的温度/℃ | 反应前体系的温度 /℃ /℃ | 反应后体系的温度 /℃ /℃ | |
| 盐酸 | 氢氧化钠溶液 | |||
| 1 | 20.0 | 20.1 | 20.05 | 23.2 |
| 2 | 20.2 | 20.4 | 20.3 | 23.4 |
| 3 | 20.3 | 20.3 | 20.3 | 24.2 |
| 4 | 20.5 | 20.6 | 20.55 | 23.6 |
 时放出的热量为
时放出的热量为 ,中和反应后生成的溶液的比热容
,中和反应后生成的溶液的比热容 ,忽略量热计的比热容。)
,忽略量热计的比热容。)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】已知部分弱酸的电离平衡常数如表,根据表中数据回答下列问题。
(1)已知某浓度的 水溶液
水溶液 ,原因是
,原因是_______ (用离子方程式表示), 的
的 溶液中,由水电离出的
溶液中,由水电离出的 浓度为
浓度为_______ 。
(2)同浓度 这4种溶液中碱性由强到弱的顺序是
这4种溶液中碱性由强到弱的顺序是_______ ; 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是_______ 。
(3)体积相同、 相同的三种酸溶液a.
相同的三种酸溶液a. ;b.
;b. ;c.
;c. 分别与同浓度的
分别与同浓度的 溶液完全中和,消耗
溶液完全中和,消耗 溶液的体积由大到小的排列顺序是(填字母)
溶液的体积由大到小的排列顺序是(填字母)_______ 。
| 弱酸 |  |  |  |
电离平衡常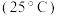 | 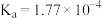 |  | 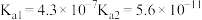 |
 水溶液
水溶液 ,原因是
,原因是 的
的 溶液中,由水电离出的
溶液中,由水电离出的 浓度为
浓度为(2)同浓度
 这4种溶液中碱性由强到弱的顺序是
这4种溶液中碱性由强到弱的顺序是 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是(3)体积相同、
 相同的三种酸溶液a.
相同的三种酸溶液a. ;b.
;b. ;c.
;c. 分别与同浓度的
分别与同浓度的 溶液完全中和,消耗
溶液完全中和,消耗 溶液的体积由大到小的排列顺序是(填字母)
溶液的体积由大到小的排列顺序是(填字母)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】Ⅰ.在0.1 mol/L的重铬酸钾(K2Cr2O7)溶液中存在如下平衡: +H2O
+H2O
 +2H+
+2H+
(1)在强碱溶液中,+6价铬元素的主要存在形式为___________ (填离子符号),向重铬酸钾溶液中加入适量稀硫酸,溶液中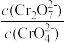 将
将___________ (填“增大”“减小”或“不变”)。
Ⅱ.已知某溶液中只存在OH-、H+、 、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
①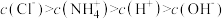 ②
②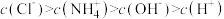
③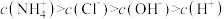 ④
④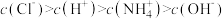
(2)若溶液中只溶解了一种溶质,则该溶质是___________ ,上述四种离子浓度的大小顺序为___________ (选填序号)。
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)___________ (填“大于”“小于”或“等于”)c(NH3·H2O)。
Ⅲ.重金属离子对河流、海洋造成严重污染。某化工厂废水(pH=2.0)中含有Ag+、Pb2+等重金属离子其浓度各约为0.01 mol/L。排放前拟用沉淀法除去这两种离子,查找有关数据如下(常温):
(4)你认为往废水中投入___________ (填字母序号),沉淀效果最好。
A.NaOH B.Na2S C.KI D.Ca(OH)2
(5)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=___________ 。
 +H2O
+H2O
 +2H+
+2H+(1)在强碱溶液中,+6价铬元素的主要存在形式为
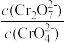 将
将Ⅱ.已知某溶液中只存在OH-、H+、
 、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:①
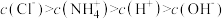 ②
②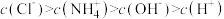
③
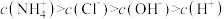 ④
④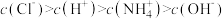
(2)若溶液中只溶解了一种溶质,则该溶质是
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)
Ⅲ.重金属离子对河流、海洋造成严重污染。某化工厂废水(pH=2.0)中含有Ag+、Pb2+等重金属离子其浓度各约为0.01 mol/L。排放前拟用沉淀法除去这两种离子,查找有关数据如下(常温):
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 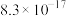 |  | 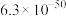 | 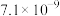 | 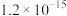 | 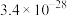 |
(4)你认为往废水中投入
A.NaOH B.Na2S C.KI D.Ca(OH)2
(5)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=
您最近一年使用:0次
【推荐1】高铁酸钾是一种高效的多功能水处理剂,具有强氧化性。制备高铁酸钾方法很多。
(1)干法制备高铁酸钾。将Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物。此制备反应中,氧化剂与还原剂的物质的量之比为_____________________ 。
(2)湿法制备高铁酸钾。工业上常采用NaClO氧化法生产,原理如下:
a.3NaClO+2Fe(NO3)3+ 10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O
b.Na2FeO4+2KOH =K2FeO4+2NaOH
主要的生产流程如图:

①流程图中“转化”是在某低温下进行的,说明此温度下的溶解度S(K2FeO4)_____ S(Na2FeO4)(填“>”“<”或“=”)。
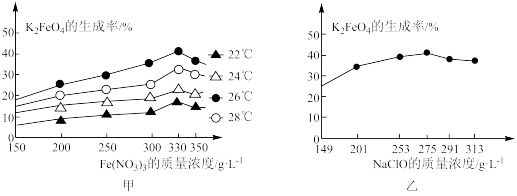
②湿法制备中,反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。如图,图甲为不同的温度下,不同质量浓度的Fe(NO3)3对K2FeO4生成率的影响;图乙为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4生成率的影响。工业生产中最佳温度为_________ ℃,此时Fe(NO3)3与NaClO 两种溶液最佳质量浓度之比为______________ 。
③若NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:_____________________ 。若Fe( NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式为__________________________________ 。
(3)K2FeO4在水溶液中易水解:4FeO42-+10H2O 4Fe(OH)3+8OH-+3O2↑。
4Fe(OH)3+8OH-+3O2↑。
①在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用__________ 溶液(填序号)。
A.H2O B.CH3COOK、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
②K2FeO4在处理水的过程中所起的作用有_______________________ 。
(4)室温下,向含有Fe3+的CuSO4溶液中加入Cu(OH)2可使Fe3+转化为Fe(O H)3沉淀,从而除去Fe3+。该反应的平衡常数为_____________________ 。(已知常温下的溶度积常数:Ksp[Cu(OH)2]=2.0×10-20, Ksp[Fe(OH)3]=4.0×10-38)。
(1)干法制备高铁酸钾。将Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物。此制备反应中,氧化剂与还原剂的物质的量之比为
(2)湿法制备高铁酸钾。工业上常采用NaClO氧化法生产,原理如下:
a.3NaClO+2Fe(NO3)3+ 10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O
b.Na2FeO4+2KOH =K2FeO4+2NaOH
主要的生产流程如图:

①流程图中“转化”是在某低温下进行的,说明此温度下的溶解度S(K2FeO4)
②湿法制备中,反应的温度、原料的浓度和配比对高铁酸钾的产率都有影响。如图,图甲为不同的温度下,不同质量浓度的Fe(NO3)3对K2FeO4生成率的影响;图乙为一定温度下,Fe(NO3)3质量浓度最佳时,NaClO浓度对K2FeO4生成率的影响。工业生产中最佳温度为

③若NaClO加入过量,氧化过程中会生成Fe(OH)3,写出该反应的离子方程式:
(3)K2FeO4在水溶液中易水解:4FeO42-+10H2O
 4Fe(OH)3+8OH-+3O2↑。
4Fe(OH)3+8OH-+3O2↑。①在“提纯”K2FeO4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
A.H2O B.CH3COOK、异丙醇 C.NH4Cl、异丙醇 D.Fe(NO3)3、异丙醇
②K2FeO4在处理水的过程中所起的作用有
(4)室温下,向含有Fe3+的CuSO4溶液中加入Cu(OH)2可使Fe3+转化为Fe(O H)3沉淀,从而除去Fe3+。该反应的平衡常数为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】工业废水随意排放会造成严重污染,根据成分不同可采用不同的处理方法。
(1)电池生产工业废水中常含有Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去。已知室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2。
①请用离子方程式说明上述除杂的原理______________________ 。
②FeS高温煅烧产生的SO2气体通入下列溶液中,能够产生沉淀的是_________ (填序号)
A.Ba(NO3)2 B.BaCl2
C.Ba(OH)2 D.溶有NH3的BaCl2溶液
③已知元素在高价态时常表现氧化性,若在酸性CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀,则生成CuCl的离子方程式是___________ 。
(2)电解法处理酸性含铬废水(主要含有Cr2O72-)时,在废水中加入适量NaCl,以铁板作阴、阳极,处理过程中存在如下反应Cr2O72+6Fe2++14H+═2Cr3++6Fe3++7H2O,最后Cr3+ 以Cr(OH)3形式除去,下列说法不正确的是______ (填序号)
A.阳极反应为Fe-2e-═Fe2+
B.电解过程中溶液pH减小
C.过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有2mol Cr2O72-被还原
(3)废氨水可以转化成氨,氨再设计成碱性燃料电池。右图是该燃料电池示意图,产生的X气体可直接排放到大气中,a电极作_________ 极(填“正”“负”“阴”或“阳”),其电极反应式为___________ 。

(1)电池生产工业废水中常含有Cu2+等重金属离子,常用FeS等难溶物质作为沉淀剂除去。已知室温下Ksp(FeS)=6.3×10-18mol2·L-2,Ksp(CuS)=1.3×10-36mol2·L-2。
①请用离子方程式说明上述除杂的原理
②FeS高温煅烧产生的SO2气体通入下列溶液中,能够产生沉淀的是
A.Ba(NO3)2 B.BaCl2
C.Ba(OH)2 D.溶有NH3的BaCl2溶液
③已知元素在高价态时常表现氧化性,若在酸性CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀,则生成CuCl的离子方程式是
(2)电解法处理酸性含铬废水(主要含有Cr2O72-)时,在废水中加入适量NaCl,以铁板作阴、阳极,处理过程中存在如下反应Cr2O72+6Fe2++14H+═2Cr3++6Fe3++7H2O,最后Cr3+ 以Cr(OH)3形式除去,下列说法不正确的是
A.阳极反应为Fe-2e-═Fe2+
B.电解过程中溶液pH减小
C.过程中有Fe(OH)3沉淀生成
D.电路中每转移12 mol电子,最多有2mol Cr2O72-被还原
(3)废氨水可以转化成氨,氨再设计成碱性燃料电池。右图是该燃料电池示意图,产生的X气体可直接排放到大气中,a电极作

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】2030年全球新能源动力电池镍消费量将达到2020年全球镍产量的近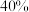 。工业上由某含镍废渣精矿(主要成分为
。工业上由某含镍废渣精矿(主要成分为 ,还有
,还有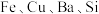 的氧化物)为原料制备碱式碳酸镍
的氧化物)为原料制备碱式碳酸镍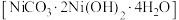 的流程如图1所示。
的流程如图1所示。

已知: 时,
时,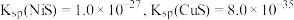
回答下列问题:
(1)滤渣I的主要成分为___________ (填化学式)。“除杂1”时,加入的 的作用是
的作用是___________ (用离子方程式表示)。
(2)“除杂2”时发生反应的离子方程式为 ,从平衡常数角度分析选择
,从平衡常数角度分析选择 的原因
的原因___________ ;实验测得此工序中加入 的物质的量与“除杂1”所得溶液
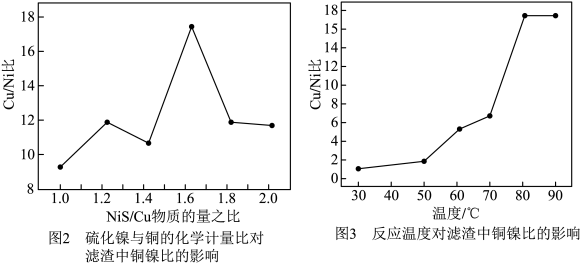
的物质的量与“除杂1”所得溶液 的物质的量之比、反应温度对“除杂2”所得滤渣中铜镍比的关系分别如图2和图3所示。则最佳的加入
的物质的量之比、反应温度对“除杂2”所得滤渣中铜镍比的关系分别如图2和图3所示。则最佳的加入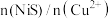 之比和反应温度分别为
之比和反应温度分别为___________ 。
(3)“萃取”过程表示为下式: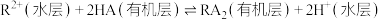 。则“反萃取”所加试剂X为
。则“反萃取”所加试剂X为___________ (填化学式)。
(4)“沉镍”时无气体产生,则该过程反应的离子方程式为___________ 。
(5)将一定量的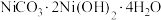 在空气中煅烧得到镍的某种氧化物Q为
在空气中煅烧得到镍的某种氧化物Q为 ,同时生成标况下
,同时生成标况下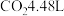 ,则Q的化学式为
,则Q的化学式为___________ 。
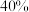 。工业上由某含镍废渣精矿(主要成分为
。工业上由某含镍废渣精矿(主要成分为 ,还有
,还有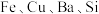 的氧化物)为原料制备碱式碳酸镍
的氧化物)为原料制备碱式碳酸镍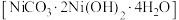 的流程如图1所示。
的流程如图1所示。
已知:
 时,
时,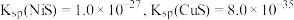
回答下列问题:
(1)滤渣I的主要成分为
 的作用是
的作用是(2)“除杂2”时发生反应的离子方程式为
 ,从平衡常数角度分析选择
,从平衡常数角度分析选择 的原因
的原因 的物质的量与“除杂1”所得溶液
的物质的量与“除杂1”所得溶液 的物质的量之比、反应温度对“除杂2”所得滤渣中铜镍比的关系分别如图2和图3所示。则最佳的加入
的物质的量之比、反应温度对“除杂2”所得滤渣中铜镍比的关系分别如图2和图3所示。则最佳的加入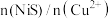 之比和反应温度分别为
之比和反应温度分别为
(3)“萃取”过程表示为下式:
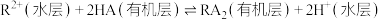 。则“反萃取”所加试剂X为
。则“反萃取”所加试剂X为(4)“沉镍”时无气体产生,则该过程反应的离子方程式为
(5)将一定量的
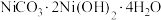 在空气中煅烧得到镍的某种氧化物Q为
在空气中煅烧得到镍的某种氧化物Q为 ,同时生成标况下
,同时生成标况下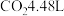 ,则Q的化学式为
,则Q的化学式为
您最近一年使用:0次



