已知部分弱酸的电离平衡常数如表,根据表中数据回答下列问题。
(1)已知某浓度的 水溶液
水溶液 ,原因是
,原因是_______ (用离子方程式表示), 的
的 溶液中,由水电离出的
溶液中,由水电离出的 浓度为
浓度为_______ 。
(2)同浓度 这4种溶液中碱性由强到弱的顺序是
这4种溶液中碱性由强到弱的顺序是_______ ; 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是_______ 。
(3)体积相同、 相同的三种酸溶液a.
相同的三种酸溶液a. ;b.
;b. ;c.
;c. 分别与同浓度的
分别与同浓度的 溶液完全中和,消耗
溶液完全中和,消耗 溶液的体积由大到小的排列顺序是(填字母)
溶液的体积由大到小的排列顺序是(填字母)_______ 。
| 弱酸 |  |  |  |
电离平衡常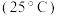 | 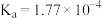 |  | 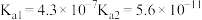 |
 水溶液
水溶液 ,原因是
,原因是 的
的 溶液中,由水电离出的
溶液中,由水电离出的 浓度为
浓度为(2)同浓度
 这4种溶液中碱性由强到弱的顺序是
这4种溶液中碱性由强到弱的顺序是 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是(3)体积相同、
 相同的三种酸溶液a.
相同的三种酸溶液a. ;b.
;b. ;c.
;c. 分别与同浓度的
分别与同浓度的 溶液完全中和,消耗
溶液完全中和,消耗 溶液的体积由大到小的排列顺序是(填字母)
溶液的体积由大到小的排列顺序是(填字母)
更新时间:2022-04-04 09:12:44
|
相似题推荐
【推荐1】回答下列问题:
(1)室温下,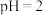 的
的 溶液、
溶液、 的
的 溶液、
溶液、 的
的 溶液,水电离出的
溶液,水电离出的 之比为
之比为_______ 。
(2)含有 的废水毒性较大,某工厂酸性废水中含
的废水毒性较大,某工厂酸性废水中含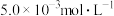 的
的 ,可先向废水中加入绿矾
,可先向废水中加入绿矾 ,搅拌后撒入生石灰处理.
,搅拌后撒入生石灰处理.
①写出加入绿矾的离子方程式_______ 。
②若处理后的废水中残留的 ,则残留的
,则残留的 的浓度为
的浓度为_______  (已知:
(已知: ,
, )
)
(3)已知反应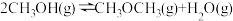 在某温度下的平衡常数为400.此温度下,在密闭容器中加入
在某温度下的平衡常数为400.此温度下,在密闭容器中加入 ,反应到某时刻测得各组分的浓度如下:
,反应到某时刻测得各组分的浓度如下:
①比较此时正、逆反应速率的大小:v(正)_______ v(逆)(填“>”“<”或“=”)。
②若加入 后,经
后,经 反应达到平衡,此时
反应达到平衡,此时 的转化率
的转化率_______ 。
(1)室温下,
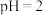 的
的 溶液、
溶液、 的
的 溶液、
溶液、 的
的 溶液,水电离出的
溶液,水电离出的 之比为
之比为(2)含有
 的废水毒性较大,某工厂酸性废水中含
的废水毒性较大,某工厂酸性废水中含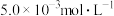 的
的 ,可先向废水中加入绿矾
,可先向废水中加入绿矾 ,搅拌后撒入生石灰处理.
,搅拌后撒入生石灰处理.①写出加入绿矾的离子方程式
②若处理后的废水中残留的
 ,则残留的
,则残留的 的浓度为
的浓度为 (已知:
(已知: ,
, )
)(3)已知反应
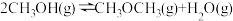 在某温度下的平衡常数为400.此温度下,在密闭容器中加入
在某温度下的平衡常数为400.此温度下,在密闭容器中加入 ,反应到某时刻测得各组分的浓度如下:
,反应到某时刻测得各组分的浓度如下:| 物质 |  |  |  |
浓度 | 0.44 | 0.6 | 0.6 |
②若加入
 后,经
后,经 反应达到平衡,此时
反应达到平衡,此时 的转化率
的转化率
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐2】烟气中的SO2可以用钠碱循环法加以处理,用Na2SO3溶液作为吸收液,当吸收液与SO2反应至pH为6左右时,可将吸收液通入电解槽进行再生,吸收液pH随微粒组成的变化关系见表:
| 91:9 | 1:1 | 9:91 |
pH | 8.2 | 7.2 | 6.2 |
回答下列问题:
(1)吸收液pH由8.2下降至6.2过程中发生反应的离子方程式为
(2)当吸收液呈中性时,溶液中

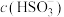 (填“>”“<”或“=”,下同);pH=7.2时,
(填“>”“<”或“=”,下同);pH=7.2时,
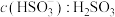 第二步电离平衡常数
第二步电离平衡常数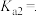
(3)NaHSO3﹣Na2SO3、H2CO3﹣NaHCO3,Na2HPO4﹣NaH2PO4都可组成缓冲溶液,缓冲溶液中lgx[x表示
 或
或 ]与pH的关系如图,当lgx数值在﹣1~1之间时具有可实用价值的缓冲能力,曲线
]与pH的关系如图,当lgx数值在﹣1~1之间时具有可实用价值的缓冲能力,曲线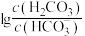 与pH的变化关系,应控制Na2HPO4﹣NaH2PO4缓冲溶液的pH范围为
与pH的变化关系,应控制Na2HPO4﹣NaH2PO4缓冲溶液的pH范围为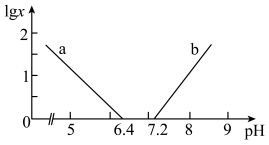
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验:将pH=2的两种酸溶液HA、HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:
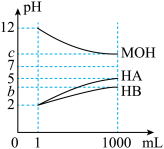
(1)HA为___ 酸,HB为___ 酸(填“强”或“弱”)。
(2)若c=9,则将pH=2的HB与pH=12的MOH等体积混合后,溶液呈__ (填“酸”“碱”或“中”)性。
(3)若c=9,稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为__ (用酸、碱化学式表示)。
(4)常温下,取pH=2的HA、HB各100mL,向其中分别加入适量的Zn粒,反应后两溶液的pH均变为4,设HA中加入的Zn质量为m1,HB中加入的Zn质量为m2,则m1__ m2(选填“<”、“=”或“>”)。
(5)若b+c=14,则MOH为___ 碱(选填“强”或“弱”)。将稀释后的HB溶液和MOH溶液取等体积混合,所得混合溶液的pH__ 7(选填“大于”、“小于”或“等于”)。

(1)HA为
(2)若c=9,则将pH=2的HB与pH=12的MOH等体积混合后,溶液呈
(3)若c=9,稀释后的三种溶液中,由水电离的氢离子浓度的大小顺序为
(4)常温下,取pH=2的HA、HB各100mL,向其中分别加入适量的Zn粒,反应后两溶液的pH均变为4,设HA中加入的Zn质量为m1,HB中加入的Zn质量为m2,则m1
(5)若b+c=14,则MOH为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】电解质的水溶液中存在电离平衡。
(1)醋酸是常见的弱酸。
①醋酸在水溶液中的电离方程式为___________ 。
②下列方法中,可以使醋酸稀溶液中 电离程度减小的是
电离程度减小的是___________ (填字母序号)。
a.滴加浓盐酸 b.微热溶液 c.加水稀释 d.加入醋酸钠晶体 e.加入冰醋酸
(2)用 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液
的盐酸和醋酸溶液,得到滴定过程中溶液 随加入
随加入 溶液体积而变化的两条滴定曲线。
溶液体积而变化的两条滴定曲线。
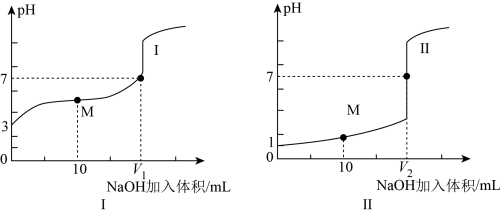
①滴定开始前,三种溶液中由水电离出的 最大的是
最大的是___________ 。
②已知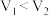 ,则滴定醋酸的曲线是
,则滴定醋酸的曲线是___________ (填“I”或“II”)。
(3)酸碱中和滴定可用于测定酸或碱的物质的量浓度,取 未知浓度的盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用
未知浓度的盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用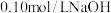 标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
①滴定达到终点的标志是___________ 。
②根据上述数据,可计算出该盐酸的浓度约为___________  (保留两位有效数字)。
(保留两位有效数字)。
③在上述实验中,下列操作会造成测定结果偏高的有___________ 。(填字母序号)。
A.滴定终点读数时俯视
B.锥形瓶水洗后未干燥
C.酸式滴定管使用前,水洗后未用待测盐酸润洗
D.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(1)醋酸是常见的弱酸。
①醋酸在水溶液中的电离方程式为
②下列方法中,可以使醋酸稀溶液中
 电离程度减小的是
电离程度减小的是a.滴加浓盐酸 b.微热溶液 c.加水稀释 d.加入醋酸钠晶体 e.加入冰醋酸
(2)用
 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液
的盐酸和醋酸溶液,得到滴定过程中溶液 随加入
随加入 溶液体积而变化的两条滴定曲线。
溶液体积而变化的两条滴定曲线。
①滴定开始前,三种溶液中由水电离出的
 最大的是
最大的是②已知
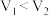 ,则滴定醋酸的曲线是
,则滴定醋酸的曲线是(3)酸碱中和滴定可用于测定酸或碱的物质的量浓度,取
 未知浓度的盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用
未知浓度的盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用 标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。| 实验编号 | NaOH溶液的浓度(mo1·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸的体积(mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 25.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
②根据上述数据,可计算出该盐酸的浓度约为
 (保留两位有效数字)。
(保留两位有效数字)。③在上述实验中,下列操作会造成测定结果偏高的有
A.滴定终点读数时俯视
B.锥形瓶水洗后未干燥
C.酸式滴定管使用前,水洗后未用待测盐酸润洗
D.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗
E.碱式滴定管尖嘴部分有气泡,滴定后消失
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】图象分析是研究化学问题的重要手段。请分析以下图象,回答有关问题。
(1)理论分析在密闭容器中发生的反应:
 。不同时刻,保持其它条件不变,只改变某一个条件,正、逆反应速率随时间变化示意图如图所示。
。不同时刻,保持其它条件不变,只改变某一个条件,正、逆反应速率随时间变化示意图如图所示。

请在以下表格中填入各时刻改变的条件。
(2)密闭容器中,发生反应: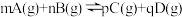
 。下图为C的体积分数
。下图为C的体积分数 在不同压强P下随时间t变化的曲线和A的转化率a(A)在不同压强下随温度T变化的曲线。
在不同压强P下随时间t变化的曲线和A的转化率a(A)在不同压强下随温度T变化的曲线。
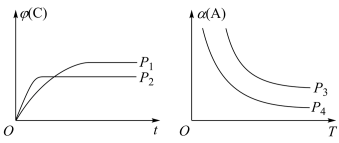
请回答下列问题(填“>”、“=”或“<”):
①m+n___________ p+q。
②
___________ 0。
③
___________  。
。
(3)常温下,相同pH的盐酸和醋酸分别加水稀释,溶液中氢离子浓度随溶液体积变化曲线如图所示。

①曲线II表示的是___________ 稀释的变化曲线。
②将a点溶液与b点溶液混合,醋酸的电离平衡 将向
将向___________ 移动。
③a、b、c三点的导电能力大小顺序为___________ 。
(4)1L的恒容密闭容器中放入2.0g碳酸钙,恒温条件下,发生反应: 。达到平衡时,
。达到平衡时, 。
。
①若达到平衡后,再通入0.008molCO2,达到新平衡时,CO2浓度随时间变化曲线应为图I中的____ (填字母)。

②若达到平衡后, 时刻将容器容积瞬间扩大至2L,请在图II中画出CO2浓度随时间变化曲线
时刻将容器容积瞬间扩大至2L,请在图II中画出CO2浓度随时间变化曲线__ 。
(1)理论分析在密闭容器中发生的反应:

 。不同时刻,保持其它条件不变,只改变某一个条件,正、逆反应速率随时间变化示意图如图所示。
。不同时刻,保持其它条件不变,只改变某一个条件,正、逆反应速率随时间变化示意图如图所示。
请在以下表格中填入各时刻改变的条件。
| 时刻 |  |  |  |  |  |  |
| 条件变化 | 使用催化剂 | 增加反应物 |
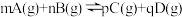
 。下图为C的体积分数
。下图为C的体积分数 在不同压强P下随时间t变化的曲线和A的转化率a(A)在不同压强下随温度T变化的曲线。
在不同压强P下随时间t变化的曲线和A的转化率a(A)在不同压强下随温度T变化的曲线。
请回答下列问题(填“>”、“=”或“<”):
①m+n
②

③

 。
。(3)常温下,相同pH的盐酸和醋酸分别加水稀释,溶液中氢离子浓度随溶液体积变化曲线如图所示。

①曲线II表示的是
②将a点溶液与b点溶液混合,醋酸的电离平衡
 将向
将向③a、b、c三点的导电能力大小顺序为
(4)1L的恒容密闭容器中放入2.0g碳酸钙,恒温条件下,发生反应:
 。达到平衡时,
。达到平衡时, 。
。①若达到平衡后,再通入0.008molCO2,达到新平衡时,CO2浓度随时间变化曲线应为图I中的

②若达到平衡后,
 时刻将容器容积瞬间扩大至2L,请在图II中画出CO2浓度随时间变化曲线
时刻将容器容积瞬间扩大至2L,请在图II中画出CO2浓度随时间变化曲线
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】某化学研究性学习小组通过分组实验来探究盐酸与醋酸电离程度的差异,探究过程如下表:

(1)若甲、乙两组同学用pH试纸测溶液的pH时,均先用蒸馏水润湿pH试纸后再分别测定盐酸、醋酸、醋酸钠、氯化钠4种溶液的pH值,这种操作会导致上述所测的三种溶液的pH值出现偏差,不会出现偏差的溶液是 :____________ ,测得溶液pH>7的有:_____ 。
(2)丙组实验中的两种溶液反应后,收集到的气体体积________ (填“相等”或“不相等”)。
(3)以上3组实验中能证明醋酸是弱酸的是:_____ 及 丙 组(填“甲”、“乙”或“丙”,下同),能证明盐酸是强酸的是____ 组。

(1)若甲、乙两组同学用pH试纸测溶液的pH时,均先用蒸馏水润湿pH试纸后再分别测定盐酸、醋酸、醋酸钠、氯化钠4种溶液的pH值,这种操作会导致上述所测的三种溶液的pH值出现偏差,不会出现偏差的溶液是 :
(2)丙组实验中的两种溶液反应后,收集到的气体体积
(3)以上3组实验中能证明醋酸是弱酸的是:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】物质在水中可能存在电离平衡、水解平衡和沉淀溶解平衡,请根据所学知识回答:
I.常温下,一定浓度的 溶液的
溶液的 ,已知
,已知 的电离平衡常数
的电离平衡常数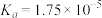 。
。
(1)乙酸钠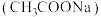 溶液呈碱性的原因是
溶液呈碱性的原因是_______ (用离子方程式表示)。 的
的 溶液中:
溶液中: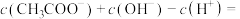
_______  。
。
Ⅱ.常温下向某氨水中缓缓通入 气体,溶液中
气体,溶液中 与
与 关系如图所示。
关系如图所示。

(2)在常温下 的电离平衡常数
的电离平衡常数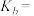
_______ (用含有a的代数式表示)。
Ⅲ. 时,向
时,向 溶液中滴加
溶液中滴加 溶液(一种酸,酸性强弱未知)时,溶液中由水电离的
溶液(一种酸,酸性强弱未知)时,溶液中由水电离的 浓度随加入的HA体积的变化如图所示:
浓度随加入的HA体积的变化如图所示:

(3)根据该图判断HA为_______ (填“强酸”或“弱酸”),理由是_______ 。
(4)若稀释a点溶液,则与稀释前相比,稀释后的溶液中水的电离程度会_______ (填“增大”、“减小”或“不变”)。
(5)d点溶液中溶质成分是_______ ,溶液中离子浓度大小关系_______ 。
I.常温下,一定浓度的
 溶液的
溶液的 ,已知
,已知 的电离平衡常数
的电离平衡常数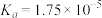 。
。(1)乙酸钠
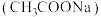 溶液呈碱性的原因是
溶液呈碱性的原因是 的
的 溶液中:
溶液中: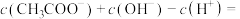
 。
。Ⅱ.常温下向某氨水中缓缓通入
 气体,溶液中
气体,溶液中 与
与 关系如图所示。
关系如图所示。
(2)在常温下
 的电离平衡常数
的电离平衡常数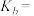
Ⅲ.
 时,向
时,向 溶液中滴加
溶液中滴加 溶液(一种酸,酸性强弱未知)时,溶液中由水电离的
溶液(一种酸,酸性强弱未知)时,溶液中由水电离的 浓度随加入的HA体积的变化如图所示:
浓度随加入的HA体积的变化如图所示:
(3)根据该图判断HA为
(4)若稀释a点溶液,则与稀释前相比,稀释后的溶液中水的电离程度会
(5)d点溶液中溶质成分是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】电解质水溶液广泛存在于生命体及其赖以生存的环境中,电离平衡、水解平衡和沉淀溶解平衡都与生活、生产等息息相关。回答下问题。
(1)室温,体积均为10mL且等pH的CH3COOH溶液与一元酸HX,分别加水稀释至100mL,溶液pH变化如图,则Ka(HX)______ Ka(CH3COOH) (填“>”、“<”或“=”)。溶液稀释后,HX溶液中水电离的c(H+)_____ CH3COOH溶液水电离的c(H+) (填“>”、“<”或“=”)。 _____ 0.01mol/L (填“>”、“<”或“=”)。
(3)在氨水和碳酸氢钠溶液中分别滴入酚酞,溶液均呈现红色,请用相关理论及离子程式解释其原因。______________ 。
(4)浓度均为0.5mol/L的Na2CO3溶液和NaHCO3溶液,以下关系式中,Na2CO3 溶液和NaHCO3溶液均满足的是______。
(5)在Na2CO3和NaHCO3的混合溶液中,一定可以大量共存的离子是______。
(6)等浓度的NH4Cl、(NH4)2CO3和NH4HCO3溶液中,c( )最大的溶液是
)最大的溶液是____ (填化学式)。
(7)含两种等物质的量的溶质的溶液,溶液中只存在OH-、H+、 、Cl-四种离子,且c(
、Cl-四种离子,且c( )>c(Cl-)>c(OH-)>c(H+),则这两种溶质分别是
)>c(Cl-)>c(OH-)>c(H+),则这两种溶质分别是________ 。
(8)我国饮用水卫生标准规定:生活用水中镉(Cd2+)的排放量不超过0.005mg/L。工业上处理含镉(Cd2+)废水常用化学沉淀法。常温下Ksp(Cd(OH)2)=3.2×10-14,若使用生石灰调节溶液pH值,以Cd(OH)2沉淀析出达到Cd2+可排放标准,则溶液pH值至少控制在_____ (保留小数点后一位) (已知:Cd相对原子质量为112.4)
(1)室温,体积均为10mL且等pH的CH3COOH溶液与一元酸HX,分别加水稀释至100mL,溶液pH变化如图,则Ka(HX)

(3)在氨水和碳酸氢钠溶液中分别滴入酚酞,溶液均呈现红色,请用相关理论及离子程式解释其原因。
(4)浓度均为0.5mol/L的Na2CO3溶液和NaHCO3溶液,以下关系式中,Na2CO3 溶液和NaHCO3溶液均满足的是______。
A.c(Na+)+c(H+)=2c( )+c( )+c( )+c(OH-) )+c(OH-) |
B.c( )+ 2c(H2CO3)+ c(H+)=c(OH-) )+ 2c(H2CO3)+ c(H+)=c(OH-) |
C.c( )+c( )+c( )+c(H2CO3)=0.5 mol/L )+c(H2CO3)=0.5 mol/L |
D.c(Na+)>c( )>c(OH-)> c( )>c(OH-)> c( )>c(H+) )>c(H+) |
(5)在Na2CO3和NaHCO3的混合溶液中,一定可以大量共存的离子是______。
| A.OH- | B. | C.H+ | D.Al3+ |
(6)等浓度的NH4Cl、(NH4)2CO3和NH4HCO3溶液中,c(
 )最大的溶液是
)最大的溶液是(7)含两种等物质的量的溶质的溶液,溶液中只存在OH-、H+、
 、Cl-四种离子,且c(
、Cl-四种离子,且c( )>c(Cl-)>c(OH-)>c(H+),则这两种溶质分别是
)>c(Cl-)>c(OH-)>c(H+),则这两种溶质分别是(8)我国饮用水卫生标准规定:生活用水中镉(Cd2+)的排放量不超过0.005mg/L。工业上处理含镉(Cd2+)废水常用化学沉淀法。常温下Ksp(Cd(OH)2)=3.2×10-14,若使用生石灰调节溶液pH值,以Cd(OH)2沉淀析出达到Cd2+可排放标准,则溶液pH值至少控制在
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】(NH4)2Fe(SO4)2俗称莫尔盐,其常见的制备工艺流程如下:

(1)已知流程中铁粉制备反应如下:
4 H2O(g) +3Fe(s) Fe3O4(s)十4H2(g) △H ="a" kJ /mol
Fe3O4(s)十4H2(g) △H ="a" kJ /mol
Fe3O4(s) =" 3" Fe(s)+ 2O2(g) △H ="b" kJ/mol
则光解气态水制备H2的热化学方程式为_____________ 。
(2)步骤I中加水发生如下反应,请完善该反应:____ +2H2O  2H++ H2TiO3 ↓;
2H++ H2TiO3 ↓;
该步骤加入铁粉的作用是①____________ ;②____________ 。
(3)步骤Ⅳ生成(NH4)2Fe(SO4)2,其化学反应方程式为_______________ ;
写出(NH4)2Fe(SO4)2溶液中各离子溶度由大到小的顺序:_______________
(4)已知在潮湿空气中Fe(OH)2比FeCl2更易被氧化。据此分析(NH4)2Fe(SO4)2比FeSO4稳定的原因是_______________________ 。
(5)室温时Fe(OH)3的悬浊液中存在Fe(OH)3(s) Fe3+(aq)+3OH-(aq) Ksp[Fe(OH)3] =8ⅹ10-32若此悬浊液中 c(Fe3+)="0.08" mol·L-1则溶液的pH等于
Fe3+(aq)+3OH-(aq) Ksp[Fe(OH)3] =8ⅹ10-32若此悬浊液中 c(Fe3+)="0.08" mol·L-1则溶液的pH等于___________________ 。

(1)已知流程中铁粉制备反应如下:
4 H2O(g) +3Fe(s)
 Fe3O4(s)十4H2(g) △H ="a" kJ /mol
Fe3O4(s)十4H2(g) △H ="a" kJ /molFe3O4(s) =" 3" Fe(s)+ 2O2(g) △H ="b" kJ/mol
则光解气态水制备H2的热化学方程式为
(2)步骤I中加水发生如下反应,请完善该反应:
 2H++ H2TiO3 ↓;
2H++ H2TiO3 ↓;该步骤加入铁粉的作用是①
(3)步骤Ⅳ生成(NH4)2Fe(SO4)2,其化学反应方程式为
写出(NH4)2Fe(SO4)2溶液中各离子溶度由大到小的顺序:
(4)已知在潮湿空气中Fe(OH)2比FeCl2更易被氧化。据此分析(NH4)2Fe(SO4)2比FeSO4稳定的原因是
(5)室温时Fe(OH)3的悬浊液中存在Fe(OH)3(s)
 Fe3+(aq)+3OH-(aq) Ksp[Fe(OH)3] =8ⅹ10-32若此悬浊液中 c(Fe3+)="0.08" mol·L-1则溶液的pH等于
Fe3+(aq)+3OH-(aq) Ksp[Fe(OH)3] =8ⅹ10-32若此悬浊液中 c(Fe3+)="0.08" mol·L-1则溶液的pH等于
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】碳酸锰是制取其他含锰化合物的原料,也可用作脱硫的催化剂等。一种焙烧氯化铵和菱锰矿粉制备高纯度碳酸锰的工艺流程如图所示
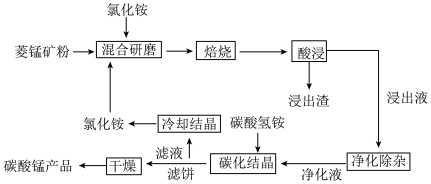
已知①菱锰矿粉的主要成分是MnCO3,还有少量的Fe、Al、Ca、Mg等元素
②常温下,相关金属离子在浓度为0.1mol/L时形成M(OH)n沉淀的pH范围如表
回答下列问题:
(1)“混合研磨”的作用为_______________________
(2)“焙烧”时发生的主要反应的化学方程式为_________________________________
(3)分析图1、图2,焙烧氯化铵、菱锰矿粉的最佳条件是_____________________________

(4)净化除杂流程如下
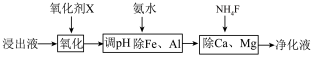
①已知几种物质氧化能力的强弱顺序为(NH4)2S2O8>KMnO4>MnO2>Fe3+,则氧化剂X宜选择__________
A.(NH4)2S2O8 B.MnO2 C.KMnO4
②调节pH时,pH可取的范围为_________________
(5)“碳化结晶”过程中不能用碳酸铵代替碳酸氢铵,可能的原因是__________________

已知①菱锰矿粉的主要成分是MnCO3,还有少量的Fe、Al、Ca、Mg等元素
②常温下,相关金属离子在浓度为0.1mol/L时形成M(OH)n沉淀的pH范围如表
| 金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ | Mn2+ | Mg2+ |
| 开始沉淀的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
| 沉淀完全的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
回答下列问题:
(1)“混合研磨”的作用为
(2)“焙烧”时发生的主要反应的化学方程式为
(3)分析图1、图2,焙烧氯化铵、菱锰矿粉的最佳条件是

(4)净化除杂流程如下

①已知几种物质氧化能力的强弱顺序为(NH4)2S2O8>KMnO4>MnO2>Fe3+,则氧化剂X宜选择
A.(NH4)2S2O8 B.MnO2 C.KMnO4
②调节pH时,pH可取的范围为
(5)“碳化结晶”过程中不能用碳酸铵代替碳酸氢铵,可能的原因是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐2】无水 具有抗菌、杀虫、抗氧化和除藻等功能,从电路板回收无水
具有抗菌、杀虫、抗氧化和除藻等功能,从电路板回收无水 的工艺如下:
的工艺如下:

已知:各离子开始沉淀和完全沉淀的pH如下表:
回答下列各题:
(1)用离子方程式表示 的作用
的作用______ ,物质x可调节溶液b的pH,最好选用______ (填正确答案的编号),加入x后调节溶液b的pH范围是______ 。
A.CuO B.NaOH C.氨水 D.
(2)废渣的主要成分的化学式是______ 。
(3)一系列操作是先蒸发浓缩,冷却结晶得到 。但冷却结晶时发现
。但冷却结晶时发现 溶液过饱和也不析出晶体。实验室模拟该过程通过玻璃棒摩擦烧杯壁或加入少量氯化铜固体粉末立即产生大量该晶体,原因是
溶液过饱和也不析出晶体。实验室模拟该过程通过玻璃棒摩擦烧杯壁或加入少量氯化铜固体粉末立即产生大量该晶体,原因是______ 。将
______ ,得到无水 。
。
(4) 是
是 分解的催化剂,其催化过程可用两步表示:
分解的催化剂,其催化过程可用两步表示:
步骤Ⅰ:
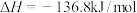
步骤Ⅱ: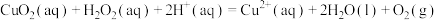

写出 分解的热化学方程式
分解的热化学方程式______ 。
(5)有机供氢剂HL与无水 可发生反应:
可发生反应:
 。某温度下,向密闭容器中加入一定量的
。某温度下,向密闭容器中加入一定量的 和
和 (反应物均足量)。
(反应物均足量)。
①其他条件不变,升高温度HL转化率提高,原因可能有______ 。
②测得反应达到平衡时,该容器压强为120kPa,维持温度等其他条件不变,将容器体积压缩至原容积的一半,达到新平衡时,容器内的压强为______ kPa.
 具有抗菌、杀虫、抗氧化和除藻等功能,从电路板回收无水
具有抗菌、杀虫、抗氧化和除藻等功能,从电路板回收无水 的工艺如下:
的工艺如下:
已知:各离子开始沉淀和完全沉淀的pH如下表:
| 金属离子 |  |  |  |
| 开始沉淀PH | 5.6 | 7.5 | 1.9 |
| 完全沉淀pH | 7.8 | 9.5 | 3.3 |
(1)用离子方程式表示
 的作用
的作用A.CuO B.NaOH C.氨水 D.

(2)废渣的主要成分的化学式是
(3)一系列操作是先蒸发浓缩,冷却结晶得到
 。但冷却结晶时发现
。但冷却结晶时发现 溶液过饱和也不析出晶体。实验室模拟该过程通过玻璃棒摩擦烧杯壁或加入少量氯化铜固体粉末立即产生大量该晶体,原因是
溶液过饱和也不析出晶体。实验室模拟该过程通过玻璃棒摩擦烧杯壁或加入少量氯化铜固体粉末立即产生大量该晶体,原因是
 。
。(4)
 是
是 分解的催化剂,其催化过程可用两步表示:
分解的催化剂,其催化过程可用两步表示:步骤Ⅰ:

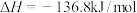
步骤Ⅱ:
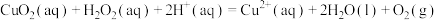

写出
 分解的热化学方程式
分解的热化学方程式(5)有机供氢剂HL与无水
 可发生反应:
可发生反应:
 。某温度下,向密闭容器中加入一定量的
。某温度下,向密闭容器中加入一定量的 和
和 (反应物均足量)。
(反应物均足量)。①其他条件不变,升高温度HL转化率提高,原因可能有
②测得反应达到平衡时,该容器压强为120kPa,维持温度等其他条件不变,将容器体积压缩至原容积的一半,达到新平衡时,容器内的压强为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】铈元素(Ce)是镧系金属中自然丰度最高的一种,常见价态有+3、+4,铈的合金耐高温,可以用来制造喷气推进器零件。
(1)雾霾中含有大量的污染物NO,可以被含Ce4+的溶液吸收。当生成 、
、 的物质的量之比为1:1时,该反应中氧化剂与还原剂的物质的量之比为
的物质的量之比为1:1时,该反应中氧化剂与还原剂的物质的量之比为_______________ 。
(2)采用电解法可将上述吸收液中的 转化为无毒物质,同时再生Ce4+,其原理如右图所示。
转化为无毒物质,同时再生Ce4+,其原理如右图所示。
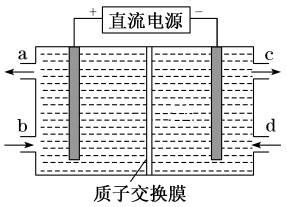
①Ce4+从电解槽的_______ 口流出。(填字母序号)
②每消耗1 mol ,阴极区H+减少
,阴极区H+减少______ mol。
(3)铈元素在自然中主要以氟碳铈矿的形式存在,主要化学成分为CeFCO3,工业上利用氟碳铈矿提取CeCl3的一种工艺流程如下:
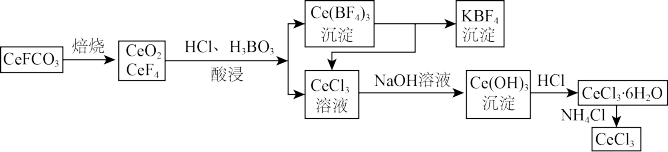
①焙烧过程中发生的主要反应的化学方程式为_________________________________ 。
②酸浸过程中可能会逸出一种污染性气体,这种气体是_______ 。用稀硫酸和H2O2替换盐酸可以避免产生这种气体,此时,酸浸过程中CeO2与H2O2之间所发生反应的离子方程式为______________ 。
③已知Ksp[Ce(BF4)3]=a、Ksp[KBF4]=b,则反应Ce(BF4)3(s)+3K+(aq)⇌3KBF4(s)+Ce3+(aq)平衡常数为______________________ 。
④加热CeCl3·6H2O和NH4Cl的固体混合物可得到无水CeCl3,其中NH4Cl的作用是_________ 。
(1)雾霾中含有大量的污染物NO,可以被含Ce4+的溶液吸收。当生成
 、
、 的物质的量之比为1:1时,该反应中氧化剂与还原剂的物质的量之比为
的物质的量之比为1:1时,该反应中氧化剂与还原剂的物质的量之比为(2)采用电解法可将上述吸收液中的
 转化为无毒物质,同时再生Ce4+,其原理如右图所示。
转化为无毒物质,同时再生Ce4+,其原理如右图所示。
①Ce4+从电解槽的
②每消耗1 mol
 ,阴极区H+减少
,阴极区H+减少(3)铈元素在自然中主要以氟碳铈矿的形式存在,主要化学成分为CeFCO3,工业上利用氟碳铈矿提取CeCl3的一种工艺流程如下:

①焙烧过程中发生的主要反应的化学方程式为
②酸浸过程中可能会逸出一种污染性气体,这种气体是
③已知Ksp[Ce(BF4)3]=a、Ksp[KBF4]=b,则反应Ce(BF4)3(s)+3K+(aq)⇌3KBF4(s)+Ce3+(aq)平衡常数为
④加热CeCl3·6H2O和NH4Cl的固体混合物可得到无水CeCl3,其中NH4Cl的作用是
您最近一年使用:0次