25℃时,浓度均为0.2 mol·L-1的NaHCO3和Na2CO3溶液中,下列判断不正确 的是
| A.均存在电离平衡和水解平衡 |
| B.存在的粒子种类相同 |
| C.c(OH-)前者大于后者 |
D.均存在c(Na+) + c(H+) =2c(CO )+c(HCO )+c(HCO )+c(OH-) )+c(OH-) |
21-22高二上·天津红桥·期末 查看更多[4]
新疆维吾尔自治区喀什市第十四中学2023-2024学年高二上学期1月期末质量检测化学试题(已下线)专项03 四大平衡常数的综合应用-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(天津专用)天津市外国语大学附属外国语学校2021-2022学年高二上学期期末检测化学试题天津市红桥区2021-2022学年高二上学期期末考试化学试题
更新时间:2022-01-19 23:37:14
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】SO2的烟气会形成酸雨,工业上常利用Na2SO3溶液作为吸收液脱除烟气中的SO2。随着SO2的吸收,吸收液的pH不断变化。下列粒子浓度关系一定正确的是
A.Na2SO3溶液中存在:c(Na+)>c(SO )>c(H2SO3)>c(HSO )>c(H2SO3)>c(HSO ) ) |
B.已知NaHSO3溶液pH<7,该溶液中:c(Na+)>c(HSO )>c(H2SO3) >c(SO )>c(H2SO3) >c(SO ) ) |
C.当吸收液呈中性时:c(Na+)=2 c(SO )+c(HSO )+c(HSO ) ) |
D.当吸收液呈酸性时:c(Na+)=c(SO )+c(HSO )+c(HSO )+c(H2SO3) )+c(H2SO3) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】298K时,将V0mL0.1mol•L-1的NaX、NaY溶液分别加水稀释至VmL的过程中,溶液的pH与lg 的变化关系如图。下列说法不正确的是
的变化关系如图。下列说法不正确的是

 的变化关系如图。下列说法不正确的是
的变化关系如图。下列说法不正确的是
| A.酸HY的电离常数约为10-5mol•L-1 |
| B.水的电离程度M点大于N点 |
| C.等浓度的NaX溶液和NaY溶液中阴离子浓度后者大 |
| D.M点溶液中c(OH-)>c(H+)+c(X-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法不正确 的是
| A.实验室酸、碱废液在确定混合无危险时可用中和法处理 |
| B.X射线衍射仪可用于有机化合物晶体结构的测定 |
| C.可用FeCl3溶液区分氢氧化钠溶液和碳酸钠溶液 |
| D.可用溴水除去苯中含有的少量苯酚 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列反应不属于水解反应或水解方程式不正确的是
①HCl+H2O H3O++Cl-
H3O++Cl-
②AlCl3+3H2O=Al(OH)3+3HCl
③Na2CO3+2H2O H2CO3+2NaOH
H2CO3+2NaOH
④碳酸氢钠溶液:HCO3-+H2O CO32-+H3O+
CO32-+H3O+
⑤NH4Cl溶于D2O中:NH4++D2O NH3·D2O+H+
NH3·D2O+H+
⑥HS-的水解:HS-+H2O S2-+H3O+
S2-+H3O+
⑦将饱和FeCl3溶液滴入沸腾的水中:FeCl3+3H2O Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl
①HCl+H2O
 H3O++Cl-
H3O++Cl-②AlCl3+3H2O=Al(OH)3+3HCl
③Na2CO3+2H2O
 H2CO3+2NaOH
H2CO3+2NaOH④碳酸氢钠溶液:HCO3-+H2O
 CO32-+H3O+
CO32-+H3O+⑤NH4Cl溶于D2O中:NH4++D2O
 NH3·D2O+H+
NH3·D2O+H+⑥HS-的水解:HS-+H2O
 S2-+H3O+
S2-+H3O+⑦将饱和FeCl3溶液滴入沸腾的水中:FeCl3+3H2O
 Fe(OH)3(胶体)+3HCl
Fe(OH)3(胶体)+3HCl| A.①②③④ | B.①②③ |
| C.②③⑤⑥⑦ | D.全部 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下 pH = 3 的醋酸溶液,下列有关叙述正确的是
| A.加水稀释 100 倍后,pH = 5 |
| B.该溶液中离子浓度大小关系:c(H+) > c(CH3COO-) > c(OH-) |
| C.加入等体积、pH = 11 的 NaOH 溶液后,混合溶液中 c(Na+) = c(CH3COO-) |
| D.滴加 0.1 mol·L-1 CH3COONa 溶液至 c(CH3COO-) < c(Na+)时,溶液的pH < 7 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列物质因发生水解反应使溶液呈碱性的是
| A.HNO3 | B.AlCl3 | C.NaHCO3 | D.Ba(OH)2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验设计、现象和结论都正确的是
| 选项 | 实验目的 | 实验设计和现象 | 实验结论 |
| A | 探究淀粉的水解程度 | 将淀粉溶液在酸性条件下加热一段时间后,向水解液中滴加银氨溶液,加热,未出现光亮的银镜 | 淀粉尚未水解 |
| B | 判断久置的亚硫酸钠是否变质 | 取一定质量的亚硫酸钠固体于试管中,加蒸馏水完全溶解后,滴加BaCl2溶液,出现白色沉淀 | 亚硫酸钠已变质 |
| C | 检验溶液中是否含Fe2+ | 向待测液中通入氯气并加入KSCN溶液,溶液变红 | 溶液中含有Fe2+ |
| D | 探究 和 和 反应原理 反应原理 | 向 溶液中滴加 溶液中滴加 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | 溶液中 结合 结合 的能力比 的能力比 强 强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】在 溶液中存在着多种离子和分子,下列关系不正确的是
溶液中存在着多种离子和分子,下列关系不正确的是
 溶液中存在着多种离子和分子,下列关系不正确的是
溶液中存在着多种离子和分子,下列关系不正确的是A. |
B. |
C. |
D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】25℃时,向20mL0.1mol/LHAuCl4溶液中滴加0.1mol/LNaOH溶液,滴定曲线如图1所示,含氯微粒的物质的量分数(δ)随pH的变化关系如图2所示,下列说法不正确的是
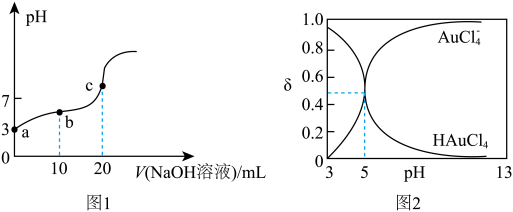

| A.Kn(HAuCl4)=10-5 |
B.b点对应溶液中:c(Na+)>c(AuCl ) ) |
| C.c点对应溶液中:c(OH-)-c(H+)=c(HAuCl4) |
D.滴定过程中,n(HAuCl4)+n(AuCl )始终保持不变 )始终保持不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,某二元酸H2R及其钠盐的溶液中,H2R、HR-、R2-三者的物质的量分数随溶液pH变化关系如图所示,下列叙述正确的是


| A.该酸的电离方程式为:H2R=2H++R2- |
| B.等体积、等浓度的NaOH溶液与H2R溶液混合后,此溶液中水的电离程度比纯水大 |
| C.在pH=4.3的溶液中:2c(R2-)=c(Na+)+c(H+)-c(OH-) |
| D.该酸一级电离平衡常数Ka1=10-1.3 |
您最近一年使用:0次

 二元弱酸
二元弱酸 溶液的
溶液的 ,溶液中的
,溶液中的 的物质的量分数
的物质的量分数 随
随
 的
的 的数量级为
的数量级为
 时,溶液中一定存在:
时,溶液中一定存在: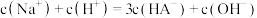
 时,
时,
 溶液中一定存在
溶液中一定存在


