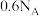25°C时部分电解质的电离平衡常数数据如下。
已知H2R=H++HR-,HR- H++R2-。下列说法错误的是
H++R2-。下列说法错误的是
| CH3COOH | H2CO3 | HClO | H2R |
| Ka=1.8×10-5 | Ka1=4.2×10-7 Ka2=5.6×10-11 | Ka=4.7×10-8 | Ka(HR-)=0.0118 |
 H++R2-。下列说法错误的是
H++R2-。下列说法错误的是| A.NaHR溶液中既存在HR-的电离也存在HR-的水解 |
| B.等浓度溶液的pH:Na2CO3>NaClO>CH3COONa |
C.向NaClO溶液中通入少量CO2,漂白性增强的原因是ClO-+CO2+H2O=HClO+HCO |
D.等浓度的NaClO和NaHCO3混合溶液中存在c(HClO)+c(ClO-)=c(HCO )+c(CO )+c(CO )+c(H2CO3) )+c(H2CO3) |
更新时间:2022-01-22 17:43:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是( )
| A.pH=4的醋酸中:c(H+)=4.0mol/L |
B.饱和小苏打溶液中:c(Na+)=c(HCO ) ) |
| C.相同温度下,pH相等的盐酸、CH3COOH溶液中,c(CH3COO-)=c(Cl-) |
| D.室温时,用广泛pH试纸测得某溶液pH为2.3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向 0.1
0.1 氨水中滴加等浓度的稀高氯酸,测得混合溶液的温度和
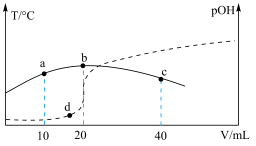
氨水中滴加等浓度的稀高氯酸,测得混合溶液的温度和 随着加入稀高氯酸的体积变化如图所示(图中实线为温度变化,虚线为pOH变化)。下列说法错误的是( )
随着加入稀高氯酸的体积变化如图所示(图中实线为温度变化,虚线为pOH变化)。下列说法错误的是( )
 0.1
0.1 氨水中滴加等浓度的稀高氯酸,测得混合溶液的温度和
氨水中滴加等浓度的稀高氯酸,测得混合溶液的温度和 随着加入稀高氯酸的体积变化如图所示(图中实线为温度变化,虚线为pOH变化)。下列说法错误的是( )
随着加入稀高氯酸的体积变化如图所示(图中实线为温度变化,虚线为pOH变化)。下列说法错误的是( )
A.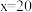 |
B.b、c点由水电离出的 大小为b>c 大小为b>c |
C.b点时溶液中微粒浓度存在关系: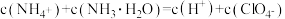 |
D.a、d点对应氨水的电离常数: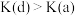 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在下列各微粒中,室温下能使水的电离平衡向电离的方向移动,且使溶液的pH>7的是
| A.Al3+ | B.HCO3- | C.HSO4- | D.26X3+ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法不正确的是
| A.pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大 |
| B.将NaCl溶液从常温加热至80℃,溶液的pH变小 |
| C.NaHA溶液呈酸性,说明H2A为弱酸,且HA﹣的电离程度大于水解 |
| D.室温下,100mLpH=10.0的Na2CO3溶液中水电离出OH﹣的物质的量为1.0×10﹣5mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】酒石酸是葡萄酒中特有的一种有机酸,葡萄酒的pH主要取决于酒石酸的含量,正常的葡萄酒pH约为2.9~3.8。常温下,酒石酸(用H2T表示)水溶液中三种微粒所占的分数(a)与pH的关系如图所示。下列表述不正确的是
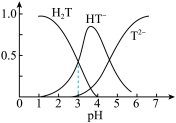

| A.葡萄酒中除了存在酒石酸外,还存在酒石酸盐 |
B.常温下,H2T H++HT- Ka=10-3 H++HT- Ka=10-3 |
| C.当葡萄酒的pH为3.7时,HT一所占分数达到最大,此时葡萄酒中H2T>T2- |
| D.当HT一和T2-物质的量浓度相等时,溶液中水电离出来的氢离子浓度小于纯水中氢离子的浓度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列有关电解质溶液的说法正确的是
| A.25℃时,pH=3的H2SO4溶液和pH=10的NaOH溶液恰好完全中和,消耗酸和碱的体积比为1:10 |
B.将CH3COONa溶液从20 ℃升温至30 ℃,溶液中 增大 增大 |
C.K2CO3、CH3COOK 和KCl 的混合溶液中,一定满足:c(K+)+c(H+)=2c(CO )+c(HCO )+c(HCO )+c(OH-)+c(CH3COO-) )+c(OH-)+c(CH3COO-) |
| D.升高温度,水的电离平衡正向移动,故c(H+)增大, Kw增大,pH也随之增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】将0.2mol·L-1HCN溶液和0.1mol·L-1的NaOH溶液等体积混合后,溶液显碱性,下列关系式中正确的是
| A.c(HCN)<c(CN-) | B.c(Na+)>c(CN-) |
| C.c(Na+)>c(HCN) | D.c(HCN)+c(CN-)=0.2mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,向碳酸钠的溶液中通入过量SO2可制备NaHSO3,主要流程如图,下列叙述错误的是
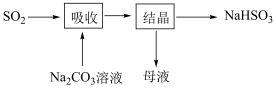
已知H2CO3:Ka1=4.4×10-7,Ka2=5.6×10-11;H2SO3:Ka1=1.3×10-2,Ka2=6.2×10-8。

已知H2CO3:Ka1=4.4×10-7,Ka2=5.6×10-11;H2SO3:Ka1=1.3×10-2,Ka2=6.2×10-8。
A.Na2CO3溶液中:c(H+)+c(HCO )+2c(H2CO3)=c(OH-) )+2c(H2CO3)=c(OH-) |
B.通入SO2开始时反应为2CO +SO2+H2O=SO +SO2+H2O=SO +2HCO +2HCO |
C.当吸收SO2后pH=9的溶液中:c(HCO )<c(CO )<c(CO )<c(Na+) )<c(Na+) |
D.母液中加KOH至中性时:3c(SO )<c(Na+)+c(K+) )<c(Na+)+c(K+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,某混合溶液中c(CH3COOH)+c(CH3COO-)=0.1mol·L-1,lgc(CH3COOH)、lgc(CH3COO-)、lgc(H+)和lgc(OH-)随pH变化的关系如图所示。Ka为CH3COOH的电离常数,Kh为CH3COO-水解常数,下列说法错误的是
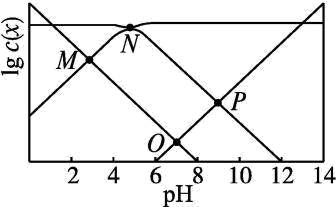

| A.N点时,c(CH3COOH)=c(CH3COO-) |
| B.P点时,pOH=-lgKh |
| C.由O点到P对应的反应过程中,CH3COO-的水解程度减小 |
D.该体系中,c(H+)=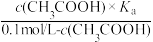 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知25℃时,几种弱酸的电离常数如下:
25℃时,下列说法正确的是
| 弱酸的化学式 | CH3COOH | HCN | H2S |
| 电离常数 |  |  | 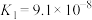 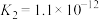 |
| A.某浓度的NaCN溶液的pH=d,则其中由水电离出的c(OH-)=10-d mol/L |
| B.用0.1 mol/L的NaOH溶液滴定pH相等的CH3COOH和HCN溶液,CH3COOH消耗的NaOH溶液体积更大 |
C.NaHS和Na2S的混合溶液中,一定存在 |
| D.常温下,pH=4的CH3COOH和pH=10的NaOH溶液等体积混合后,溶液中离子浓度由大到小的顺序为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) |
您最近一年使用:0次

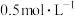
 的过程中,下列关系式的值随加入水的体积增大而减小的是
的过程中,下列关系式的值随加入水的体积增大而减小的是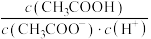

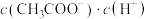

 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是 溶液中
溶液中 的数目为
的数目为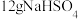 固体中含有的阳离子数为
固体中含有的阳离子数为
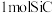 晶体中含有
晶体中含有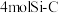
 乙醛
乙醛 中含有
中含有 的
的 键数目为
键数目为