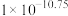在25℃时,向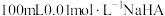 溶液中分别加入浓度均为
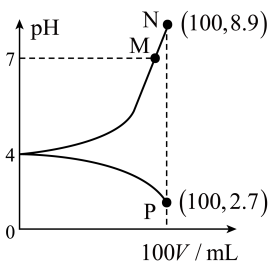
溶液中分别加入浓度均为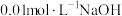 溶液和盐酸,混合溶液的pH随着所加溶液体积的变化如图所示。下列说法正确的是
溶液和盐酸,混合溶液的pH随着所加溶液体积的变化如图所示。下列说法正确的是
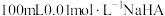 溶液中分别加入浓度均为
溶液中分别加入浓度均为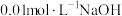 溶液和盐酸,混合溶液的pH随着所加溶液体积的变化如图所示。下列说法正确的是
溶液和盐酸,混合溶液的pH随着所加溶液体积的变化如图所示。下列说法正确的是
A.25℃时, 的第二步电离平衡常数约为 的第二步电离平衡常数约为 |
B. 溶液中: 溶液中: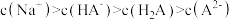 |
C.P点时溶液中存在: |
| D.水的电离程度:M>N>P |
更新时间:2022-01-23 19:53:12
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】如图表示水中c(H+)和c(OH-)的关系,下列判断错误的是
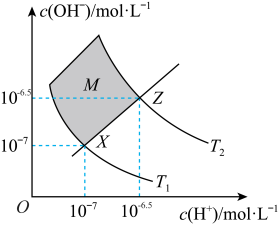

| A.XZ线上任意点均有c(H+)=c(OH-) |
| B.M区域内(不包括边界)任意点均有c(H+)<c(OH-) |
| C.温度为T2时,pH=9的NaOH溶液与pH=12的NaOH溶液等体积混合,该混合液的pH为11.7 |
| D.温度为T2时,某溶液由水电离出H+的浓度为10-8mol/L,则该溶液的pH=8 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】25℃下,向20.00mL0.1mol/L二元弱酸H2X溶液中滴入0.1mol/LNaOH溶液,溶液中由水电离出的c水(OH-)的负对数[-lgc水(OH-)]与所加NaOH溶液体积的关系如图所示:

下列说法中不正确的是

下列说法中不正确的是
| A.M点溶液中:c(Na+)>c(HX-)>c(X2-) |
| B.水的电离程度:P>N=Q>M |
| C.N、Q两点溶液pH值均等于7 |
D.溶液中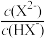 :M<N<P<Q :M<N<P<Q |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】根据下列实验操作和现象,得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 常温下,用pH计分别测定等体积1  溶液和0.1 溶液和0.1  溶液的pH,测得的pH值相同 溶液的pH,测得的pH值相同 | 浓度对水的电离程度无影响 |
| B | 灼烧铜丝至其表面变黑、灼热,伸入盛有某有机物的试管中,铜丝恢复亮红色 | 该有机物中可能有醇羟基或羧基 |
| C | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去,试管里出现凝胶 | 非金属性:Cl>Si |
| D | 加热麦芽糖和稀 混合溶液,冷却;加入NaOH溶液后加入银氨溶液,加热,出现银镜 混合溶液,冷却;加入NaOH溶液后加入银氨溶液,加热,出现银镜 | 麦芽糖发生了水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】在常温下,有关下列4种溶液的叙述中正确的是
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
 | 11 | 11 | 3 | 3 |
| A.在溶液①、②中分别加入适量的氯化铵晶体后,两种溶液的pH不都减小 |
| B.分别加水稀释10倍,四种溶液的pH:②>①>④>③ |
C.将溶液①、④等体积混合,所得溶液中: |
| D.将aL溶液④与bL溶液②混合后,若所得溶液的pH=4,则a:b=11:9 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下,pH=10的强碱溶液与pH=3的强酸溶液混合,所得混合液的pH=5,则强酸与强碱的体积比是
| A.11:1 | B.9:1 | C.1:9 | D.1:11 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】电解质溶液电导率越大导电能力越强。常温下用0.100 mol·L-1盐酸分别滴定10.00 mL浓度均为0.100 mol·L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氨相似,常温Kb[(CH3)2NH·H2O]=1.6×10-4]。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法不正确的是( )


| A.曲线②代表滴定二甲胺溶液的曲线 |
| B.b点溶液中:pH<7 |
| C.d点溶液中:c(H+)=c(OH-)+c[(CH3)2NH·H2O] |
| D.c、d、e三点的溶液中,水的电离程度最大的是d点 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知AG=lg ,电离度α=
,电离度α= ×100%。常温下,向10mL0.1mol/LHX溶液中滴加0.1mol/LNaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。
×100%。常温下,向10mL0.1mol/LHX溶液中滴加0.1mol/LNaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。
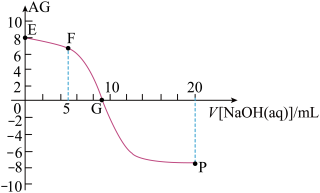
下列说法错误的是( )
 ,电离度α=
,电离度α= ×100%。常温下,向10mL0.1mol/LHX溶液中滴加0.1mol/LNaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。
×100%。常温下,向10mL0.1mol/LHX溶液中滴加0.1mol/LNaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。
下列说法错误的是( )
| A.F点溶液pH<7 |
| B.G点溶液中c(Na+)=c(X-)>c(H+)=c(OH-) |
| C.V=10时,溶液中c(OH-)<c(HX) |
| D.常温下,HX的电离度约为1% |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】常温下,用0.10 mol·L-1 KOH溶液滴定10.00 mL 0.10 mol·L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成两者溶液的体积之和),下列说法正确的是( )
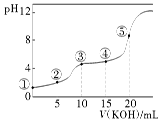
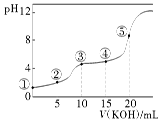
| A.点②所示溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-) |
| B.点③所示溶液中:c(K+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-) |
| C.点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.10 mol·L-1 |
| D.点⑤所示溶液中:c(OH-)= c(H+)+ c(HC2O4-)+ c(C2O42-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】天然水体中的碳酸盐系统(CO2、H2CO3、HCO 、CO
、CO ),微粒不同浓度分布会影响溶液的pH。某温度下,溶洞水体中lgc(X)(X为H2CO3、HCO
),微粒不同浓度分布会影响溶液的pH。某温度下,溶洞水体中lgc(X)(X为H2CO3、HCO 、CO
、CO 或Ca2+)与pH关系如图所示。下列说法错误的是
或Ca2+)与pH关系如图所示。下列说法错误的是

 、CO
、CO ),微粒不同浓度分布会影响溶液的pH。某温度下,溶洞水体中lgc(X)(X为H2CO3、HCO
),微粒不同浓度分布会影响溶液的pH。某温度下,溶洞水体中lgc(X)(X为H2CO3、HCO 、CO
、CO 或Ca2+)与pH关系如图所示。下列说法错误的是
或Ca2+)与pH关系如图所示。下列说法错误的是
| A.H2CO3的Ka1数量级为10-9 |
B.溶液中可能存在c(Ca2+)+c(H+)=c(OH-)+c(CO )+c(HCO )+c(HCO ) ) |
| C.曲线②lgc(X)不变的原因是水体中的H2CO3和空气中的CO2保持平衡 |
| D.该温度下c(Ca2+)与c2(H+)为线性关系 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】室温下,向某浓度的二元碱X(OH)2水溶液中逐滴加入一定浓度的盐酸,所得溶液中相关组分的物质的量分数随溶液pH变化的曲线如图所示。下列说法错误的是


| A.X(OH)2的Kb1=10-4.8 |
| B.X(OH)Cl的水溶液显碱性 |
| C.pH=7时,c[X(OH)2]<c(X2+)<c[X(OH)+] |
| D.pH=9.2时,c(OH-)=2c(X2+)+c(H+)+c[X(OH)+] |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】两种溶液混合后的成分与溶液酸碱性的变化可能有关,下列说法正确的是
A. 的 的 溶液与 溶液与 的NaOH溶液等体积混合后所得溶液中: 的NaOH溶液等体积混合后所得溶液中: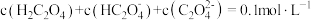 |
B.等体积、等物质的量浓度的 溶液和 溶液和 溶液混合: 溶液混合: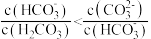 |
C.常温下, 的HA溶液与 的HA溶液与 的BOH溶液等体积混合,所得溶液pH>7,则 的BOH溶液等体积混合,所得溶液pH>7,则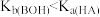 |
D.向某 溶液中加入少量 溶液中加入少量 晶体,所得溶液中 晶体,所得溶液中 水解程度增大,pH增大 水解程度增大,pH增大 |
您最近一年使用:0次

 。25℃时,用0.100
。25℃时,用0.100 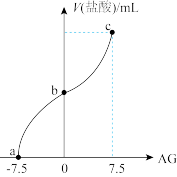
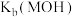 约为
约为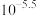
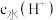 为
为