在常温下,有关下列4种溶液的叙述中正确的是
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
 | 11 | 11 | 3 | 3 |
| A.在溶液①、②中分别加入适量的氯化铵晶体后,两种溶液的pH不都减小 |
| B.分别加水稀释10倍,四种溶液的pH:②>①>④>③ |
C.将溶液①、④等体积混合,所得溶液中: |
| D.将aL溶液④与bL溶液②混合后,若所得溶液的pH=4,则a:b=11:9 |
更新时间:2023-12-15 14:13:12
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】常温下,将pH=3的HA溶液V1mL与pH=11的NaOH溶液V2mL混合,则下列说法不正确的是
| A.若反应后溶液呈酸性,则V1一定大于V2 |
| B.若V1=V2,反应后溶液的PH可能等于7 |
| C.若反应后溶液呈中性,则c(H+)+c(OH-)=2×10-7mol/L |
| D.若反应后溶液呈碱性,则V1一定小于V2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下用aLpH=3的HX溶液与bLpH=11的氢氧化钠溶液相混合,下列叙述正确的是
| A.若两者恰好中和,则一定是a=b |
| B.若混合液显碱性,则一定是b≥a |
| C.若混合液显中性,则一定是a≤b |
| D.若混合液显酸性,则一定是a≥b |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】在0.1mol·L-1 CH3COOH溶液中存在如下电离平衡CH3COOH CH3COO-+H+对于该平衡,下列叙述正确的是
CH3COO-+H+对于该平衡,下列叙述正确的是
 CH3COO-+H+对于该平衡,下列叙述正确的是
CH3COO-+H+对于该平衡,下列叙述正确的是| A.溶液PH等于1 |
| B.加入少量NaOH固体,平衡向正反应方向移动 |
| C.加入少量0.1 mol·L-1 HCl溶液,溶液中c(H+)降低 |
| D.加入少量CH3COONa固体,平衡向左移动,导电能力不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】25℃时,下列关系式正确的是
| A.pH=2的CH3COOH 溶液与pH=12的NaOH溶液等体积混合:c(Na+)=c(CH3COO-)>c(CH3COOH) |
| B.盐酸与FeCl3的混合溶液pH=2,稀释10倍后:pH<3 |
| C.pH相同的① NH4HSO4、② NH4Cl、③(NH4)2SO4三种溶液的c(NH4+): ③>①>② |
| D.pH=3的H2C2O4溶液:c(H+)=c(HC2O4-)+c(OH-)=1×10-3mol/L |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】下列物质溶于水时会破坏水的电离平衡,且属于强电解质的是
| A.酒精 | B.冰醋酸 | C.硝酸钾 | D.醋酸钠 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列事实不能用勒夏特列原理解释的是
| A.升高温度,水的 Kw 增大 |
| B.实验室中常用排饱和食盐水的方法收集氯气 |
C.对2HI(g) H2(g)+I2(g)平衡体系加压,颜色迅速变深 H2(g)+I2(g)平衡体系加压,颜色迅速变深 |
| D.开启啤酒瓶后,瓶中马上泛起大量泡沫 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列说法中正确的是( )
A.已知0.1 mol·L-1的CH3COOH溶液中存在电离平衡:CH3COOH CH3COO-+H+,加少量烧碱溶液可使溶液 CH3COO-+H+,加少量烧碱溶液可使溶液 增大 增大 |
B.25 ℃时,向水中加入少量固体CH3COONa,水的电离平衡:H2O H++OH-逆向移动,c(H+)降低 H++OH-逆向移动,c(H+)降低 |
C.室温下向10 mL pH=3的醋酸溶液中加水稀释后,溶液中 不变 不变 |
| D.0.1 mol·L-1的醋酸加水稀释后,溶液中所有离子的浓度均减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】已知亚硒酸(H2SeO3)为二元弱酸,常温下,向某浓度的亚硒酸溶液中逐滴加入一定浓度的NaOH溶液,所得溶液中H2SeO3、HSeO3-、SeO32-三种微粒的物质的量分数与溶液pH 的关系如图所示。下列说法不正确的是
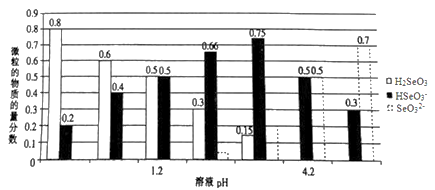

| A.将相同物质的量NaHSeO3和Na2SeO3 固体完全溶于水可配得pH为4.2的混合液 |
| B.pH=l.2的溶液中:c(Na+)+c(H+)=c(OH-)+c(H2SeO3) |
| C.常温下,亚硒酸的电离平衡常数K2=10-4.2 |
| D.向pH=1.2的溶液中滴加NaOH溶液至pH=4.2的过程中水的电离程度一直增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】测定溶液电导率的变化是定量研究电解质在溶液中反应规律的一种方法,溶液电导率越大其导电能力越强。室温下,用0.100mol•L-1的NH3•H2O滴定10.00mL浓度均为0.100mol•L-1HCl和CH3COOH的混合溶液,所得电导率曲线如图所示。下列说法正确的是( )
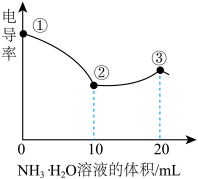

| A.①点溶液:pH最大 |
| B.溶液温度:①高于② |
| C.③点溶液中:c(Cl-)>c(CH3COO-) |
| D.②点溶液中:c(NH4+)+c(NH3•H2O)>c(CH3COOH)+c(CH3COO-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】25 ℃时,将1.0 L w mol·L-1的CH3COOH溶液与0.1 mol的NaOH固体混合,充分反应后向混合液中通(加)入HCl气体或NaOH固体。溶液pH随通(加)入HCl或NaOH的物质的量的变化如下图。下列叙述正确的是 ( )
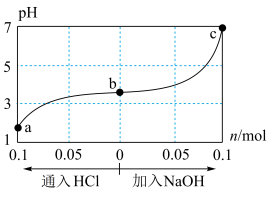

| A.a、b、c对应的混合液中,水的电离程度由大到小的顺序是a>b>c |
B.若忽略体积变化,则25 ℃时,CH3COOH的电离平衡常数K=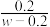 ×10-7 mol·L-1 ×10-7 mol·L-1 |
C.加入NaOH过程中,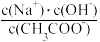 逐渐减小 逐渐减小 |
| D.加入NaOH过程中,c(Na+)·c(CH3COO-)逐渐减小 |
您最近一年使用:0次

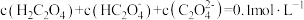 的草酸溶液。
的草酸溶液。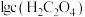 、
、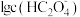 和
和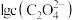 随
随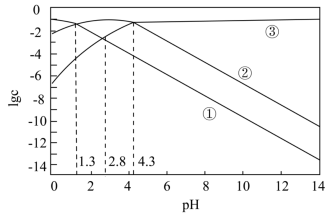
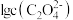
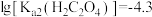
 时,
时,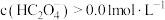
 时,
时,