常温下,几种弱酸的电离平衡常数如表所示,下列说法正确的是
| 化学式 | HCOOH | H2CO3 | HCN |
| 电离平衡常数 | K=1.8×10-4 | K1=4.3×10-7、K2=5.6×10-11 | K=4.9×10-10 |
A.结合H+的能力由大到小:CO <CN-<HCO <CN-<HCO <HCOO- <HCOO- |
| B.等物质的量浓度的HCOONa溶液和NaCN溶液,pH大小顺序:HCOONa>NaCN |
| C.加水稀释HCOOH溶液,其电离平衡常数将减小 |
D.NaCN溶液中通入少量的CO2反应的离子方程式为CN-+CO2+H2O=HCO +HCN +HCN |
更新时间:2022-01-05 16:14:31
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法中正确的是( )
A.常温下,pH均等于2的硫酸溶液与醋酸溶液,两种溶液中c(SO )与c(CH3COO-)之比为1∶2 )与c(CH3COO-)之比为1∶2 |
| B.常温下,向pH=1.0的醋酸溶液中加入水稀释后,溶液中c(H+)和c(OH-)都将变小 |
| C.常温下,0.1 mol·L-1 NaHA溶液的pH=4,溶液中:c(HA-)>c(H+)>c(H2A)>c(A2-) |
D.0.1 mol·L-1的(NH4)2Fe(SO4)2溶液中:c(NH4+)=c(SO )>c(Fe2+)>c(H+) )>c(Fe2+)>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列物质中属于弱电解质的是
| A.CO2 | B.氨水 | C.HClO | D.BaSO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下,向25mL0.1mol·L-1HA溶液中滴加一定浓度的氢氧化钠溶液,滴定曲线如图所示。下列有关说法正确的是


| A.HA为弱酸,Ka≈1×10-3 |
| B.氢氧化钠的物质的量浓度等于0.1mol·L-1 |
| C.a点溶液中2c(Na+)=c(A-)+c(HA) |
| D.b点溶液中c(Na+)>c(A-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知醋酸在水溶液中建立如下电离平衡: CH3COOH H++ CH3COO-,若只改变一个条件,一定可以使c(CH3COOH)/c(H+)减小的是
H++ CH3COO-,若只改变一个条件,一定可以使c(CH3COOH)/c(H+)减小的是
 H++ CH3COO-,若只改变一个条件,一定可以使c(CH3COOH)/c(H+)减小的是
H++ CH3COO-,若只改变一个条件,一定可以使c(CH3COOH)/c(H+)减小的是| A.通氯化氢气体 | B.加入少量醋酸钾固体 |
| C.加入少量氢氧化钠固体 | D.通入少量冰醋酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某研究小组为了探究NaClO溶液的性质,设计了下列实验,并记录实验现象。
则以下判断错误的是
| 实验装置 | 实验序号 | 滴管试剂 | 试管试剂 | 实验现象 |
 | ① |  NaClO溶液 NaClO溶液 | 饱和 溶液 溶液 | 产生白色沉淀,继而转化为棕黑色沉淀 |
| ② |  溶液 溶液 | 光照管壁有无色气泡产生 | ||
| ③ |   酸性溶液和KSCN溶液 酸性溶液和KSCN溶液 | 溶液变红 | ||
| ④ |   溶液 溶液 | 产生白色沉淀 |
A.实验①:发生的反应为 |
B.实验②:无色气体为 |
C.实验③:还原性强弱顺序: |
D.实验④: 与 与 的水解相互促进 的水解相互促进 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列事实中不一定能证明CH3COOH是弱电解质的是
| A.用CH3COOH溶液做导电实验,灯泡很暗 |
| B.常温下某CH3COONa溶液的pH=8 |
| C.等pH、等体积的盐酸、CH3COOH溶液分别和足量锌反应,CH3COOH放出的氢气较多 |
| D.CH3COONa和H3PO4反应,生成CH3COOH |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知常温下 ,下列有关电解质溶液的叙述正确的是
,下列有关电解质溶液的叙述正确的是
 ,下列有关电解质溶液的叙述正确的是
,下列有关电解质溶液的叙述正确的是A.在 的氨水溶液中 的氨水溶液中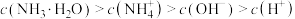 |
B.向 的氨水溶液中加入等体积 的氨水溶液中加入等体积 的醋酸,溶液的导电性减弱 的醋酸,溶液的导电性减弱 |
C.向 的氨水溶液中加水稀释,溶液中 的氨水溶液中加水稀释,溶液中 的比值减小 的比值减小 |
D.等物质的量浓度的氨水和 溶液等体积混合后 溶液等体积混合后 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
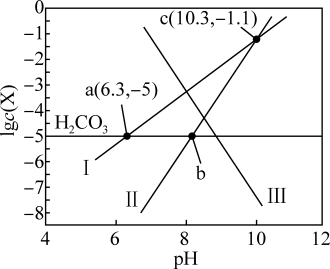
【推荐2】溶洞水体中的H2CO3与空气中的CO2保持平衡,其水体中lgc(X)(X为H2CO3、HCO 、CO
、CO 或Ca2+)与pH的关系如图所示。已知Ksp(CaCO3)=2.8×10-9,下列说法错误的是
或Ca2+)与pH的关系如图所示。已知Ksp(CaCO3)=2.8×10-9,下列说法错误的是
 、CO
、CO 或Ca2+)与pH的关系如图所示。已知Ksp(CaCO3)=2.8×10-9,下列说法错误的是
或Ca2+)与pH的关系如图所示。已知Ksp(CaCO3)=2.8×10-9,下列说法错误的是
A. |
B.线Ⅱ代表CO 与pH的关系曲线 与pH的关系曲线 |
| C.2pH(b)>pH(a)+pH(c) |
| D.a点溶液中,c(Ca2+)=2.8mol/L |
您最近一年使用:0次

 的盐酸、一氯乙酸
的盐酸、一氯乙酸 溶液至
溶液至 ,溶液的
,溶液的 与
与 的关系如图所示。
的关系如图所示。
 代表盐酸的
代表盐酸的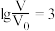 时,加热两种溶液,
时,加热两种溶液, 不变
不变 的电离常数
的电离常数 为
为

 相等(HR代表HCOOH或HClO)
相等(HR代表HCOOH或HClO)


