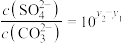常温下,向 一定浓度的硫酸铜溶液中逐滴滴入
一定浓度的硫酸铜溶液中逐滴滴入 的氨水,首先析出浅蓝色的
的氨水,首先析出浅蓝色的 沉淀,氨水过量时此沉淀溶解,形成
沉淀,氨水过量时此沉淀溶解,形成 络离子(假定溶液混合后体积不变)。滴加过程中
络离子(假定溶液混合后体积不变)。滴加过程中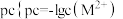 ,
, 为
为 或
或 与氨水体积的关系如图所示。下列说法错误的是
与氨水体积的关系如图所示。下列说法错误的是
 一定浓度的硫酸铜溶液中逐滴滴入
一定浓度的硫酸铜溶液中逐滴滴入 的氨水,首先析出浅蓝色的
的氨水,首先析出浅蓝色的 沉淀,氨水过量时此沉淀溶解,形成
沉淀,氨水过量时此沉淀溶解,形成 络离子(假定溶液混合后体积不变)。滴加过程中
络离子(假定溶液混合后体积不变)。滴加过程中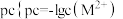 ,
, 为
为 或
或 与氨水体积的关系如图所示。下列说法错误的是
与氨水体积的关系如图所示。下列说法错误的是
A.硫酸铜溶液的浓度为 |
B.常温下, 点溶液中水的电离程度低于纯水的 点溶液中水的电离程度低于纯水的 |
C. 点溶液中存在 点溶液中存在 |
D.常温下,忽略 的影响,可得 的影响,可得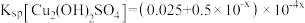 |
更新时间:2022-03-02 00:26:14
|
相似题推荐
多选题
|
较难
(0.4)
解题方法
【推荐1】25℃时,向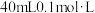 的
的 溶液中逐滴加入
溶液中逐滴加入 的
的 溶液,溶液的
溶液,溶液的 随加入
随加入 溶液体积的变化关系如图所示。下列说法错误的是
溶液体积的变化关系如图所示。下列说法错误的是
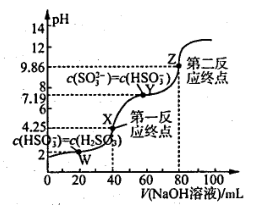
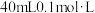 的
的 溶液中逐滴加入
溶液中逐滴加入 的
的 溶液,溶液的
溶液,溶液的 随加入
随加入 溶液体积的变化关系如图所示。下列说法错误的是
溶液体积的变化关系如图所示。下列说法错误的是
A.X点时,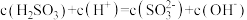 |
B.Y点时,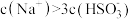 |
C. 的水解平衡常数 的水解平衡常数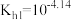 |
D.水的电离程度: |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】室温下,向10mL0.1mol·L-1HA溶液中滴加0.1mol·L-1的NaOH溶液,溶液的酸度(AG)与NaOH溶液体积的关系如图所示。已知:AG=lg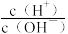 。
。
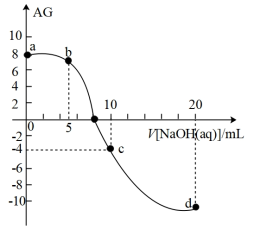
下列说法错误的是
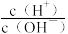 。
。
下列说法错误的是
| A.在a、b、c、d点对应的溶液中,c点时水的电离程度最大 |
| B.b点对应的溶液中:c(A-)>c(Na+)>c(H+)>c(OH-) |
| C.d点对应的溶液中:c(OH-)=c(H+)+c(HA)+c(A-) |
| D.室温下,HA的电离常数Ka约为1.0×10-4 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐1】25℃时,将V mL 0.10mol·L-1的NaOH溶液逐滴滴入到20.00mL 0.10mol·L-1的醋酸溶液中,溶液pH随所加V(NaOH)的变化而变化(忽略混合时溶液体积变化),数据如下表所示:
下列说法正确的是
编号 | ① | ② | ③ |
V(NaOH)/mL | 10.00 | x | 20.00 |
pH | 4.70 | 7.00 | 8.70 |
| A.①中存在c(CH3COO-)>c(Na+)=0.05mol·L-1 |
| B.②中存在c(CH3COOH)<c(Na+)=c(CH3COO-)=x /(200+10x) |
| C.③中存在c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.05mol·L-1 |
| D.通过①进行近似计算可知醋酸的数量级是10-6 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】 时,向
时,向 的
的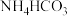 溶液(
溶液( )中通入
)中通入 或加入
或加入 调节
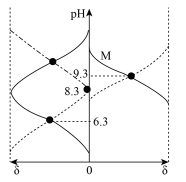
调节 ,不考虑溶液体积变化且过程中无气体逸出。含碳(或氮)微粒的分布分数
,不考虑溶液体积变化且过程中无气体逸出。含碳(或氮)微粒的分布分数 [如:
[如: ]与
]与 关系如图。下列说法正确的是
关系如图。下列说法正确的是
 时,向
时,向 的
的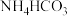 溶液(
溶液( )中通入
)中通入 或加入
或加入 调节
调节 ,不考虑溶液体积变化且过程中无气体逸出。含碳(或氮)微粒的分布分数
,不考虑溶液体积变化且过程中无气体逸出。含碳(或氮)微粒的分布分数 [如:
[如: ]与
]与 关系如图。下列说法正确的是
关系如图。下列说法正确的是
A. 溶液中存在: 溶液中存在: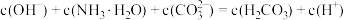 |
B.曲线M表示 的分布分数随 的分布分数随 变化 变化 |
C.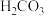 的 的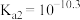 |
D.该体系中 |
您最近一年使用:0次
多选题
|
较难
(0.4)
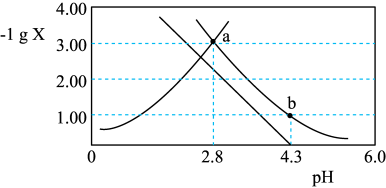
【推荐3】常温下,向一定浓度H2C2O4溶液中加入KOH(s),保持溶液体积和温度不变,测得pH与-lg X[X为 、
、 、
、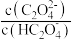 ]变化如图所示。下列说法错误的是
]变化如图所示。下列说法错误的是
 、
、 、
、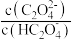 ]变化如图所示。下列说法错误的是
]变化如图所示。下列说法错误的是
A.常温下, 的 的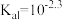 |
B.a点溶液中: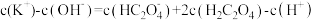 |
C. 溶液中: 溶液中: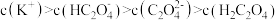 |
D.b点溶液中: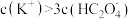 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
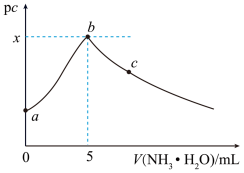
【推荐1】室温下,向10mL浓度均为0.1mol/L的CuCl2、FeCl2和ZnCl2溶液中分别滴加等浓度的Na2S溶液,滴加过程中pc[pc=-lgc(M2+),M2+为Cu2+或Fe2+或Zn2+]与Na2S溶液体积的关系如图所示。已知:Ksp(CuS)<Ksp(ZnS),Ksp(FeS)=6.25×10-18,lg25=1.4。下列说法正确的是
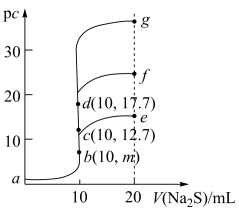

| A.m=8.6 |
| B.a点的CuCl2溶液中:2c(Cu2+)>c(Cl−)+c(OH−) |
| C.a→d→g的过程中,水的电离程度经历由大到小后又增大的过程 |
| D.将足量晶体ZnCl2加入0.1mol/L的Na2S溶液中,c(Zn2+)最大可达到10−24.4mol·L−1 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】已知常温下Ksp[Mg(OH)2]=3.2×10﹣11、Ksp[Fe(OH)3]=2.7×10﹣39,下列说法正确的是
| A.将10g氢氧化铁粉末加入100mL水中,充分搅拌后仍有固体剩余,静置后上层清液为饱和氢氧化铁溶液,c(OH﹣)=3×10﹣10mol/L |
| B.将10g氢氧化镁粉末加入100mL水中,充分搅拌后仍有固体剩余,静置后上层清液为饱和氢氧化镁溶液,加入酚酞试液后不能变红 |
| C.若1mol/L氯化镁溶液中混有氯化铁,调节pH=9,可以保证镁离子不沉淀而铁离子沉淀完全 |
| D.根据溶度积数据,可以计算出氢氧化铁固体与盐酸反应:Fe(OH)3+3H+⇌Fe3++3H2O的平衡常数为2.7×103 |
您最近一年使用:0次

 溶液滴定某二元弱酸
溶液滴定某二元弱酸 ,滴定过程中溶液的
,滴定过程中溶液的 、
、 的物质的量浓度变化如图所示。下列说法错误的是
的物质的量浓度变化如图所示。下列说法错误的是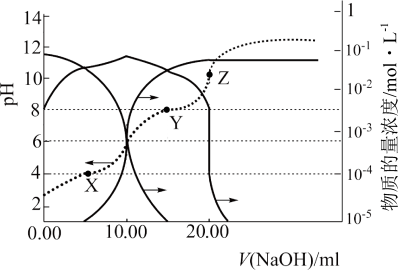
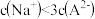

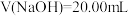 时,
时,
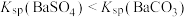 某温度下,饱和溶液中
某温度下,饱和溶液中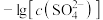 、
、 与
与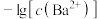 的关系如图所示。
的关系如图所示。
 的
的 值为
值为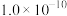
 固体可使溶液由a点变到b点
固体可使溶液由a点变到b点 时,两溶液中
时,两溶液中