关于硫酸工业中的催化氧化反应(2SO2+O2 2SO3 △H<0),可以用勒夏特列原理解的是
2SO3 △H<0),可以用勒夏特列原理解的是
 2SO3 △H<0),可以用勒夏特列原理解的是
2SO3 △H<0),可以用勒夏特列原理解的是| A.升温至450℃左右 | B.选择V2O5做催化剂 |
| C.选择常压条件 | D.通入过量氧气 |
更新时间:2022-02-18 19:59:37
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】下列实验操作、现象及所得出的结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 常温下,用pH计分别测定 溶液和 溶液和 溶液的pH 溶液的pH | 测得pH都等于7 | 同温下,不同浓度的 溶液中水的电离程度相同 溶液中水的电离程度相同 |
| B | 常温下,将锌片与铝片用导线连接后,插入浓硫酸中 | 锌片缓慢溶解,铝片上有气体产生 | 金属活泼性:铝<锌 |
| C | 向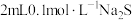 溶液中先后滴加2滴等浓度的 溶液中先后滴加2滴等浓度的 溶液和 溶液和 溶液 溶液 | 先有白色沉淀生成,后又有黑色沉淀 | 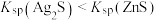 |
| D | 向两支盛有 5% 5% 溶液的试管中,分别加入 溶液的试管中,分别加入 的 的 溶液和 溶液和 蒸馏水 蒸馏水 | 加入 溶液的小试管中产生大量气泡,加入蒸馏水的小试管中无明显现象 溶液的小试管中产生大量气泡,加入蒸馏水的小试管中无明显现象 |  对 对 的分解起催化作用 的分解起催化作用 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法正确的是( )
| A.氢氧燃料电池工作时,H2在正极上失去电子 |
| B.铜在酸性条件下发生析氢腐蚀,在弱酸性或中性条件下发生吸氧腐蚀 |
C.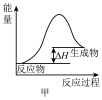 图甲表示燃料燃烧反应的能量变化 图甲表示燃料燃烧反应的能量变化 |
D.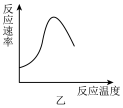 图乙表示酶催化反应的反应速率随反应温度的变化 图乙表示酶催化反应的反应速率随反应温度的变化 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】可逆反应:3A(g)⇌3B(?)+C(?)-Q,(Q>0). 随着温度升高,气体平均相对分子质量有变小趋势,则下列判断正确的是
| A.B和C可能都是固体 | B.B和C一定都是气体 |
| C.若C为固体,则B一定是气体 | D.B和C可能都是气体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】2X+Y 2Z(气)△H<0,温度升高,气体平均相对分子质量减小,说法正确的是
2Z(气)△H<0,温度升高,气体平均相对分子质量减小,说法正确的是
 2Z(气)△H<0,温度升高,气体平均相对分子质量减小,说法正确的是
2Z(气)△H<0,温度升高,气体平均相对分子质量减小,说法正确的是| A.X和Y可能都是固体 | B.X和Y一定都是气体 |
| C.若Y为固体,X一定是气体 | D.X和Y不可能都是气体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐3】在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中发生下述反应:PCl3(g)+Cl2(g) PCl5(g)。5min末达到平衡,有关数据如表:
PCl5(g)。5min末达到平衡,有关数据如表:
下列判断不正确的是
 PCl5(g)。5min末达到平衡,有关数据如表:
PCl5(g)。5min末达到平衡,有关数据如表:| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度(mol·L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol·L-1) | c1 | c2 | 0.4 |
| A.若升高温度,反应的平衡常数减小,则正反应为吸热反应 |
| B.反应5min内,v(PCl3)=0.08mol∙L-1∙min-1 |
| C.当容器中Cl2为1.2mol时,可逆反应达到平衡状态 |
| D.平衡后移去2.0molPCl3和1.0molCl2,相同条件再达平衡时,c(PCl5)<0.2mol·L-1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】恒容条件下, 发生如下反应:
发生如下反应: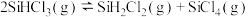 。已知:
。已知: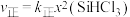 ,
,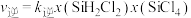 ,
, 、
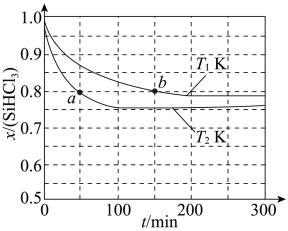
、 分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下
分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下 随时间的变化。下列说法正确的是
随时间的变化。下列说法正确的是
 发生如下反应:
发生如下反应: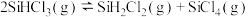 。已知:
。已知: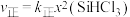 ,
,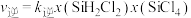 ,
, 、
、 分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下
分别为正、逆向反应速率常数(仅与温度有关),x为物质的量分数。如图是不同温度下 随时间的变化。下列说法正确的是
随时间的变化。下列说法正确的是
| A.该反应为放热反应 |
B.在b点充入 使体系压强增大,可缩短达到平衡的时间 使体系压强增大,可缩短达到平衡的时间 |
C.当反应进行到a处时, |
D.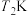 时平衡体系中再充入 时平衡体系中再充入 ,重新达到平衡时, ,重新达到平衡时,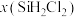 增大 增大 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】在一个固定体积的密闭容器中,加入 和
和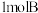 ,发生反应
,发生反应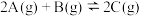 ,达到平衡时,C的物质的量浓度为
,达到平衡时,C的物质的量浓度为 ,若维持容器体积和温度不变,按下列配比作为起始物质,达到平衡后,C的物质的量浓度仍是
,若维持容器体积和温度不变,按下列配比作为起始物质,达到平衡后,C的物质的量浓度仍是 的是
的是
 和
和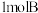 ,发生反应
,发生反应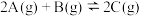 ,达到平衡时,C的物质的量浓度为
,达到平衡时,C的物质的量浓度为 ,若维持容器体积和温度不变,按下列配比作为起始物质,达到平衡后,C的物质的量浓度仍是
,若维持容器体积和温度不变,按下列配比作为起始物质,达到平衡后,C的物质的量浓度仍是 的是
的是A.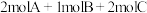 | B. |
C. | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
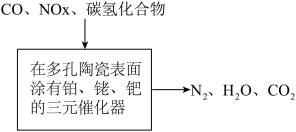
【推荐1】勒夏特列原理在化工和环保等领域有十分重要的应用。下列事实不能用勒夏特列原理解释的是( )
| A.夏天打开啤酒瓶,有许多气泡冒出 |
B.用饱和 溶液除去 溶液除去 中的 中的 蒸气 蒸气 |
| C.用水洗涤硫酸钡造成的损失量大于用稀硫酸造成的损失量 |
| D.硫酸工业中,二氧化硫转化为三氧化硫选用常压条件 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列操作或事实不能 用勒夏特列原理解释的是
A. ,把充有 ,把充有 的球浸泡在冰水中,气体颜色变浅 的球浸泡在冰水中,气体颜色变浅 |
| B.打开碳酸饮料瓶盖时,会有气泡冒出 |
| C.合成氨工业中,采用高温有利于提高生产效率 |
D.向含有 的红色溶液中加入铁粉,振荡,溶液颜色变浅或褪去 的红色溶液中加入铁粉,振荡,溶液颜色变浅或褪去 |
您最近一年使用:0次

 化合制备硫酸,已知
化合制备硫酸,已知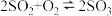
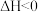 ,下列的说法正确的是
,下列的说法正确的是 ,任何温度下均可以自发反应
,任何温度下均可以自发反应 ,说明反应达到了平衡状态
,说明反应达到了平衡状态

