已知室温时:K1(H2C2O4)=6×10-2,K2(H2C2O4)=6.4×10-5,Kp(Ag2C2O4)=5×10-12,K(AgCl)=1.8×10-10。向20mL0.02mol/L的Na2C2O4溶液中滴加0.02mol/L的盐酸,相关图象如下所示。下列说法错误的是
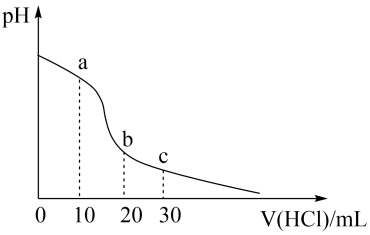

| A.a点溶液显酸性 |
| B.a点溶液滴加0.01mol/L硝酸银溶液,先产生AgCl沉淀 |
C.c点溶液中c(Na+)>4c(HC2O )+8c(C2O )+8c(C2O ) ) |
| D.水电离程度:a>b>c |
更新时间:2022-04-08 16:53:39
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度时,水的离子积为1.0×10-14,由此可知在该温度时水的电离度为
| A.1.8×10-7% | B.1.0×10-2% | C.1.8×10-9% | D.1.8×10-14% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设NA为阿伏加德罗常数值。下列说法不正确的是
A. 的 的 中,含有0.6 NA个中子 中,含有0.6 NA个中子 |
B.含NA个 的 的 溶解于 溶解于 水中, 水中, 的物质的量浓度为 的物质的量浓度为 |
C.常温下,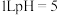 的 的 溶液中水电离的 溶液中水电离的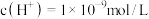 |
D.电解足量的 溶液,当标况下阳极产生 溶液,当标况下阳极产生 气体时,转移电子数目为2NA 气体时,转移电子数目为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列说法正确的是
A.常温下,0.1mol·L-1CH3COONa溶液加水稀释后,溶液中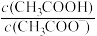 的值增大 的值增大 |
| B.常温下,等物质的量浓度的CH3COOH溶液和HCl溶液中,水的电离程度相同 |
| C.常温下,反应NH3(g)+HCl(g)=NH4Cl(s)能自发发生反应,则该反应的∆H>0 |
D.常温下,向BaCO3、BaSO4 的饱和溶液中加入少量BaCl2固体,溶液中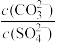 减小 减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下浓度均为0.1mol/L的NaOH溶液和氨水,下列说法正确的是
| A.两种溶液的pH值相同 |
B.氨水的电离方程式为:NH3·H2O=NH +OH- +OH- |
| C.分别取等体积的两溶液加水稀释100倍后,氨水的pH值更大 |
| D.等体积的两溶液,分别加入同浓度的盐酸至溶液呈中性,消耗盐酸的体积前者大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】乙二胺( ,缩写为EDA)为二元弱碱,在水中的电离方式与氨类似,即
,缩写为EDA)为二元弱碱,在水中的电离方式与氨类似,即
 、
、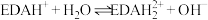 。常温下,向
。常温下,向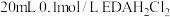 溶液中加入NaOH固体(忽略溶液体积变化),溶液中
溶液中加入NaOH固体(忽略溶液体积变化),溶液中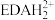 、
、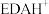 、EDA三种粒子浓度的对数值
、EDA三种粒子浓度的对数值 、所加入NaOH固体的质量与pOH的关系如图所示,下列说法错误的是
、所加入NaOH固体的质量与pOH的关系如图所示,下列说法错误的是

 ,缩写为EDA)为二元弱碱,在水中的电离方式与氨类似,即
,缩写为EDA)为二元弱碱,在水中的电离方式与氨类似,即
 、
、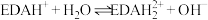 。常温下,向
。常温下,向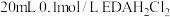 溶液中加入NaOH固体(忽略溶液体积变化),溶液中
溶液中加入NaOH固体(忽略溶液体积变化),溶液中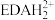 、
、 、EDA三种粒子浓度的对数值
、EDA三种粒子浓度的对数值 、所加入NaOH固体的质量与pOH的关系如图所示,下列说法错误的是
、所加入NaOH固体的质量与pOH的关系如图所示,下列说法错误的是
A.乙二胺第二步电离常数的数量级为 |
B. 时, 时,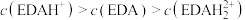 |
C. 时, 时,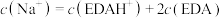 |
D. 时,加入NaOH固体的质量 时,加入NaOH固体的质量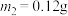 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25℃时,下列有关电解质溶液的说法错误的是
| A.pH=9.25、浓度均为0.1 mol•L-1的NH4C1、NH3·H2O混合溶液:c(NH4+)+c(H+) >c(NH3·H2O)+c(OH-) |
| B.0.1mol/LH2SO4溶液与0.1mol/LNaOH溶液等体积混合:c(H+)=c(SO42-)+c(OH-) |
| C.向0.1 mol•L-1NaHSO3溶液中通NH3至pH=7: c(Na+)> c(NH4+)>c(SO32-) |
| D.CO2通入KOH溶液,当由水电离的H+浓度为10-7mol/L,一定存在:c(K+)=2c(CO32-)+c(HCO3-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】室温下, 溶液的
溶液的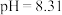 ,有关该溶液的判断正确的是
,有关该溶液的判断正确的是
 溶液的
溶液的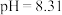 ,有关该溶液的判断正确的是
,有关该溶液的判断正确的是A. |
B.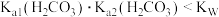 |
C. |
D.加入适量NaOH溶液后: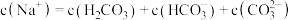 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】温度为t ℃时,向10 mL 1.0 mol·L−1盐酸中,逐滴滴入浓度为x mol·L−1的氨水,随着氨水的不断加入,溶液的温度变化曲线(曲线Ⅰ)和pH变化曲线(曲线Ⅱ)如图所示。下列有关判断正确的是
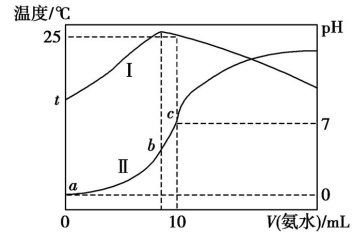

| A.x=1.0 |
| B.b点时,水的电离程度最小 |
C.b点时,c( )>c(Cl−)>c(H+)>c(OH−) )>c(Cl−)>c(H+)>c(OH−) |
D.假设混合液的体积等于两种溶液体积之和,c点时,c(NH3·H2O)= 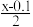 mol·L−1 mol·L−1 |
您最近一年使用:0次


 、
、
 、
、 氨水加水稀释后,溶液中
氨水加水稀释后,溶液中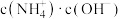 变大
变大 是强酸还是弱酸,可测
是强酸还是弱酸,可测 溶液的
溶液的 。若
。若 ,则
,则 ,则
,则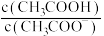 变大
变大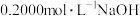 标准溶液滴定
标准溶液滴定 与
与 ),至中性时,溶液中的酸未被完全中和
),至中性时,溶液中的酸未被完全中和 、
、 、
、 、
、
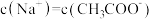 时:
时: 、
、 、
、 、
、
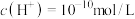 的溶液:
的溶液:
 、
、 、
、
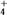 ):③<①
):③<①

