氨是重要的基础化工原料,工业上常用于制备氨水、亚硝酸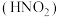 、连二次硝酸
、连二次硝酸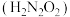 、尿素
、尿素 等多种含氮的化工产品。
等多种含氮的化工产品。
(1)已知: 时,连二次硝酸
时,连二次硝酸 的电离常数为
的电离常数为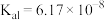 、
、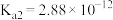 ;往
;往 溶液中滴加氢氧化钠溶液至
溶液中滴加氢氧化钠溶液至 ,
, 、
、 、离子浓度由大到小的顺序为
、离子浓度由大到小的顺序为___________ 。
(2)常温下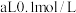 的
的 和
和 的
的 混合,混合后溶液呈中性,
混合,混合后溶液呈中性, 的电离常数为
的电离常数为___________ (用含a、b的式子表示)
(3)向浓度均为 的
的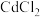 和
和 混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成两种沉淀,则溶液中
混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成两种沉淀,则溶液中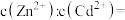
___________ 。[已知: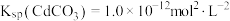 ,
,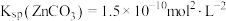 ]
]
可乐中的食品添加剂有白砂糖、二氧化碳、焦糖色、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为 ,沸点高难挥发)有一定关系。
,沸点高难挥发)有一定关系。
(4)羟基磷灰石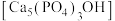 是牙釉质的主要成分,在唾液中存在平衡:
是牙釉质的主要成分,在唾液中存在平衡: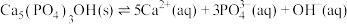 。长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:
。长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:___________
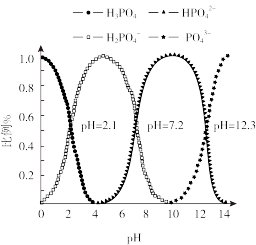
(5)常温下,向磷酸溶液中滴加 溶液,含磷微粒的分布比例与
溶液,含磷微粒的分布比例与 的关系如图所示。
的关系如图所示。 溶液显酸性,下列有关分析正确的是___________。
溶液显酸性,下列有关分析正确的是___________。
(6)联氨(又称联肼, 无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离的方程式为:
无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离的方程式为:____________ 平衡常数值为___________ (已知: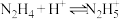 的
的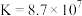 ;
;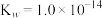 )。
)。
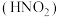 、连二次硝酸
、连二次硝酸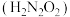 、尿素
、尿素 等多种含氮的化工产品。
等多种含氮的化工产品。(1)已知:
 时,连二次硝酸
时,连二次硝酸 的电离常数为
的电离常数为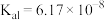 、
、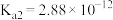 ;往
;往 溶液中滴加氢氧化钠溶液至
溶液中滴加氢氧化钠溶液至 ,
, 、
、 、离子浓度由大到小的顺序为
、离子浓度由大到小的顺序为(2)常温下
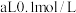 的
的 和
和 的
的 混合,混合后溶液呈中性,
混合,混合后溶液呈中性, 的电离常数为
的电离常数为(3)向浓度均为
 的
的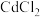 和
和 混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成两种沉淀,则溶液中
混合液中滴加碳酸铵溶液,当加入碳酸铵溶液至生成两种沉淀,则溶液中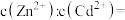
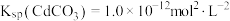 ,
,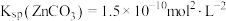 ]
]可乐中的食品添加剂有白砂糖、二氧化碳、焦糖色、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为
 ,沸点高难挥发)有一定关系。
,沸点高难挥发)有一定关系。(4)羟基磷灰石
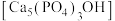 是牙釉质的主要成分,在唾液中存在平衡:
是牙釉质的主要成分,在唾液中存在平衡: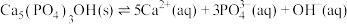 。长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:
。长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:(5)常温下,向磷酸溶液中滴加
 溶液,含磷微粒的分布比例与
溶液,含磷微粒的分布比例与 的关系如图所示。
的关系如图所示。 溶液显酸性,下列有关分析正确的是___________。
溶液显酸性,下列有关分析正确的是___________。
A.溶液中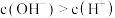 |
B. 的电离程度大于其水解程度 的电离程度大于其水解程度 |
C. c(Na+)+ c(H+)=c(H2PO )+2c(HPO )+2c(HPO )+3c(PO )+3c(PO )+c(OH—) )+c(OH—) |
| D.溶液中水的电离程度比纯水大 |
(6)联氨(又称联肼,
 无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离的方程式为:
无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离的方程式为: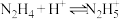 的
的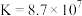 ;
;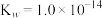 )。
)。
更新时间:2022-04-05 18:50:15
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】回答下列问题:
(1)常温下,向20 mL 0.010 mol·L-1的HA溶液中逐滴加入0.010 mol·L-1的NaOH溶液,溶液中lg c(OH-)与所加NaOH溶液的体积(V)的关系如图。
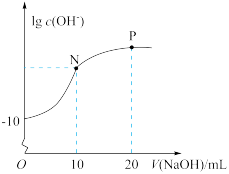
HA是__________ (“强酸”或“弱酸”)。N点溶液中2c(H+)-2c(OH-)=____________ (用含A微粒的符号表示)
(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数δ(X)= ,X为HClO或ClO-与pH的关系如图所示。HClO的电离常数Ka值为
,X为HClO或ClO-与pH的关系如图所示。HClO的电离常数Ka值为__________ 。常温下向0.1 mol·L-1的HClO溶液中加入等体积的0.1mol·L-1的NaOH溶液后,c(ClO-)+c(HClO)=__________ mol·L-1。
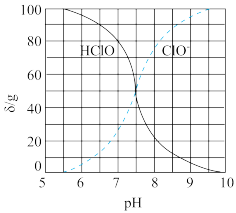
(3)PH相同、等体积的两份溶液A(盐酸)和B(CH3COOH)分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是____ (填序号)。
①反应所需要的时间B>A ②开始反应时的速率A>B
③参加反应的锌的物质的量A=B ④反应过程的平均速率B>A
⑤A中有锌剩余 ⑥B中有锌剩余
(4)已知草酸为二元弱酸:H2C2O4 HC2O
HC2O +H+ Ka1,HC2O
+H+ Ka1,HC2O
 C2O
C2O +H+ Ka2,常温下,向某浓度的H2C2O4溶液中逐滴加入一定浓度的KOH溶液,所得溶液中H2C2O4、HC2O
+H+ Ka2,常温下,向某浓度的H2C2O4溶液中逐滴加入一定浓度的KOH溶液,所得溶液中H2C2O4、HC2O 、C2O
、C2O 三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。
三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。
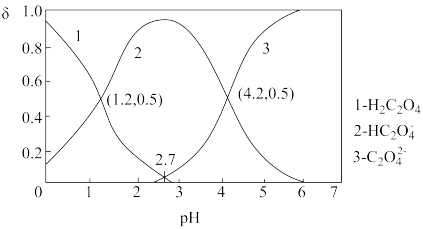
①则常温下0.1 mol/L的NaHC2O4溶液显_________ 填酸性、碱性或中性)
②pH=2.7时,溶液中 =
=______ 。
(1)常温下,向20 mL 0.010 mol·L-1的HA溶液中逐滴加入0.010 mol·L-1的NaOH溶液,溶液中lg c(OH-)与所加NaOH溶液的体积(V)的关系如图。

HA是
(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数δ(X)=
 ,X为HClO或ClO-与pH的关系如图所示。HClO的电离常数Ka值为
,X为HClO或ClO-与pH的关系如图所示。HClO的电离常数Ka值为
(3)PH相同、等体积的两份溶液A(盐酸)和B(CH3COOH)分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是
①反应所需要的时间B>A ②开始反应时的速率A>B
③参加反应的锌的物质的量A=B ④反应过程的平均速率B>A
⑤A中有锌剩余 ⑥B中有锌剩余
(4)已知草酸为二元弱酸:H2C2O4
 HC2O
HC2O +H+ Ka1,HC2O
+H+ Ka1,HC2O
 C2O
C2O +H+ Ka2,常温下,向某浓度的H2C2O4溶液中逐滴加入一定浓度的KOH溶液,所得溶液中H2C2O4、HC2O
+H+ Ka2,常温下,向某浓度的H2C2O4溶液中逐滴加入一定浓度的KOH溶液,所得溶液中H2C2O4、HC2O 、C2O
、C2O 三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。
三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。
①则常温下0.1 mol/L的NaHC2O4溶液显
②pH=2.7时,溶液中
 =
=
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】雌黄( )和雄黄(
)和雄黄( )都是自然界中常见的砷化合物,早期曾用作绘画颜料,因都有抗病毒疗效而入药。
)都是自然界中常见的砷化合物,早期曾用作绘画颜料,因都有抗病毒疗效而入药。
(1) 可转化为用于治疗白血病的亚砷酸(
可转化为用于治疗白血病的亚砷酸( )。亚砷酸在溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液
)。亚砷酸在溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液 关系如图(a)所示。
关系如图(a)所示。
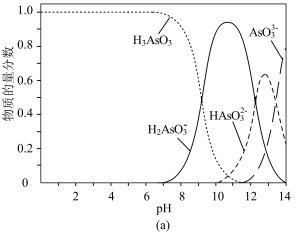
①人体血液的 为7.35~7.45,用药后人体中含砷元素的主要微粒是
为7.35~7.45,用药后人体中含砷元素的主要微粒是_______ 。
②将 溶液滴入亚砷酸溶液,当
溶液滴入亚砷酸溶液,当 调至11时,所发生反应的离子方程式是
调至11时,所发生反应的离子方程式是_______ 。
③下列说法中,正确的是_______ (填字母序号)。
a.当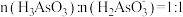 时,溶液呈碱性
时,溶液呈碱性
b. 时,溶液中
时,溶液中
c.在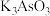 溶液中,
溶液中, 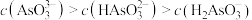
(2)工业含砷(Ⅲ)废水常用铁盐处理后排放。其原理是:铁盐混凝剂在溶液中产生 胶粒,其表面带有正电荷,可吸附含砷化合物。测得不同
胶粒,其表面带有正电荷,可吸附含砷化合物。测得不同 条件下铁盐对含砷(Ⅲ)化合物的去除率,如图(b)所示。
条件下铁盐对含砷(Ⅲ)化合物的去除率,如图(b)所示。 为5~9时,随溶液
为5~9时,随溶液 增大,铁盐混凝剂对含砷(Ⅲ)化合物的吸附效果增强。结合图(a)和图(b),解释可能的原因:
增大,铁盐混凝剂对含砷(Ⅲ)化合物的吸附效果增强。结合图(a)和图(b),解释可能的原因:_______ 。

 )和雄黄(
)和雄黄( )都是自然界中常见的砷化合物,早期曾用作绘画颜料,因都有抗病毒疗效而入药。
)都是自然界中常见的砷化合物,早期曾用作绘画颜料,因都有抗病毒疗效而入药。(1)
 可转化为用于治疗白血病的亚砷酸(
可转化为用于治疗白血病的亚砷酸( )。亚砷酸在溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液
)。亚砷酸在溶液中存在多种微粒形态,各种微粒的物质的量分数与溶液 关系如图(a)所示。
关系如图(a)所示。
①人体血液的
 为7.35~7.45,用药后人体中含砷元素的主要微粒是
为7.35~7.45,用药后人体中含砷元素的主要微粒是②将
 溶液滴入亚砷酸溶液,当
溶液滴入亚砷酸溶液,当 调至11时,所发生反应的离子方程式是
调至11时,所发生反应的离子方程式是③下列说法中,正确的是
a.当
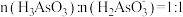 时,溶液呈碱性
时,溶液呈碱性b.
 时,溶液中
时,溶液中
c.在
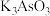 溶液中,
溶液中, 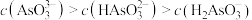
(2)工业含砷(Ⅲ)废水常用铁盐处理后排放。其原理是:铁盐混凝剂在溶液中产生
 胶粒,其表面带有正电荷,可吸附含砷化合物。测得不同
胶粒,其表面带有正电荷,可吸附含砷化合物。测得不同 条件下铁盐对含砷(Ⅲ)化合物的去除率,如图(b)所示。
条件下铁盐对含砷(Ⅲ)化合物的去除率,如图(b)所示。 为5~9时,随溶液
为5~9时,随溶液 增大,铁盐混凝剂对含砷(Ⅲ)化合物的吸附效果增强。结合图(a)和图(b),解释可能的原因:
增大,铁盐混凝剂对含砷(Ⅲ)化合物的吸附效果增强。结合图(a)和图(b),解释可能的原因:
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】(1)将NaHCO3溶液跟Al2(SO4)3溶液混合,相关反应的离子方程式是____________ 。
(2)有浓度均为0.2 mol·L-1的Na2CO3溶液与NaHCO3溶液,试回答下列问题:
①微粒种类 :Na2CO3__________ NaHCO3溶液(填“﹥”、“<”或“=”)。
②两溶液分别加入0.1 molNaOH固体,恢复到室温,Na2CO3溶液中的c(CO32-)____________ (填“增大”、“减小”或“不变”);NaHCO3溶液中的c(HCO3-)_________ (填“增大”、“减小”或“不变”)。
(3)常温下,甲为0.1 mol·L-1的HA溶液,pH﹥1;乙为0.1 mol·L-1的BOH溶液,且溶液中c(OH-):c(H+)=1012。请分别写出甲、乙两溶液中溶质的电离方程式:
甲__________________ 、乙_________________ 。
(4)相同条件下,对于浓度均为0.1 mol·L-1的NaCl溶液和CH3COONa溶液,溶液中的离子总数:NaCl溶液__________ CH3COONa溶液(填“﹥”、“<”或“=”)。
(5)物质的量浓度相同的 ①氨水 ②氯化铵 ③碳酸氢铵 ④硫酸氢铵 ⑤硫酸铵五种溶液中c(NH4+)由大到小的顺序为__________________ 。
(2)有浓度均为0.2 mol·L-1的Na2CO3溶液与NaHCO3溶液,试回答下列问题:
①
②两溶液分别加入0.1 molNaOH固体,恢复到室温,Na2CO3溶液中的c(CO32-)
(3)常温下,甲为0.1 mol·L-1的HA溶液,pH﹥1;乙为0.1 mol·L-1的BOH溶液,且溶液中c(OH-):c(H+)=1012。请分别写出甲、乙两溶液中溶质的电离方程式:
甲
(4)相同条件下,对于浓度均为0.1 mol·L-1的NaCl溶液和CH3COONa溶液,溶液中的离子总数:NaCl溶液
(5)物质的量浓度相同的 ①氨水 ②氯化铵 ③碳酸氢铵 ④硫酸氢铵 ⑤硫酸铵五种溶液中c(NH4+)由大到小的顺序为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】弱电解质有许多,如:醋酸、碳酸、氢氰酸、一水合氨、氢氧化铝、氢氧化铜等。 时,醋酸、碳酸、氢氰酸的电离平衡常数如下表:
时,醋酸、碳酸、氢氰酸的电离平衡常数如下表:
(1) 时,pH相等的三种溶液①
时,pH相等的三种溶液① 溶液、②
溶液、② 溶液、③
溶液、③ 溶液,浓度由大到小的顺序为
溶液,浓度由大到小的顺序为___________ (填序号)。
(2) 时,向
时,向 溶液中通入少量
溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(3)将浓度为 的
的 与
与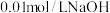 溶液等体积混合,充分反应后混合溶液中
溶液等体积混合,充分反应后混合溶液中
__________ 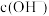 ( “大于”、 “等于”或 “小于”),结合所学知识与必要数据,解释原因:
( “大于”、 “等于”或 “小于”),结合所学知识与必要数据,解释原因:__________ 。
(4)用蒸馏水稀释 的醋酸,下列各式表示的数值随水量的增加而增大的是_____
的醋酸,下列各式表示的数值随水量的增加而增大的是_____
 时,醋酸、碳酸、氢氰酸的电离平衡常数如下表:
时,醋酸、碳酸、氢氰酸的电离平衡常数如下表:| 化学式 | 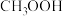 |  |  |
| 电离平衡常数 |  | 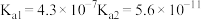 |  |
 时,pH相等的三种溶液①
时,pH相等的三种溶液① 溶液、②
溶液、② 溶液、③
溶液、③ 溶液,浓度由大到小的顺序为
溶液,浓度由大到小的顺序为(2)
 时,向
时,向 溶液中通入少量
溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为(3)将浓度为
 的
的 与
与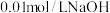 溶液等体积混合,充分反应后混合溶液中
溶液等体积混合,充分反应后混合溶液中
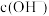 ( “大于”、 “等于”或 “小于”),结合所学知识与必要数据,解释原因:
( “大于”、 “等于”或 “小于”),结合所学知识与必要数据,解释原因:(4)用蒸馏水稀释
 的醋酸,下列各式表示的数值随水量的增加而增大的是_____
的醋酸,下列各式表示的数值随水量的增加而增大的是_____A. | B. | C.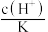 | D. |
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】研究硫元素及其化合物的性质具有重要意义。
(1)25℃,向0.10mol/LH2S溶液中通入HCl气体或加入NaOH固体调节溶液的pH,溶液的pH与c(S2-)的关系如图所示(忽略溶液体积的变化、H2S的挥发)。
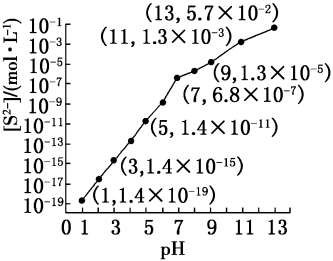
①pH=13时,溶液中的c(H2S)+c(HS-)=___ mol/L。
②pH=7时,c(Na+)___ c(H2S)+c(HS-)+c(S2-)(填“>”、“<”或“=”)。[已知:Ka1(H2S)=1.1×10-7,Ka2(H2S)=1.3×10-13]
③某溶液含0.0040mol/LMn2+、0.0040mol/LFe2+、0.10mol/LH2S,当溶液pH=___ 时,Fe2+开始沉淀;当Fe2+完全沉淀时,溶液中Mn2+___ (填“是”或“否”)生成沉淀。[已知:Ksp(FeS)=5.6×10-18,Ksp(MnS)=2.8×10-13]
(2)25℃,两种酸的电离平衡常数如表。
①将SO2通入0.10mol/LNaOH溶液,当pH=8时溶液中离子浓度由大到小的顺序为___ 。
②将少量SO2通入过量的Na2CO3溶液中反应的离子方程式为___ 。
(1)25℃,向0.10mol/LH2S溶液中通入HCl气体或加入NaOH固体调节溶液的pH,溶液的pH与c(S2-)的关系如图所示(忽略溶液体积的变化、H2S的挥发)。

①pH=13时,溶液中的c(H2S)+c(HS-)=
②pH=7时,c(Na+)
③某溶液含0.0040mol/LMn2+、0.0040mol/LFe2+、0.10mol/LH2S,当溶液pH=
(2)25℃,两种酸的电离平衡常数如表。
| Ka1 | Ka2 | |
| H2SO3 | 1.4×10-2 | 6.0×10-8 |
| H2CO3 | 4.5×10-7 | 4.7×10-11 |
①将SO2通入0.10mol/LNaOH溶液,当pH=8时溶液中离子浓度由大到小的顺序为
②将少量SO2通入过量的Na2CO3溶液中反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】结合下表回答下列问题(均为常温下的数据):
(1)同浓度的 、
、 、
、 、
、 、
、 、
、 中结合
中结合 的能力最弱的是
的能力最弱的是_______ 。
(2)下列反应可以发生的是_______ (填序号)
a.
b.
c.
(3) 的
的 溶液与
溶液与 的KOH的溶液等体积混合后所得溶液呈
的KOH的溶液等体积混合后所得溶液呈_______ 性,请用计算数据说明:_______ 。
(4)pH相同的NaClO和 溶液,其溶液的物质的量浓度的大小关系是
溶液,其溶液的物质的量浓度的大小关系是
_______ NaClO,两溶液中:
_______ 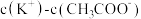 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(5)向
 溶液中滴加NaOH溶液至
溶液中滴加NaOH溶液至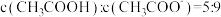 ,此时溶液
,此时溶液
_______ 。
| 酸 | 电力常数( ) ) |
 |  |
| HClO |  |
 | 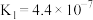 ; ; |
 | 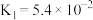 ; ; |
 |  ; ; |
(1)同浓度的
 、
、 、
、 、
、 、
、 、
、 中结合
中结合 的能力最弱的是
的能力最弱的是(2)下列反应可以发生的是
a.

b.

c.

(3)
 的
的 溶液与
溶液与 的KOH的溶液等体积混合后所得溶液呈
的KOH的溶液等体积混合后所得溶液呈(4)pH相同的NaClO和
 溶液,其溶液的物质的量浓度的大小关系是
溶液,其溶液的物质的量浓度的大小关系是

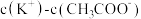 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(5)向

 溶液中滴加NaOH溶液至
溶液中滴加NaOH溶液至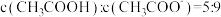 ,此时溶液
,此时溶液
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】 常用作陶瓷材料,可由锆英砂(主要成分为
常用作陶瓷材料,可由锆英砂(主要成分为 ,也可表示为
,也可表示为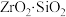 ,还含少量
,还含少量 等杂质)通过如图方法制取。
等杂质)通过如图方法制取。

已知:① 能与烧碱反应生成可溶于水的
能与烧碱反应生成可溶于水的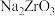 ,
,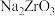 与酸反应生成
与酸反应生成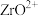 。
。
②部分金属离子在实验条件下开始沉淀和完全沉淀的 如表。
如表。
(1)熔融时 发生反应的化学方程式为
发生反应的化学方程式为_______ ,滤渣Ⅰ的化学式为_______ 。
(2)滤液Ⅰ中除 外还含金属的阳离子有
外还含金属的阳离子有_______ ,为使滤液Ⅰ的杂质离子沉淀完全,需用氨水调 ,则a的范围是
,则a的范围是_______ 。
(3)继续加氨水至 时,所发生反应的离子方程式为
时,所发生反应的离子方程式为_______ 。
(4)向过滤Ⅲ所得滤液中加入 粉末并加热,得到两种气体。该反应的离子方程式为
粉末并加热,得到两种气体。该反应的离子方程式为_______ 。
(5)为得到纯净的 ,
,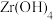 需要洗涤,检验
需要洗涤,检验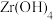 是否洗涤干净的方法是
是否洗涤干净的方法是_______ 。
 常用作陶瓷材料,可由锆英砂(主要成分为
常用作陶瓷材料,可由锆英砂(主要成分为 ,也可表示为
,也可表示为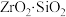 ,还含少量
,还含少量 等杂质)通过如图方法制取。
等杂质)通过如图方法制取。
已知:①
 能与烧碱反应生成可溶于水的
能与烧碱反应生成可溶于水的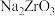 ,
,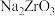 与酸反应生成
与酸反应生成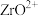 。
。②部分金属离子在实验条件下开始沉淀和完全沉淀的
 如表。
如表。| 金属离子 |  | 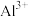 | 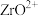 |
开始沉淀时 | 1.9 | 3.3 | 6.2 |
沉淀完全时 | 3.2 | 5.2 | 8.0 |
 发生反应的化学方程式为
发生反应的化学方程式为(2)滤液Ⅰ中除
 外还含金属的阳离子有
外还含金属的阳离子有 ,则a的范围是
,则a的范围是(3)继续加氨水至
 时,所发生反应的离子方程式为
时,所发生反应的离子方程式为(4)向过滤Ⅲ所得滤液中加入
 粉末并加热,得到两种气体。该反应的离子方程式为
粉末并加热,得到两种气体。该反应的离子方程式为(5)为得到纯净的
 ,
,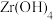 需要洗涤,检验
需要洗涤,检验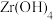 是否洗涤干净的方法是
是否洗涤干净的方法是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】实验小组对Mg与NH4Cl溶液的反应进行探究。
(1)用pH计测定1.0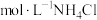 溶液约为4.6,分析NH4Cl溶液呈酸性的原因
溶液约为4.6,分析NH4Cl溶液呈酸性的原因______ (用化学用语表示)。
(2)探究镁与NH4Cl溶液的反应:实验Ⅰ、Ⅱ所取镁粉质量均为0.5g,分别加入选取的实验试剂中。
①实验Ⅰ中发生反应的化学方程式为______ 。
②经检验实验Ⅱ中刺激性气味气体为NH3和H2的混合气体,用平衡移动原理解释产生NH3的原因______ 。
③已知灰白色沉淀中含有Mg2+、OH-。为研究固体成分,进行实验:将生成的灰白色固体洗涤数次,至洗涤液中滴加AgNO3溶液后无明显浑浊。将洗涤后的固体溶于稀HNO3,再滴加AgNO3溶液,出现白色沉淀。推测沉淀中含有______ ,灰白色固体可能是______ (填化学式)。
④针对实验Ⅱ比实验Ⅰ反应剧烈的原因,小组同学提出了两种假设:
假设l:NH4Cl溶液中的H+溶解了Mg(OH)2;
假设2:NH4Cl溶液中的 溶解了Mg(OH)2。
溶解了Mg(OH)2。
为证明假设的合理性.小组同学做了如下对比实验:
实验结论是______ 。
(3)甲同学通过深入思考,认为Mg与NH4Cl溶液反应剧烈.可能还与 有关.并通过设计实验,证明了猜想的正确性.他设计的实验方案和实验证据为
有关.并通过设计实验,证明了猜想的正确性.他设计的实验方案和实验证据为______ 。
(4)由上述实验得出的结论是______ 。
(1)用pH计测定1.0
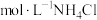 溶液约为4.6,分析NH4Cl溶液呈酸性的原因
溶液约为4.6,分析NH4Cl溶液呈酸性的原因(2)探究镁与NH4Cl溶液的反应:实验Ⅰ、Ⅱ所取镁粉质量均为0.5g,分别加入选取的实验试剂中。
实验 | 实验试剂 | 实验现象 |
Ⅰ | 5mL蒸馏水 | 反应缓慢,有少量气泡产生(经检验为H2) |
Ⅱ | 5mL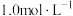 NH4Cl溶液(pH=4.6) | 剧烈反应,产生刺激性气味气体和灰白色难溶固体 |
②经检验实验Ⅱ中刺激性气味气体为NH3和H2的混合气体,用平衡移动原理解释产生NH3的原因
③已知灰白色沉淀中含有Mg2+、OH-。为研究固体成分,进行实验:将生成的灰白色固体洗涤数次,至洗涤液中滴加AgNO3溶液后无明显浑浊。将洗涤后的固体溶于稀HNO3,再滴加AgNO3溶液,出现白色沉淀。推测沉淀中含有
④针对实验Ⅱ比实验Ⅰ反应剧烈的原因,小组同学提出了两种假设:
假设l:NH4Cl溶液中的H+溶解了Mg(OH)2;
假设2:NH4Cl溶液中的
 溶解了Mg(OH)2。
溶解了Mg(OH)2。为证明假设的合理性.小组同学做了如下对比实验:
实验 | 实验方案 | 实验现象 |
Ⅲ | 取2根覆盖了Mg(OH)2的Mg条,分别同时放入相同体积相同pH的盐酸和饱和NH4Cl溶液中。 | 饱和NH4Cl溶液中反应更剧烈。 |
Ⅳ | 向饱和NH4Cl溶液中滴加浓氨水,使溶液呈中性或略显碱性,再放入覆盖了Mg(OH)2的镁条。 | 剧烈反应,但是比实验Ⅲ饱和NH4Cl溶液略慢,产生刺激性气味气体和灰白色难溶固体。 |
(3)甲同学通过深入思考,认为Mg与NH4Cl溶液反应剧烈.可能还与
 有关.并通过设计实验,证明了猜想的正确性.他设计的实验方案和实验证据为
有关.并通过设计实验,证明了猜想的正确性.他设计的实验方案和实验证据为(4)由上述实验得出的结论是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】I.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过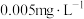 。处理含镉废水可采用化学沉淀法。
。处理含镉废水可采用化学沉淀法。
(1)写出磷酸镉[ ]沉淀溶解平衡常数的表达式:
]沉淀溶解平衡常数的表达式: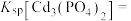
_______ 。
(2)一定温度下, 的
的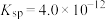 ,
, 的
的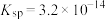 ,该温度下
,该温度下_______ [填“ ”或“
”或“ ”]的饱和溶液中
”]的饱和溶液中 浓度较大。
浓度较大。
(3)向某含镉废水中加入 ,当
,当 浓度达到
浓度达到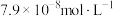 时,废水中
时,废水中 的浓度为
的浓度为____  [已知:
[已知: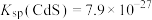 ],此时
],此时____ (填“符合”或“不符合”)《生活饮用水卫生标准》。
II.根据题目提供的溶度积数据进行计算并回答下列问题:
(4)已知25℃时,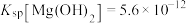 ;酸碱指示剂百里酚蓝变色的pH范围如下:
;酸碱指示剂百里酚蓝变色的pH范围如下:
25℃时,向 饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为
饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为_______ 。
(5)常温下,向50mL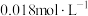 的
的 溶液中加入50mL
溶液中加入50mL 的盐酸,生成沉淀。已知该温度下,
的盐酸,生成沉淀。已知该温度下, ,忽略溶液体积的变化。
,忽略溶液体积的变化。
①反应后,溶液中
_______  。
。
②反应后,溶液的
_______ 。
③如果向反应后的溶液中继续加入50mL 的盐酸,
的盐酸,____ (填“有”或“无”)白色沉淀生成。
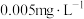 。处理含镉废水可采用化学沉淀法。
。处理含镉废水可采用化学沉淀法。(1)写出磷酸镉[
 ]沉淀溶解平衡常数的表达式:
]沉淀溶解平衡常数的表达式: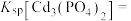
(2)一定温度下,
 的
的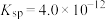 ,
, 的
的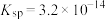 ,该温度下
,该温度下 ”或“
”或“ ”]的饱和溶液中
”]的饱和溶液中 浓度较大。
浓度较大。(3)向某含镉废水中加入
 ,当
,当 浓度达到
浓度达到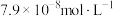 时,废水中
时,废水中 的浓度为
的浓度为 [已知:
[已知: ],此时
],此时II.根据题目提供的溶度积数据进行计算并回答下列问题:
(4)已知25℃时,
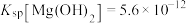 ;酸碱指示剂百里酚蓝变色的pH范围如下:
;酸碱指示剂百里酚蓝变色的pH范围如下:| pH |  | 8.0~9.6 | 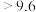 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
 饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为
饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为(5)常温下,向50mL
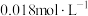 的
的 溶液中加入50mL
溶液中加入50mL 的盐酸,生成沉淀。已知该温度下,
的盐酸,生成沉淀。已知该温度下, ,忽略溶液体积的变化。
,忽略溶液体积的变化。①反应后,溶液中

 。
。②反应后,溶液的

③如果向反应后的溶液中继续加入50mL
 的盐酸,
的盐酸,
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐1】按要求填空
(1)KAl(SO4)2·12H2O可做净水剂,其原理是(用离子方程式表示)___________ 。
(2)将体积相等的NaOH稀溶液和CH3COOH稀溶液充分混合后,若溶液中c(Na+)=c(CH3COO-),则混合前c(NaOH)___________ (填“ ”“
”“ ”或“
”或“ ”)c(CH3COOH)。
”)c(CH3COOH)。
(3)将AgCl分别放入①5mL H2O、②10mL 0.2mol/L MgCl2溶液、③20mL 0.5mol/L AgNO3溶液、④40mL 0.1mol/L HCl溶液中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是___________ (用序号填空)。
(4)常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合,若溶液呈中性则CH3COOH的电离平衡常数Ka=___________ 。
(5)室温下,1mol/L相同体积的下列四种溶液①BaCl2、②FeCl3、③HF、④Na2CO3所含阳离子数由少到多的顺序是(用序号填空)___________ 。
(6)标准状况下,将2.24L CO2通入100mL浓度为1.5mol/L的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:2c(Na+)=___________ 。
(1)KAl(SO4)2·12H2O可做净水剂,其原理是(用离子方程式表示)
(2)将体积相等的NaOH稀溶液和CH3COOH稀溶液充分混合后,若溶液中c(Na+)=c(CH3COO-),则混合前c(NaOH)
 ”“
”“ ”或“
”或“ ”)c(CH3COOH)。
”)c(CH3COOH)。(3)将AgCl分别放入①5mL H2O、②10mL 0.2mol/L MgCl2溶液、③20mL 0.5mol/L AgNO3溶液、④40mL 0.1mol/L HCl溶液中溶解至饱和,各溶液中Ag+的浓度由大到小的顺序是
(4)常温下a mol/L CH3COOH稀溶液和b mol/L KOH稀溶液等体积混合,若溶液呈中性则CH3COOH的电离平衡常数Ka=
(5)室温下,1mol/L相同体积的下列四种溶液①BaCl2、②FeCl3、③HF、④Na2CO3所含阳离子数由少到多的顺序是(用序号填空)
(6)标准状况下,将2.24L CO2通入100mL浓度为1.5mol/L的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式:2c(Na+)=
您最近一年使用:0次
【推荐2】雌黄 和雄黄都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。
和雄黄都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。 可转化为治疗白血病的亚砷酸(
可转化为治疗白血病的亚砷酸( )。
)。
(1)向 中滴加
中滴加 溶液反应,溶液中
溶液反应,溶液中 、
、 、
、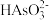 、
、 的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与pH的关系如图所示。
的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与pH的关系如图所示。

① 溶液呈
溶液呈_______ (填酸性、碱性或中性)。
②25℃时, 的第一电离平衡常数
的第一电离平衡常数 的值为
的值为_______ 。
③人体血液的pH在7.35~7.45之间,用药后人体中含砷元素的主要微粒是_______ 。
④下列说法正确的是_______ (填字母序号)。
a.M点对应的溶液中:
b.N点,
c.在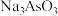 溶液中,
溶液中,
d. 时,溶液中:
时,溶液中:
⑤将 溶液滴入亚砷酸溶液,当
溶液滴入亚砷酸溶液,当 调至12.8时发生反应的离子方程式是
调至12.8时发生反应的离子方程式是__ 。
(2)P和As属于同主族元素,存在亚磷酸( ),常温下,
),常温下,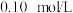 的
的 溶液的
溶液的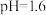 ,亚磷酸与足量的
,亚磷酸与足量的 溶液反应生成
溶液反应生成 。则
。则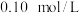 的
的 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是_______ 。
(3)25℃,在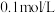 的
的 溶液中,通入
溶液中,通入 气体或加入
气体或加入 固体以调节溶液
固体以调节溶液 ,溶液
,溶液 与c(S2-)关系如图(忽略溶液体积的变化、
与c(S2-)关系如图(忽略溶液体积的变化、 的挥发)。某溶液含
的挥发)。某溶液含 、
、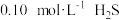 ,当溶液
,当溶液
_______ 时, 开始沉淀[已知
开始沉淀[已知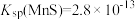 ]。
]。

 和雄黄都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。
和雄黄都是自然界中常见的砷化物,早期都曾用作绘画颜料,因都有抗病毒疗效也用来入药。 可转化为治疗白血病的亚砷酸(
可转化为治疗白血病的亚砷酸( )。
)。(1)向
 中滴加
中滴加 溶液反应,溶液中
溶液反应,溶液中 、
、 、
、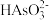 、
、 的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与pH的关系如图所示。
的分布分数(平衡时某微粒的浓度占微粒浓度之和的分数)与pH的关系如图所示。
①
 溶液呈
溶液呈②25℃时,
 的第一电离平衡常数
的第一电离平衡常数 的值为
的值为③人体血液的pH在7.35~7.45之间,用药后人体中含砷元素的主要微粒是
④下列说法正确的是
a.M点对应的溶液中:

b.N点,

c.在
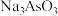 溶液中,
溶液中,
d.
 时,溶液中:
时,溶液中:
⑤将
 溶液滴入亚砷酸溶液,当
溶液滴入亚砷酸溶液,当 调至12.8时发生反应的离子方程式是
调至12.8时发生反应的离子方程式是(2)P和As属于同主族元素,存在亚磷酸(
 ),常温下,
),常温下,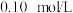 的
的 溶液的
溶液的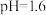 ,亚磷酸与足量的
,亚磷酸与足量的 溶液反应生成
溶液反应生成 。则
。则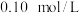 的
的 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是(3)25℃,在
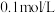 的
的 溶液中,通入
溶液中,通入 气体或加入
气体或加入 固体以调节溶液
固体以调节溶液 ,溶液
,溶液 与c(S2-)关系如图(忽略溶液体积的变化、
与c(S2-)关系如图(忽略溶液体积的变化、 的挥发)。某溶液含
的挥发)。某溶液含 、
、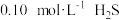 ,当溶液
,当溶液
 开始沉淀[已知
开始沉淀[已知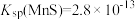 ]。
]。
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】已知常温下,几种电解质的电离常数如表所示:
回答下列问题:
(1)在 溶液中滴几滴酚酞,可能的现象是
溶液中滴几滴酚酞,可能的现象是___________ 。
(2)常温下,在醋酸溶液中加蒸馏水, 将
将___________ (填“增大”“减小”或“不变”)。
(3)常温下,体积均为 、物质的量浓度相等的下列三种溶液:
、物质的量浓度相等的下列三种溶液:
①NaClO溶液;②NaCl溶液;③ 溶液
溶液
其中离子总数由大到小的排序为___________ (填序号)。
(4)向 溶液通入少量
溶液通入少量 ,离子方程式为
,离子方程式为___________ 。
(5) 溶液中离子浓度(除
溶液中离子浓度(除 )大小排序为
)大小排序为___________ 。
| 电解质 |  |  |  |  |
 或 或 | 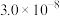 | 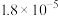 | 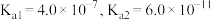 | 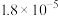 |
(1)在
 溶液中滴几滴酚酞,可能的现象是
溶液中滴几滴酚酞,可能的现象是(2)常温下,在醋酸溶液中加蒸馏水,
 将
将(3)常温下,体积均为
 、物质的量浓度相等的下列三种溶液:
、物质的量浓度相等的下列三种溶液:①NaClO溶液;②NaCl溶液;③
 溶液
溶液其中离子总数由大到小的排序为
(4)向
 溶液通入少量
溶液通入少量 ,离子方程式为
,离子方程式为(5)
 溶液中离子浓度(除
溶液中离子浓度(除 )大小排序为
)大小排序为
您最近一年使用:0次



