亚铁氰化钾{ }是一种重要的工业产品,工业中常用于制备铁氰化钾{
}是一种重要的工业产品,工业中常用于制备铁氰化钾{ },食品工业中作为添加剂常用作食盐的防结块剂。工业制备亚铁氯化钾{
},食品工业中作为添加剂常用作食盐的防结块剂。工业制备亚铁氯化钾{ }的流程如图:
}的流程如图:
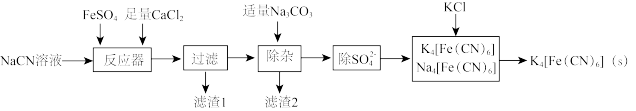
(1)实验室用NaCN固体配制NaCN溶液时,应将其先溶于_______ (填化学式)溶液,再用蒸馏水稀释到目标浓度。
(2) (滤渣1)
(滤渣1)_______  (滤渣2)(填“>”或“<”)。
(滤渣2)(填“>”或“<”)。
(3)溶解度:
_______ 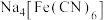 (填“>”或“<”)。
(填“>”或“<”)。
(4) 可用于检验
可用于检验 ,生成难溶盐
,生成难溶盐 ,该难溶盐可用于治疗
,该难溶盐可用于治疗 中毒,生成更难溶的物质排出体外,写出治疗
中毒,生成更难溶的物质排出体外,写出治疗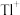 中毒的离子方程式:
中毒的离子方程式:_______ 。
(5)pH为6-7时, 可与
可与 饱和溶液反应,制取
饱和溶液反应,制取 ,反应时有灰黑色悬浮物生成,写出该反应的化学方程式:
,反应时有灰黑色悬浮物生成,写出该反应的化学方程式:_______ 。
(6)实验室中的 常因温度、光照等原因变质为
常因温度、光照等原因变质为 ,因此使用时需现配现用。重庆一中某科研小组设计了如图的原电池,制备
,因此使用时需现配现用。重庆一中某科研小组设计了如图的原电池,制备 ,并用沉淀滴定法,计算转化率。
,并用沉淀滴定法,计算转化率。
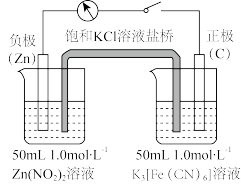
①盐桥中的 移向
移向_______ 侧烧杯(填“左”或“右”)。
②反应10分钟后,取左侧烧杯中5mL溶液,用0.1000 的
的 标准液滴定至终点,消耗标准液1.00mL,则右侧烧杯中
标准液滴定至终点,消耗标准液1.00mL,则右侧烧杯中 的转化率为
的转化率为_______ %(保留两位有效数字)。
 }是一种重要的工业产品,工业中常用于制备铁氰化钾{
}是一种重要的工业产品,工业中常用于制备铁氰化钾{ },食品工业中作为添加剂常用作食盐的防结块剂。工业制备亚铁氯化钾{
},食品工业中作为添加剂常用作食盐的防结块剂。工业制备亚铁氯化钾{ }的流程如图:
}的流程如图:
(1)实验室用NaCN固体配制NaCN溶液时,应将其先溶于
(2)
 (滤渣1)
(滤渣1) (滤渣2)(填“>”或“<”)。
(滤渣2)(填“>”或“<”)。(3)溶解度:

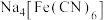 (填“>”或“<”)。
(填“>”或“<”)。(4)
 可用于检验
可用于检验 ,生成难溶盐
,生成难溶盐 ,该难溶盐可用于治疗
,该难溶盐可用于治疗 中毒,生成更难溶的物质排出体外,写出治疗
中毒,生成更难溶的物质排出体外,写出治疗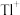 中毒的离子方程式:
中毒的离子方程式:(5)pH为6-7时,
 可与
可与 饱和溶液反应,制取
饱和溶液反应,制取 ,反应时有灰黑色悬浮物生成,写出该反应的化学方程式:
,反应时有灰黑色悬浮物生成,写出该反应的化学方程式:(6)实验室中的
 常因温度、光照等原因变质为
常因温度、光照等原因变质为 ,因此使用时需现配现用。重庆一中某科研小组设计了如图的原电池,制备
,因此使用时需现配现用。重庆一中某科研小组设计了如图的原电池,制备 ,并用沉淀滴定法,计算转化率。
,并用沉淀滴定法,计算转化率。
①盐桥中的
 移向
移向②反应10分钟后,取左侧烧杯中5mL溶液,用0.1000
 的
的 标准液滴定至终点,消耗标准液1.00mL,则右侧烧杯中
标准液滴定至终点,消耗标准液1.00mL,则右侧烧杯中 的转化率为
的转化率为
更新时间:2022-05-20 16:37:53
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某实验小组研究溶液中AgNO3和Na2S的反应。
(1)用离子方程式解释Na2S溶液pH>7的原因:___________ 。
(2)实验小组同学认为黑色沉淀中可能含有Ag2O、Ag2S或Ag,设计实验验证。
已知:i.浓硝酸能将Ag2S转化为Ag+和 :
:
ii.Ag2O能溶解在浓氨水中形成银氨溶液,而Ag2S和Ag均不能溶于氨水。
实验2:①设计并实施如下实验,证实沉淀中含有Ag2S。

试剂1和试剂2分别是___________ 、___________ 。
现象1和现象2分别是___________ 、___________ 。
实验3:②设计并实施如下实验,证实沉淀中不含有Ag2O,将实验操作和现象补充完整。
③经检验,沉淀不含有Ag。该黑色沉淀是Ag2S
| 实验I | 试剂 | 现象 | |
 | 试管 | 滴管 | |
| 0.lmol/LAgNO3溶液(pH=4) | 0.lmol/LNa2S溶液(pH=9) | 出现黑色沉淀 | |
(2)实验小组同学认为黑色沉淀中可能含有Ag2O、Ag2S或Ag,设计实验验证。
已知:i.浓硝酸能将Ag2S转化为Ag+和
 :
:ii.Ag2O能溶解在浓氨水中形成银氨溶液,而Ag2S和Ag均不能溶于氨水。
实验2:①设计并实施如下实验,证实沉淀中含有Ag2S。

试剂1和试剂2分别是
现象1和现象2分别是
实验3:②设计并实施如下实验,证实沉淀中不含有Ag2O,将实验操作和现象补充完整。
| 实验操作 | 实验现象 | |
| 步骤i | 取少量银氨溶液,向其中滴加盐酸 | 出现白色沉淀 |
| 步骤ii | 取少量实验1洗涤后的黑色沉淀, |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】如图是工业利用菱镁矿MgCO3(含杂质Al2O3、FeCO3)制取镁的工艺流程。
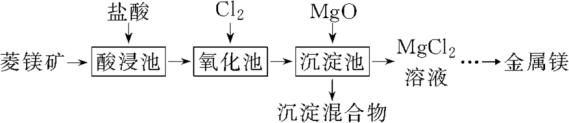
回答有关问题:
(1)菱镁矿送入酸浸池前需要粉碎,目的是___________ 。
(2)氧化池中通入氯气的目的是氧化___________ (填化学式),工业上不选用硝酸作氧化剂的原因是___________ 和___________ 。
(3)沉淀混合物为___________ 和___________ (填化学式)。
(4)利用熔融氯化镁制取金属镁,选用的方法是___________(填字母)。

回答有关问题:
(1)菱镁矿送入酸浸池前需要粉碎,目的是
(2)氧化池中通入氯气的目的是氧化
(3)沉淀混合物为
(4)利用熔融氯化镁制取金属镁,选用的方法是___________(填字母)。
| A.电解法 | B.氢气还原法 |
| C.碳还原法 | D.分解法 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】含碳化合物种类繁多。回答下列问题:
(1)一定温度下,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应CO(g)+H2O(g) CO2(g)+H2(g),已知此温度下,该反应的平衡常数K=16,则平衡时体系中H2的物质的量分数为
CO2(g)+H2(g),已知此温度下,该反应的平衡常数K=16,则平衡时体系中H2的物质的量分数为___ 。
(2)在催化剂Ru催化下,CO2与H2反应可生成CH4,反应方程式为CO2(g)+4H2(g)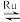 CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升至400℃,重新达到平衡,则v正
CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升至400℃,重新达到平衡,则v正___ (填"增大"减小"或"不变",下同),v逆___ ,平衡常数K___ ,转化率α(H2)___ ;若在相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如表:
则a、b、c、d与m、n、x、y之间的关系式为___ 。
(3)已知相关物质的电离平衡常数如表:
①0.1mol•L-1的Na2CO3溶液的pH___ (填“大于”“小于”或“等于”)0.1mol•L-1的Na2C2O4溶液的pH。
②若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中粒子浓度大小的顺序正确的是___ (填字母)。
a.c(H+)>c(HC2O )>c(HCO
)>c(HCO )>c(CO
)>c(CO )
)
b.c(HCO )>c(HC2O
)>c(HC2O )>c(C2O
)>c(C2O )>c(CO
)>c(CO )
)
c.c(H+)>c(HC2O )>c(CO
)>c(CO )>c(C2O
)>c(C2O )
)
d.c(H2CO3)>c(HCO )>c(HC2O
)>c(HC2O )>c(CO
)>c(CO )
)
(1)一定温度下,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应CO(g)+H2O(g)
 CO2(g)+H2(g),已知此温度下,该反应的平衡常数K=16,则平衡时体系中H2的物质的量分数为
CO2(g)+H2(g),已知此温度下,该反应的平衡常数K=16,则平衡时体系中H2的物质的量分数为(2)在催化剂Ru催化下,CO2与H2反应可生成CH4,反应方程式为CO2(g)+4H2(g)
 CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升至400℃,重新达到平衡,则v正
CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升至400℃,重新达到平衡,则v正| c(CO2)/mol·L-1 | c(H2)/mol·L-1 | c(CH4)/mol·L-1 | c(H2O)/mol·L-1 | |
| 平衡Ⅰ | a | b | c | d |
| 平衡Ⅱ | m | n | x | y |
(3)已知相关物质的电离平衡常数如表:
| 物质 | 电离平衡常数K |
| H2CO3 | Ka1=4.3×10-7,Ka2=5.6×10-11 |
| H2C2O4 | Ka1=5.9×10-2,Ka2=6.4×10-5 |
②若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中粒子浓度大小的顺序正确的是
a.c(H+)>c(HC2O
 )>c(HCO
)>c(HCO )>c(CO
)>c(CO )
)b.c(HCO
 )>c(HC2O
)>c(HC2O )>c(C2O
)>c(C2O )>c(CO
)>c(CO )
)c.c(H+)>c(HC2O
 )>c(CO
)>c(CO )>c(C2O
)>c(C2O )
)d.c(H2CO3)>c(HCO
 )>c(HC2O
)>c(HC2O )>c(CO
)>c(CO )
)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】用工业制立德粉后的铅锌废渣(主要成分为ZnO和PbSO4,杂质为含Si、Fe(III)、Cu、Cd等元素的化合物)为原料,制活性氧化锌和黄色颜料铅铬黄,工业流程如图所示:
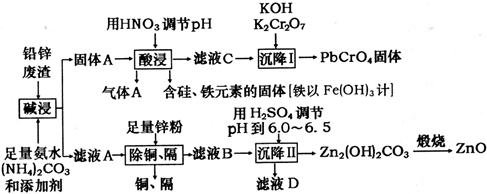
已知常温下Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=7.4×10-14,Ksp[Fe(OH)3]=1.0×10-38。
(1)“碱浸”过程中PbSO4发生反应的离子方程式为_______________________________ ,气体A的化学式为_________________________ 。
(2)“酸浸”过程中,在常温下应控制pH不低于________________________________ 。
(3)“沉降I”中发生沉降反应的离子方程式为____________________________ 。
(4)滤液D中溶质的主要成分为________________ 。
(5)以1t含锌元素10%的铅锌废渣制得活性氧化锌113.4kg,依据以上数据能否计算出锌元素的回收率。若能,写出计算结果,若不能,请说明理由。___________________ 。
(6)常温下NH3·H2O的电离常数Kb=1.8×10-5;碳酸的电离常数:Ka1=4.4×10-7,Ka2=5.6×10-11。该温度下某浓度的(NH4)2CO3溶液中c(NH4+)/c(NH3·H2O)=18。则溶液pH为__________________ ,c(HCO3-)/c(H2CO3)=____________________ 。

已知常温下Ksp(PbSO4)=1.6×10-5,Ksp(PbCO3)=7.4×10-14,Ksp[Fe(OH)3]=1.0×10-38。
(1)“碱浸”过程中PbSO4发生反应的离子方程式为
(2)“酸浸”过程中,在常温下应控制pH不低于
(3)“沉降I”中发生沉降反应的离子方程式为
(4)滤液D中溶质的主要成分为
(5)以1t含锌元素10%的铅锌废渣制得活性氧化锌113.4kg,依据以上数据能否计算出锌元素的回收率。若能,写出计算结果,若不能,请说明理由。
(6)常温下NH3·H2O的电离常数Kb=1.8×10-5;碳酸的电离常数:Ka1=4.4×10-7,Ka2=5.6×10-11。该温度下某浓度的(NH4)2CO3溶液中c(NH4+)/c(NH3·H2O)=18。则溶液pH为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】软锰矿的主要成分为 ,还含有
,还含有 等杂质,工业上用软锰矿制取
等杂质,工业上用软锰矿制取 的流程如图:
的流程如图:

已知:部分金属阳离子完全沉淀时的 如下表:
如下表:
(1)“浸出”过程中 转化为
转化为 的离子方程式为
的离子方程式为___________ 。
(2)第1步除杂中形成滤渣1的主要成分为___________ (填化学式),调 至
至 所加的试剂,可选择
所加的试剂,可选择___________ (填字母)。
a. b.
b. c.
c. d.氨水
d.氨水
(3)第2步除杂,主要是将 转化为相应氟化物沉淀除去,写出
转化为相应氟化物沉淀除去,写出 除去
除去 的离子方程式:
的离子方程式:___________ ,该反应的平衡常数为___________ (结果保留一位小数)(已知: 的
的 ;
; 的
的 )。
)。
(4)取少量 溶于水,配成溶液,测其
溶于水,配成溶液,测其 发现该溶液显酸性,原因是
发现该溶液显酸性,原因是___________ (用离子方程式表示)。
 ,还含有
,还含有 等杂质,工业上用软锰矿制取
等杂质,工业上用软锰矿制取 的流程如图:
的流程如图:
已知:部分金属阳离子完全沉淀时的
 如下表:
如下表:| 金属阳离子 |  |  |  |  |
完全沉淀时的 | 3.2 | 5.0 | 10.4 | 12.4 |
(1)“浸出”过程中
 转化为
转化为 的离子方程式为
的离子方程式为(2)第1步除杂中形成滤渣1的主要成分为
 至
至 所加的试剂,可选择
所加的试剂,可选择a.
 b.
b. c.
c. d.氨水
d.氨水(3)第2步除杂,主要是将
 转化为相应氟化物沉淀除去,写出
转化为相应氟化物沉淀除去,写出 除去
除去 的离子方程式:
的离子方程式: 的
的 ;
; 的
的 )。
)。(4)取少量
 溶于水,配成溶液,测其
溶于水,配成溶液,测其 发现该溶液显酸性,原因是
发现该溶液显酸性,原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】根据要求完成下列各题。
(1)25℃时,向AgCl的悬浊液中加入KI固体,有黄色沉淀生成。说明Ksp(AgCl)___ Ksp(AgI)(填“<”、“>”或“=”下同)。
(2)已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-。若浓硫酸与氢氧化钠溶液发生中和反应生成1mol水,则ΔH的数值___ 57.3kJ·mol-;若稀盐酸与氨水发生中和反应生成1mol水,则ΔH的数值___ 57.3kJ·mol-1。
(3)在化学反应里只有活化分子才可能发生化学反应,使普通分子变成活化分子所需提供的最低限度的能量叫活化能。根据如图回答问题。
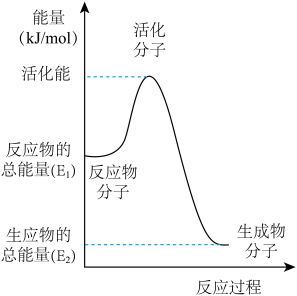
①图中所示反应是___ (填“吸热”或“放热”)反应,该反应___ (填“需要”或“不需要”)加热,该反应的△H=___ (用含E1、E2的代数式表示)。
②已知热化学方程式:H2(g)+ O2(g)=H2O(g) △H=-241.8kJ·mol-1,该反应的活化能为167.2kJ·mol-1,则其逆反应的活化能为
O2(g)=H2O(g) △H=-241.8kJ·mol-1,该反应的活化能为167.2kJ·mol-1,则其逆反应的活化能为___ 。
(1)25℃时,向AgCl的悬浊液中加入KI固体,有黄色沉淀生成。说明Ksp(AgCl)
(2)已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ·mol-。若浓硫酸与氢氧化钠溶液发生中和反应生成1mol水,则ΔH的数值
(3)在化学反应里只有活化分子才可能发生化学反应,使普通分子变成活化分子所需提供的最低限度的能量叫活化能。根据如图回答问题。

①图中所示反应是
②已知热化学方程式:H2(g)+
 O2(g)=H2O(g) △H=-241.8kJ·mol-1,该反应的活化能为167.2kJ·mol-1,则其逆反应的活化能为
O2(g)=H2O(g) △H=-241.8kJ·mol-1,该反应的活化能为167.2kJ·mol-1,则其逆反应的活化能为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】(1)室温时氢氧化钙的溶度积Ksp=4.7×10-6,室温时将9mL 0.02mol·L-1的氯化钙溶液与1mL pH=13的氢氧化钠溶液混合后(溶液体积可直接加和),溶液中_____ 沉淀析出(填有或无)。
(2)2.24升(标准状态)氨气通入250mL浓度为0.1mol·L-1的硫酸溶液中,充分反应后溶液中各离子浓度由大到小的顺序为________ 。
(3)用下图完成相应实验。
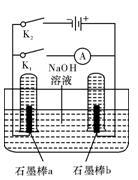
①断开K1,闭合K2接通直流电源,写出阳极的电极反应式__________ ;
②电解一段时间后,当两石墨棒均有气体包围时,切断K2闭合K1,发现电路中有电流通过。写出a极的电极反应式______________________ 。
(2)2.24升(标准状态)氨气通入250mL浓度为0.1mol·L-1的硫酸溶液中,充分反应后溶液中各离子浓度由大到小的顺序为
(3)用下图完成相应实验。

①断开K1,闭合K2接通直流电源,写出阳极的电极反应式
②电解一段时间后,当两石墨棒均有气体包围时,切断K2闭合K1,发现电路中有电流通过。写出a极的电极反应式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】三氯氧磷(POCl3)可用作半导体掺杂剂及光导纤维原料,是能推进中国半导体产业链发展壮大的一种重要的化工原料。工业上可以直接氧化 PCl3 制备 POCl3,反应原理为:P4(白磷)+6Cl2 4PCl3,2PCl3+O2
4PCl3,2PCl3+O2 2POCl3。
2POCl3。
已知:PCl3、POCl3的部分性质如下:
某化学兴趣小组模拟该工艺设计实验装置如图(某些夹持装置和加热装置已略去):
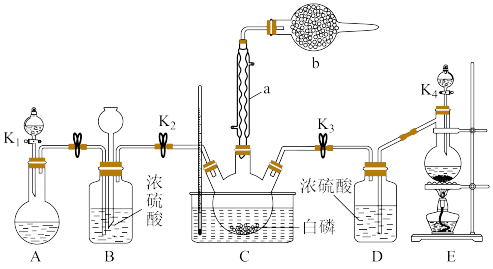
(1)检查装置气密性并加入纯净的白磷,先制取一种气体,缓慢地通入C中,直至C中的白磷完全消失后,再通入另一种气体。仪器b的名称为___________ ,B装置的作用是___________ 。
(2)装置 E 反应的离子方程式为___________ 。
(3)C反应温度控制 60~65 ℃,不能过高或过低的原因是___________ 。分离提纯获得 POCl3 的实验方法是___________ 。
(4)通过测定三氯氧磷产品中(含PCl3 杂质)氯元素含量,可进一步计算产品的纯度,实验步骤如下:
①取a g产品置于盛50.00 mL 蒸馏水的水解瓶中,摇动至完全水解,将水解液配成 100.00 mL 溶液,预处理排除含磷粒子的影响。
②取10.00 mL溶液于锥形瓶中,向其中加入c0 mol/L-1的AgNO3溶液V0 mL,使Cl-完全沉淀,再加入20 mL硝基苯,振荡,使沉淀表面被有机物覆盖;然后选择Fe(NO3)3 指示剂,用c1 mol/L-1 NH4SCN 溶液滴定过量Ag+ 至终点,记下所用体积为V1 mL。
滴定终点的现象:___________ 。实验过程中加入硝基苯覆盖沉淀的目的是___________ ,若无此操作,则所测POCl3的含量将___________ (填“偏高”“偏低”或“不变”)。[已知:Ksp(AgCl)=3.2×10-10,Ksp(AgSCN)=2.0×10-12]
(5)产品中POCl3的质量分数为___________ 。
 4PCl3,2PCl3+O2
4PCl3,2PCl3+O2 2POCl3。
2POCl3。已知:PCl3、POCl3的部分性质如下:
| 物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其它 |
| PCl3 | -112 | 75.5 | 137.5 | 遇水生成H3PO3和HCl |
| POCl3 | 2 | 105.3 | 153.5 | 遇水生成H3PO4和HCl |

(1)检查装置气密性并加入纯净的白磷,先制取一种气体,缓慢地通入C中,直至C中的白磷完全消失后,再通入另一种气体。仪器b的名称为
(2)装置 E 反应的离子方程式为
(3)C反应温度控制 60~65 ℃,不能过高或过低的原因是
(4)通过测定三氯氧磷产品中(含PCl3 杂质)氯元素含量,可进一步计算产品的纯度,实验步骤如下:
①取a g产品置于盛50.00 mL 蒸馏水的水解瓶中,摇动至完全水解,将水解液配成 100.00 mL 溶液,预处理排除含磷粒子的影响。
②取10.00 mL溶液于锥形瓶中,向其中加入c0 mol/L-1的AgNO3溶液V0 mL,使Cl-完全沉淀,再加入20 mL硝基苯,振荡,使沉淀表面被有机物覆盖;然后选择Fe(NO3)3 指示剂,用c1 mol/L-1 NH4SCN 溶液滴定过量Ag+ 至终点,记下所用体积为V1 mL。
滴定终点的现象:
(5)产品中POCl3的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】我国是最早发现并使用青铜器的国家,后母戊鼎是我国的一级文物,是世界上出土的最大最重的青铜礼器。现代社会中铜的应用常广泛,铜的回收再利用是化工生产的一个重要领域。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)回收Cu并制备ZnO的部分实验过程如下:

请回答下列问题:
(1)请写出一种加快铜帽溶解的方法:__________________ 。铜帽溶解时通入空气的作用是___________________________ (用化学方程式表示)。
(2)调节溶液pH时,是将溶液的pH调_________ (填“大”或“小”)到2~3。
(3)电解精炼粗铜时,阴极的电极反应式为___________________________ 。工业上常采用甲醇燃料电池作为电解精炼铜旳电源,写出碱性甲醇燃料电池的负极反应式:___________________________ 。
(4)已知:pH>11时,Zn(OH)2能溶于NaOH溶液生成ZnO22-。室温下,几种离子生成氢氧化物沉淀的pH如下表所小(开始沉淀的pH按金属离子浓度为0.01mol·L-1计算):
①上表中Fe3+沉淀完全的pH为__________________ 。
②由过滤粗铜的滤液制备ZnO的实验步骤依次为(可选用的试剂:30%H2O2、稀硝酸、1.0mol·L-1NaOH溶液):
a.___________________________ ;b.___________________________ ;c.过滤;
d.___________________________ ;e.过滤、洗涤、干燥;f.900℃煅烧。

请回答下列问题:
(1)请写出一种加快铜帽溶解的方法:
(2)调节溶液pH时,是将溶液的pH调
(3)电解精炼粗铜时,阴极的电极反应式为
(4)已知:pH>11时,Zn(OH)2能溶于NaOH溶液生成ZnO22-。室温下,几种离子生成氢氧化物沉淀的pH如下表所小(开始沉淀的pH按金属离子浓度为0.01mol·L-1计算):
| Fe3+ | Fe2+ | Zn2+ | Al3+ | |
| 开始沉淀的pH | 2 | 7.3 | 7.2 | 3.9 |
| 沉淀完全的pH | 8.3 | 8.2 | 5.2 |
②由过滤粗铜的滤液制备ZnO的实验步骤依次为(可选用的试剂:30%H2O2、稀硝酸、1.0mol·L-1NaOH溶液):
a.
d.
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】我国提出争取在2060年实现碳中和,这对于改善环境,实现绿色发展至关重要。将 转化为甲烷或甲醇有助于碳中和的实现。
转化为甲烷或甲醇有助于碳中和的实现。
(1)科学家们经过探索实践,建立了如图所示的 新循环体系:
新循环体系:

根据上图分析,下列相关说法不正确的是_______。
(2)在容积为2L的恒温密闭容器中,充入1mol 和3mol
和3mol ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间的变化情况如下表。
的物质的量随时间的变化情况如下表。
①下列说法正确的是_______ 。
A.反应达到平衡后,反应不再进行
B.使用催化剂可以增大反应速率,提高生产效率
C.改变条件, 可以100%转化为
可以100%转化为
D.通过调控反应条件,可以提高该反应进行的程度
②a=_______ ;3~6min内,
_______ 。
③第3min时
_______ (填“>”“<”或“=”)第9min时 。
。
(3)某种甲烷燃料电池的工作原理如图所示。

通入甲烷的一极为电源的_______ 极,该电极反应式_______ 。当电路中累计有2mol电子通过时,理论上消耗氧气的体积为(在标准状况下)_______ L。
 转化为甲烷或甲醇有助于碳中和的实现。
转化为甲烷或甲醇有助于碳中和的实现。(1)科学家们经过探索实践,建立了如图所示的
 新循环体系:
新循环体系:
根据上图分析,下列相关说法不正确的是_______。
| A.化学变化中质量和能量都是守恒的 |
B. 和H2生成甲烷的反应中原子利用率为100% 和H2生成甲烷的反应中原子利用率为100% |
C.将 还原为甲醇能有效促进“碳中和” 还原为甲醇能有效促进“碳中和” |
| D.无机物和有机物可以相互转化 |
 和3mol
和3mol ,一定条件下发生反应
,一定条件下发生反应 ,测得
,测得 和
和 的物质的量随时间的变化情况如下表。
的物质的量随时间的变化情况如下表。| 时间 | 0min | 3min | 6min | 9min | 12min |
 | 0 | 0.50 | 0.65 | 0.75 | 0.75 |
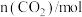 | 1 | 0.50 | 0.35 | a | 0.25 |
①下列说法正确的是
A.反应达到平衡后,反应不再进行
B.使用催化剂可以增大反应速率,提高生产效率
C.改变条件,
 可以100%转化为
可以100%转化为
D.通过调控反应条件,可以提高该反应进行的程度
②a=

③第3min时

 。
。(3)某种甲烷燃料电池的工作原理如图所示。

通入甲烷的一极为电源的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】联氨(N2H4)是一种应用广泛的化工原料,常用作火箭和燃料电池的燃料。回答下列问题:
(1)工业上利用N2和H2合成NH3,用NH3进一步制备联氨N2H4。已知断开(或形成)1molN≡N键、H-H键分别需要吸收(或放出)948.9kJ、436.0kJ的热量,合成1molNH3可放出46.1kJ的热量,则形成1molN-H放出的热量为___________ kJ(保留一位小数)。
(2)发射航天器时常以N2H4为燃料,NO2为推进剂。
已知ⅰ.N2H4(g)的摩尔燃烧焓为-622kJ/mol。
ⅱ.N2(g)与O2(g)反应的物质和能量变化示意图如下:
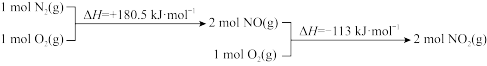
N2H4(g)与NO2(g)反应生成N2(g)和H2O(l)的热化学方程式为____________ 。
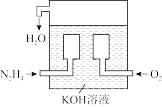
(3)燃料电池已广泛应用于航空领域。下图是一种新型燃料电池装置,其总反应方程式为N2H4+O2=N2+2H2O,通入N2H4(肼)的一极是电池的___________ (填“正极”或“负极”),该电极的电极反应式为___________ 。放电过程中,溶液中的阳离子移向___________ (填“正极”或“负极”)。
(4)在上述燃料电池中,若完全消耗16gN2H4,则理论上外电路中转移电子的物质的量为___________ mol,消耗氧气的体积为___________ L(标准状况)。
(1)工业上利用N2和H2合成NH3,用NH3进一步制备联氨N2H4。已知断开(或形成)1molN≡N键、H-H键分别需要吸收(或放出)948.9kJ、436.0kJ的热量,合成1molNH3可放出46.1kJ的热量,则形成1molN-H放出的热量为
(2)发射航天器时常以N2H4为燃料,NO2为推进剂。
已知ⅰ.N2H4(g)的摩尔燃烧焓为-622kJ/mol。
ⅱ.N2(g)与O2(g)反应的物质和能量变化示意图如下:
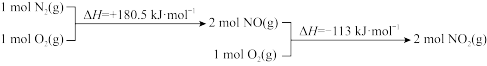
N2H4(g)与NO2(g)反应生成N2(g)和H2O(l)的热化学方程式为
(3)燃料电池已广泛应用于航空领域。下图是一种新型燃料电池装置,其总反应方程式为N2H4+O2=N2+2H2O,通入N2H4(肼)的一极是电池的

(4)在上述燃料电池中,若完全消耗16gN2H4,则理论上外电路中转移电子的物质的量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】电池的种类很多,在生活中有广泛的用途。
Ⅰ.其中纽扣式微型银锌电池广泛的应用于电子表和电子计算器中,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O===2Ag+Zn(OH)2。
(1)其正极的电极反应式:_________________________________ ,工作时电池电解质溶液的碱性_______ (填“增强”、“减弱”或“不变”)。
Ⅱ.固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。
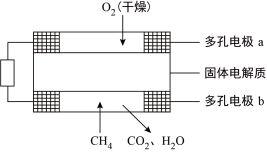
(2) a电极为电源的_______ 极,固体电解质中的阳离子向_______ 极移动;
(3) b电极的电极反应式为:_______________________________________ ;
(4)电池的总反应方程式为:______________________________________ ;
当电路中有2mol电子转移时,理论上负极消耗的标况下气体体积是______________ L。
Ⅰ.其中纽扣式微型银锌电池广泛的应用于电子表和电子计算器中,其电极分别为Ag2O和Zn,电解质为KOH溶液,工作时电池总反应为Ag2O+Zn+H2O===2Ag+Zn(OH)2。
(1)其正极的电极反应式:
Ⅱ.固体氧化物甲烷燃料电池以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。

(2) a电极为电源的
(3) b电极的电极反应式为:
(4)电池的总反应方程式为:
当电路中有2mol电子转移时,理论上负极消耗的标况下气体体积是
您最近一年使用:0次



