向体积均为2L的两个恒容密闭容器中分别充入 ,维持容器的温度分别为T1℃和T2℃不变,发生反应:
,维持容器的温度分别为T1℃和T2℃不变,发生反应: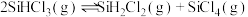
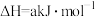 。反应过程中
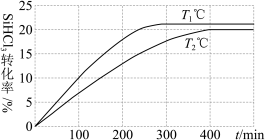
。反应过程中 的转化率随时间的变化如图所示。下列说法正确的是
的转化率随时间的变化如图所示。下列说法正确的是
 ,维持容器的温度分别为T1℃和T2℃不变,发生反应:
,维持容器的温度分别为T1℃和T2℃不变,发生反应: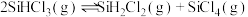
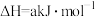 。反应过程中
。反应过程中 的转化率随时间的变化如图所示。下列说法正确的是
的转化率随时间的变化如图所示。下列说法正确的是
| A.a<0 |
B.T1℃时,0~100min内,反应的平均速率 |
C.T2℃时,使用合适的催化剂,可使 的平衡转化率与T1℃时相同 的平衡转化率与T1℃时相同 |
D.T2℃时,向平衡后的容器中充入少量 ,此时反应向正反应方向进行 ,此时反应向正反应方向进行 |
21-22高二下·安徽阜阳·期末 查看更多[8]
更新时间:2022-07-04 06:43:06
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】将气体A、B置于固定容积为2L的密闭容器中,发生如下反应: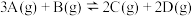 ,反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。下列说法中不正确的是
,反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。下列说法中不正确的是
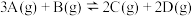 ,反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。下列说法中不正确的是
,反应进行到10s末,达到平衡,测得A的物质的量为1.8mol,B的物质的量为0.6mol,C的物质的量为0.8mol。下列说法中不正确的是| A.当v(A)正=3v(B)逆时,反应达到平衡状态 |
B.用B表示10s内反应的平均反应速率为0.03 |
C.A与B的平衡转化率(转化率= 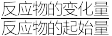  100%)比为1:1 100%)比为1:1 |
| D.反应过程中容器内气体的平均相对分子质量不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示。则下列对该反应的推断合理的是
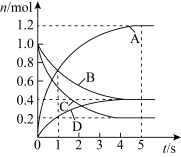

A.该反应的化学方程式为6A+2D 3B+4C 3B+4C |
| B.0~1s内,v(A)=v(B) |
| C.5s时,v(A)=v(B)=v(C)=v(D) |
| D.0~5s内,B的平均反应速率为0.06mol/(L·s) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】PCl3和PCl5都是重要的化工原料。将PCl3(g)和Cl2(g)充入2L的恒容密闭容器中,在一定条件下发生反应PCl3(g)+Cl2(g) PCl5(g),△H<0并于10min时达到平衡。有关数据如下:下列判断正确的是
PCl5(g),△H<0并于10min时达到平衡。有关数据如下:下列判断正确的是
 PCl5(g),△H<0并于10min时达到平衡。有关数据如下:下列判断正确的是
PCl5(g),△H<0并于10min时达到平衡。有关数据如下:下列判断正确的是| PCl3(g) | Cl2(g) | PCl5(g) | |
| 初始浓度/(mol•L-1) | 2.0 | 1.0 | 0 |
| 平衡浓度/(mol•L-1) | c1 | c2 | 0.4 |
| A.10 min内,v(Cl2)=0.02 mol/( L•min) |
| B.升高温度,反应的平衡常数增大 |
| C.反应达到平衡时容器内的压强与初始时容器的压强之比为1:2 |
| D.平衡后移走2.0 mol PCl3和1.0 mol Cl2,相同条件下再达平衡时,c(PCl5)<0.2 mol•L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】一定温度下,向某真空密闭容器中投入碳酸钙,发生反应CaCO3(s)⇌CaO(s)+CO2(g),达到平衡后,将容器容积缩小为原来的一半。当体系再次达到平衡时,CO2的浓度
| A.增大为原来的2倍 | B.比原来大,但比2倍小 |
| C.不变 | D.减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】科研人员提出120℃下CeO2催化合成DMC(碳酸二甲酯)需经历三步反应,示意图如下。下列说法正确的是

注: 表示催化剂
表示催化剂

注:
 表示催化剂
表示催化剂| A.DMC与过量稀H2SO4溶液完全反应生成CH3OCOOH和甲醇 |
| B.改用更高效的催化剂,可提高DMC的平衡产率 |
| C.反应历程①②③中,活化能越高,反应速率越慢 |
| D.向反应体系中加入少量水蒸气,反应物的平衡转化率升高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】根据下列图示所得出的结论正确的是:
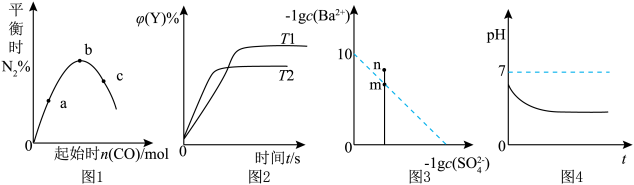

| A.图1表示反应2CO(g)+2NO(g) ⇌N2(g)+2CO2(g)在其他条件不变时,起始CO物质的量与平衡时N2的体积分数关系,说明NO的转化率b>c>a |
| B.图2表示反应2X(g) ⇌Y(g)分别在T1、T2温度下,Y的体积分数随时间的变化,说明该反应的ΔH<0 |
C.图3是室温下BaSO4达到沉淀溶解平衡时,溶液中c(Ba2+)与c( )的关系曲线,说明通过蒸发浓缩可使溶液由n点转化到m点 )的关系曲线,说明通过蒸发浓缩可使溶液由n点转化到m点 |
| D.图4表示含少量SO2的水溶液暴露在空气中,溶液的pH随时间的变化,说明在空气中时间越长,亚硫酸的电离程度越大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】化学中常用图象直观地描述化学反应的进程或结果。下列图象描述正确的是
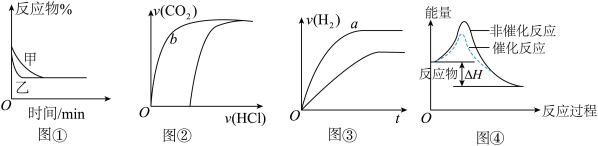

A.图①表示不同压强对可逆反应2A(g)+2B(g) 3C(g) +D(s)的影响 3C(g) +D(s)的影响 |
| B.图②表示向10ml 0.1mol·L-1Na2CO3和NaHCO3两种溶液中分别滴加0.lnol·L-1HCl溶液时,CO2的体积随盐酸体积的变化,则b 表示的是NaHCO3溶液 |
| C.图③表示体积和pH 均相同的HCl、CH3COOH 两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示的是HCl 溶液 |
| D.图④表示该反应为放热反应,且催化剂能改变反应的焓变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g) 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。
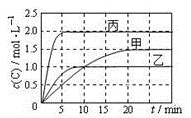
下列说法正确的是
 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。
| 容器 | 甲 | 乙 | 丙 |
| 容积 | 1L | 1L | 2L |
| 温度/℃ | T1 | T2 | T2 |
| 反应物 起始量 | 1molA 2molB | 1molA 2molB | 4molA 8molB |
下列说法正确的是
| A.由图可知T1<T2,且该反应为吸热反应 |
| B.前10min内甲、乙、丙三个容器中反应的平均速率:v(A)乙<v(A)甲< v(A)丙 |
| C.平衡时A的转化率a:a乙<a甲<a丙 |
| D.T1时该反应的平衡常数K=7.2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】乙炔( )是重要的化工原料。工业上可用甲烷裂解法制取乙炔,发生反应:
)是重要的化工原料。工业上可用甲烷裂解法制取乙炔,发生反应:
反应Ⅰ: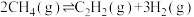
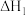
反应Ⅱ: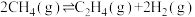
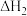
甲烷裂解时,几种气体平衡时分压(Pa)的对数即lgp与温度(℃)之间的关系如图所示,(注:用平衡分压代替平衡浓度计算可得平衡常数 分压=总压×物质的量分数)。下列说法不正确的是
分压=总压×物质的量分数)。下列说法不正确的是
 )是重要的化工原料。工业上可用甲烷裂解法制取乙炔,发生反应:
)是重要的化工原料。工业上可用甲烷裂解法制取乙炔,发生反应:反应Ⅰ:
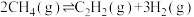
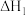
反应Ⅱ:
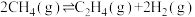
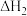
甲烷裂解时,几种气体平衡时分压(Pa)的对数即lgp与温度(℃)之间的关系如图所示,(注:用平衡分压代替平衡浓度计算可得平衡常数
 分压=总压×物质的量分数)。下列说法不正确的是
分压=总压×物质的量分数)。下列说法不正确的是
A.1725℃时,向恒容密闭容器中充入 ,达到平衡时 ,达到平衡时 生成 生成 的平衡转化率为62.5% 的平衡转化率为62.5% |
B.1725℃时,若图中 的 的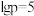 ,则反应 ,则反应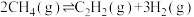 的平衡常数 的平衡常数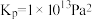 |
C.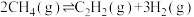 的 的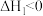 |
| D.为提高甲烷制乙炔的产率,除改变温度外,可充入适量乙烯,还可以使用对反应选择性更高的催化剂 |
您最近一年使用:0次

 xC(g),有下图所示的关系曲线,根据下图下列判断正确的是
xC(g),有下图所示的关系曲线,根据下图下列判断正确的是