(1)常温时,0.1mol•L-1NH4Al(SO4)2溶液的pH=3。
①溶液中的Kw=
②溶液中c(NH
 )+c(NH3•H2O)
)+c(NH3•H2O) )-c(NH
)-c(NH )-3c(Al3+)=
)-3c(Al3+)=(2)80℃时,0.1mol•L-1NH4Al(SO4)2溶液的pH小于3,分析导致pH随温度变化的原因是
(3)常温时,向100mL0.1mol•L-1NH4HSO4溶液中滴加0.1mol•L-1NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。

①图中a、b、c、d四点中水的电离程度最大的是
②向NH4HSO4溶液中滴加NaOH溶液从a点到d点的过程中,发生反应的离子方程式
③NH4HSO4溶液中各离子浓度由大到小的排列顺序是
相似题推荐
甲:取纯度相同,质量、大小相等的锌粒于两支试管中,同时加入0.1 mol·L-1的 HA、HCl溶液各10 mL,按图装好,观察现象;
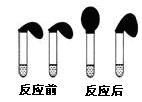
乙:① 用pH计测定物质的量浓度均为0.1 mol·L-1 HA和HCl溶液的pH;
② 再取0.1 mol·L-1的HA和HCl溶液各2滴(1滴约为1/25 mL)分别稀释至100 mL,再用pH计测其pH变化
(1)乙方案中说明HA是弱电解质的理由是:测得0.1 mol·L-1的HA溶液的pH
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后, 试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第
A. NaA固体(可完全溶于水) B.1 mol·L-1 NaOH溶液
C. 1 mol·L-1 H2SO4 D.2 mol·L-1 HA
(3)pH=1的两种酸溶液A、B各1 mL,分别加水稀释到1000 mL,其pH与溶液体积V的关系如图所示,则下列说法不正确的有

A.两种酸溶液的物质的量浓度一定相等
B.稀释后,A酸溶液的酸性比B酸溶液弱
C.若a=4,则A是强酸,B是弱酸
D.若1<a<4,则A、B都是弱酸
E.稀释后A溶液中水的电离程度比B溶液中水的电离程度小
Ⅰ.化学家研究发现,SbF5能将MnF4从离子[MnF6]2-的盐中反应得到,SbF5转化成稳定离子[SbF6]-的盐。而MnF4很不稳定,受热易分解为MnF3和F2。根据以上研究写出以K2MnF6和SbF5为原料,在 423 K 的温度下制备F2的化学方程式:

现代工业以电解熔融的氟氢化钾(KHF2)和氟化氢(HF)混合物制备氟单质,电解制氟装置如图所示。
已知KHF2是一种酸式盐,写出阴极上发生的电极反应式
Ⅱ.①卤化氢的熔沸点随相对分子质量增加而升高,而HF熔沸点高于HCl的原因是
②已知25 ℃时,氢氟酸(HF)的电离平衡常数Ka=3.6×10-4。
某pH=2的氢氟酸溶液,由水电离出的c(H+)=
③又已知25 ℃时,溶度积常数Ksp(CaF2)=1.46×10-10。现向1 L 0.2 mol/L HF溶液中加入 1 L 0.2 mol/L CaCl2 溶液,通过列式计算说明是否有沉淀产生:
| 弱酸 |  |  |  |
电离平衡常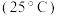 | 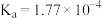 |  | 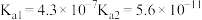 |
 水溶液
水溶液 ,原因是
,原因是 的
的 溶液中,由水电离出的
溶液中,由水电离出的 浓度为
浓度为(2)同浓度
 这4种溶液中碱性由强到弱的顺序是
这4种溶液中碱性由强到弱的顺序是 溶液中各离子浓度由大到小的顺序是
溶液中各离子浓度由大到小的顺序是(3)体积相同、
 相同的三种酸溶液a.
相同的三种酸溶液a. ;b.
;b. ;c.
;c. 分别与同浓度的
分别与同浓度的 溶液完全中和,消耗
溶液完全中和,消耗 溶液的体积由大到小的排列顺序是(填字母)
溶液的体积由大到小的排列顺序是(填字母)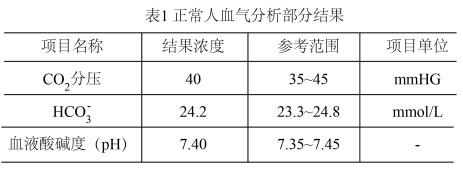
(1)人体血液呈弱碱性的原因是
(2)从平衡角度解释人体血液pH稳定的原因
(3)当人体代谢性酸中毒严重时,需要血液透析治疗。
①预测“酸中毒”时表1“结果浓度”有可能会有哪些变化:
②配制某浓缩透析液需要用到的溶质有:0.7mol/LNaCl,0.01mol/LKCl,0.075mol/LCaCl2和0.15mol/LNaHCO3,直接混合各溶质会有沉淀
③医院透析液分两瓶存放,使用时稀释再混合。其中一瓶为NaHCO3,下列说法正确的是
A.c(Na+)>c(
 )>c(H+)>c(OH-) B.c(Na+)+c(H+)=c(
)>c(H+)>c(OH-) B.c(Na+)+c(H+)=c( )+c(OH-)+2c(
)+c(OH-)+2c( )
)C.c(
 )>c(H2CO3) D.c(Na+)=c(
)>c(H2CO3) D.c(Na+)=c( )+c(H2CO3)+c(
)+c(H2CO3)+c( )
)(4)常温下,反应CaCO3(s)+2F-(aq)
 CaF2(s) +
CaF2(s) + (aq)的平衡常数K=
(aq)的平衡常数K= 主要含
主要含 、
、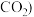 的
的 形成酸雨、污染大气,对烟气进行脱硫,回答下列问题:
形成酸雨、污染大气,对烟气进行脱硫,回答下列问题:

(1)采用
 烟气脱硫可得到较好的效果.已知下列反应:
烟气脱硫可得到较好的效果.已知下列反应: 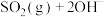
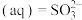
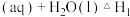

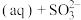
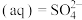
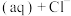
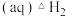
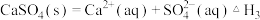
则反应
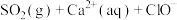

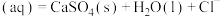
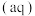 的
的
(2)采用氨水烟气脱硫,最终可得到氮肥.将相同物质的量的
 与
与 溶于水所得溶液中
溶于水所得溶液中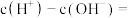
 填字母编号
填字母编号 .
.A.
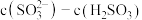
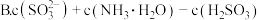
C.
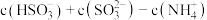
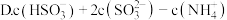
(3)烟气在较高温度经如图1方法脱除
 ,并制得
,并制得 .
. ①在阴极放电的物质是
②在阳极生成
 的电极反应式是
的电极反应式是 ③已知室温下,
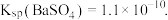 将脱除
将脱除 后制得的
后制得的 配成
配成 的
的 溶液,与
溶液,与 的
的  溶液混合,若所得混合溶液的
溶液混合,若所得混合溶液的  ,则
,则  溶液与
溶液与  溶液的体积比为
溶液的体积比为  欲使溶液中
欲使溶液中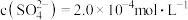 ,则应保持溶液中
,则应保持溶液中 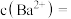
 .
. (4)一定条件下,用
 、NiO或
、NiO或 作催化剂,利用如下反应回收燃煤烟气中的硫.反应为:
作催化剂,利用如下反应回收燃煤烟气中的硫.反应为: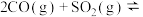
 其他条件相同、催化剂不同时,
其他条件相同、催化剂不同时, 的转化率随反应温度的变化如图2,不考虑催化剂的价格因素,选择
的转化率随反应温度的变化如图2,不考虑催化剂的价格因素,选择  选填序号
选填序号 ;
;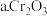
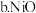
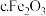
选择该催化剂的理由是:
某科研小组用选择的催化剂,在
 时,研究了
时,研究了 :
: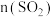 分别为1:1、3:1时,
分别为1:1、3:1时, 转化率的变化情况
转化率的变化情况 图
图 则图3中表示
则图3中表示 :
: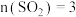 :1的变化曲线为
:1的变化曲线为 A.在250 mL的容量瓶中定容配成250mL烧碱溶液
B.用移液管移取25 mL烧碱溶液于锥形瓶中并滴几滴指示剂甲基橙
C.在天平上准确称取烧碱样品Wg,在烧杯中用蒸馏水溶解
D.将物质的量浓度为c的标准盐酸溶液装入酸式滴定管,调节液面,记下开始读数为V1
E.在锥形瓶下垫一张白纸,滴定至终点,记下读数V2
回答下列各问题:
(1)正确操作步骤的顺序是(用字母填写)
(2)D步骤中液面应调节到
(3)滴定终点时锥形瓶中颜色变化是
(4)若酸式滴定管不用标准盐酸润洗,在其他操作均正确的前提下,会对测定结果(指烧碱的纯度)有何影响?
(5)该烧碱样品纯度的计算式为
Ⅱ. (1)常温下,0.2 mol/L HCl溶液与0.2 mol/L MOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=6,则①混合溶液中由水电离出的c(H+)
②求出混合溶液中下列算式的精确计算结果(填具体数字)。
c(Cl-)-c(M+)=
(2)常温下若将pH=3的HR溶液与pH=11的NaOH溶液等体积混合,测得混合溶液的pH≠7,则混合溶液的pH
 时,三种酸的电离平衡常数如下,回答下列问题:
时,三种酸的电离平衡常数如下,回答下列问题:| 化学式 |  |  |  |
| 电离平衡常数 |  | 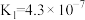 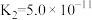 |  |
(1)一般情况下,当温度升高时,电离平衡常数K
(2)下列四种离子结合质子能力最强的是___________(填字母)。
A. | B. | C. | D. |
 、
、 均为2的醋酸溶液与
均为2的醋酸溶液与 溶液分别加水稀释至
溶液分别加水稀释至 ,稀释过程中
,稀释过程中 变化如图所示。
变化如图所示。
则
 的电离平衡常数
的电离平衡常数 溶液中水电离出来的
溶液中水电离出来的
 ;用同浓度的
;用同浓度的 溶液分别中和上述两种酸溶液,恰好中和时消耗
溶液分别中和上述两种酸溶液,恰好中和时消耗 溶液的体积:醋酸
溶液的体积:醋酸 。
。(4)常温下,用
 溶液作
溶液作 捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品
捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品 ,某次捕捉后得到
,某次捕捉后得到 的溶液、则溶液中
的溶液、则溶液中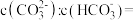
(5)已知某二元弱酸
 :
: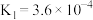 ;
;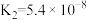 ,则
,则 溶液显
溶液显 的认识及其再利用的研究尤为重要。
的认识及其再利用的研究尤为重要。(1)海水中溶解一定量
 ,主要含有的离子是
,主要含有的离子是 、
、 、
、 、
、 、
、 、
、 。
。①海水的弱碱性(pH约为8.1)有利于维持海洋生态环境,请用离子方程式解释海水呈弱碱性的原因
②炎炎夏日,海水的pH会
③随着人类活动的影响,过量的
 的排放使得海水酸性增强,海洋生态系统面临巨大威胁,有研究者提出,用如图所示方法可从海水中提取
的排放使得海水酸性增强,海洋生态系统面临巨大威胁,有研究者提出,用如图所示方法可从海水中提取 。
。
a室电极反应方程式为
 提取,发生的反应离子方程式为
提取,发生的反应离子方程式为(2)“碳捕捉技术”可实现
 的分离、储存和利用,其流程如下所示。
的分离、储存和利用,其流程如下所示。
已知:25℃时,
 电离常数分别为
电离常数分别为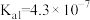 、
、 。
。溶液中含碳物种的浓度
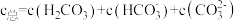 。
。④若忽略溶液体积的变化,以0.1
 NaOH溶液捕捉
NaOH溶液捕捉 ,当NaOH溶液吸收
,当NaOH溶液吸收 至溶液中含碳物种的浓度
至溶液中含碳物种的浓度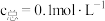 溶液时,
溶液时,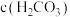
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。⑤整个流程中,可循环利用的物质有
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g)
 2CO2(g)+N2(g)
2CO2(g)+N2(g)①在一定条件下,在一个容积固定为2L的密闭容器中充入0.8mol NO和1.20mol CO,开始反应至3 min时测得CO的转化率为20%,则用N2表示的平均反应速率为v(N2)=
②对于气相反应,用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可以表示平衡常数(记作Kp),则该反应平衡常数的表达式Kp=
③该反应在低温下能自发进行,该反应的ΔH
(2)使用甲醇汽油能减少汽车尾气对环境的污染,某化工厂用水煤气为原料合成甲醇,在恒温恒压条件下的密闭容器中发生反应:CO(g)+2H2(g)⇌CH3OH(g),到达平衡时,测得CO、H2、CH3OH分别为1mol、1mol、1mol,容器的体积为3L,现往容器中继续通入3molCO,此时v(正)
(3)已知:H2A=H++HA-,HA-⇌H++A2-。常温下,0.1 mol·L-1的NaHA溶液其pH=2,则0.1 mol·L-1的H2A溶液中氢离子浓度的大小范围是
(4)常温时,Fe(OH)3的Ksp=1×10-38,要使溶液中的Fe3+沉淀完全[残留在溶液中的c(Fe3+)<10-5 mol·L-1],则溶液的pH应大于



