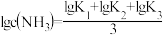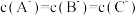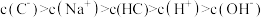焦磷酸盐(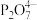 )常用于电镀工业。焦磷酸(
)常用于电镀工业。焦磷酸(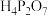 )为两分子磷酸脱水而成的多元酸,不同型体的分布分数(
)为两分子磷酸脱水而成的多元酸,不同型体的分布分数( )与
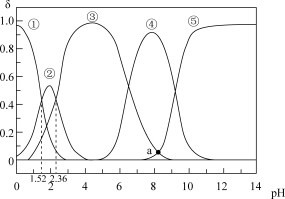
)与 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
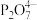 )常用于电镀工业。焦磷酸(
)常用于电镀工业。焦磷酸(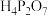 )为两分子磷酸脱水而成的多元酸,不同型体的分布分数(
)为两分子磷酸脱水而成的多元酸,不同型体的分布分数( )与
)与 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
A.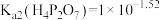 |
B.0.1 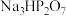 溶液中: 溶液中: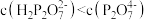 |
C.a点,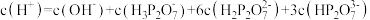 |
D.反应 趋于完全 趋于完全 |
更新时间:2022-11-11 18:20:17
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下列说法正确的是
| A.电解法精炼镍时,粗镍作阴极,纯镍作阳极 |
B.反应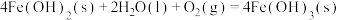 常温下能自发进行,该反应的 常温下能自发进行,该反应的 |
C.常温下 溶液中加入少量 溶液中加入少量 固体,溶液中 固体,溶液中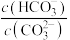 值减小 值减小 |
D.在一容积可变的密闭容器中反应 达平衡后,保持温度不变,缩小体积,平衡正向移动, 达平衡后,保持温度不变,缩小体积,平衡正向移动, 的值增大 的值增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】向温度为300℃的2 L密闭容器中充入2 mol SO2和1 mol O2,发生反应2SO2 (g)+ O2 (g)  2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是
2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是
 2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是
2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是| A.该温度下,反应的平衡常数K =1620 |
| B.SO2和O2的平衡转化率相等 |
| C.平衡后保持温度和容器体积不变,再充入SO3(g),平衡常数不变 |
| D.若不再向容器中加入任何物质,仅改变条件不可能使SO2的浓度达到1 mol/L |
您最近一年使用:0次
【推荐3】N2O5是一种新型硝化剂,在一定温度下可发生如下反应:2N2O5(g)⇌4NO2(g)+O2(g)△H>0.T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
下列说法正确的是( )
| 时间/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/(mol·L-1) | 5.00 | 3.52 | 2.50 | 2.50 |
| A.500_s内NO2的生成速率为2.96×10﹣3_mol•L﹣1•s﹣1 |
| B.T1温度下该反应平衡时N2O5的转化率为29.6% |
| C.达到平衡其他条件不变,将容器的体积压缩到原来1/2,则c(N2O5)<5.00mol•L﹣ |
| D.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1>K2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
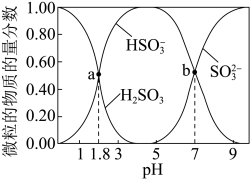
【推荐1】室温时,配制一组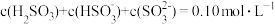 的H2SO3和NaOH混合溶液,溶液中H2SO3、
的H2SO3和NaOH混合溶液,溶液中H2SO3、 、
、 随pH的分布如图所示,下列指定溶液中微粒物质的量浓度关系正确的是
随pH的分布如图所示,下列指定溶液中微粒物质的量浓度关系正确的是
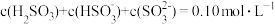 的H2SO3和NaOH混合溶液,溶液中H2SO3、
的H2SO3和NaOH混合溶液,溶液中H2SO3、 、
、 随pH的分布如图所示,下列指定溶液中微粒物质的量浓度关系正确的是
随pH的分布如图所示,下列指定溶液中微粒物质的量浓度关系正确的是
| A.a点和b点对应水溶液中均有水电离出的c(H+)·c(OH-)=10-14 |
B.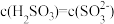 时,溶液的pH为4.4 时,溶液的pH为4.4 |
C.c(Na+)=0.10 mol·L-1时:c(H+)+c(H2SO3)>c(OH-)+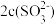 |
D.b点:c(Na+)>0.10 mol·L-1+ |
您最近一年使用:0次
单选题
|
较难
(0.4)
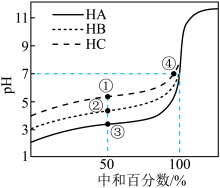
【推荐2】25℃时,将浓度均为0.1mol/L、体积不同的HA溶液与BOH 溶液混合,保持溶液的总体积为100 mL,溶液的体积与混合液pH 的关系如图所示。下列说法正确的是


| A.V1表示HA 溶液的体积,V2表示BOH 溶液的体积 |
| B.Ka(HA) 和Kb(BOH) 的数量级相等,均为10-6 |
| C.y点时,c(B+)=c(A-)=c(OH-)=c(H+) |
| D.x、y、z 所示三点时水的电离程度:y>x=z |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】常温下,向1升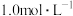 的NaClO溶液中缓慢通入
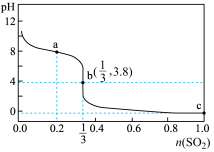
的NaClO溶液中缓慢通入 气体,使其充分吸收,溶液pH与通入
气体,使其充分吸收,溶液pH与通入 的物质的量关系如图所示(忽略溶液体积变化及NaClO、HClO的分解,以上发生的氧化还原反应均为不可逆反应)。下列说法错误的是
的物质的量关系如图所示(忽略溶液体积变化及NaClO、HClO的分解,以上发生的氧化还原反应均为不可逆反应)。下列说法错误的是
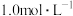 的NaClO溶液中缓慢通入
的NaClO溶液中缓慢通入 气体,使其充分吸收,溶液pH与通入
气体,使其充分吸收,溶液pH与通入 的物质的量关系如图所示(忽略溶液体积变化及NaClO、HClO的分解,以上发生的氧化还原反应均为不可逆反应)。下列说法错误的是
的物质的量关系如图所示(忽略溶液体积变化及NaClO、HClO的分解,以上发生的氧化还原反应均为不可逆反应)。下列说法错误的是
A.常温下,HClO电离平衡常数的数量级为 |
B.a点溶液中: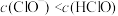 |
C.b点溶液中: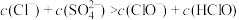 |
D.c点溶液中: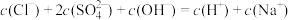 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】t℃时,将0.200mol/L的某一元酸HA与0.200mol/L的NaOH溶液等体积混合,所得混合溶液中部分离子浓度如下表。
下列说法中正确的是
微粒 | H+ | Na+ | A- |
| 浓度(mol/L) | 2.50×10-10 | 0.100 | 9.92×10-2 |
下列说法中正确的是
| A.所得溶液中: c(Na+) >c(A-) >c(HA) >c(OH-) |
| B.t℃时,水的离子积Kw < 1.0×10-14 |
| C.t℃时,一元酸HA的电离常数K=3.10×10-8 |
| D.t℃时,0.100mol/LNaA溶液中A-的水解率为0.400% |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】常温下联氨 的水溶液中有:
的水溶液中有:

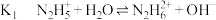

 提示:二元弱碱的电离也是分步电离
提示:二元弱碱的电离也是分步电离
该溶液中的微粒的物质的量分数 随
随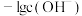 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是

 的水溶液中有:
的水溶液中有:
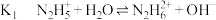

 提示:二元弱碱的电离也是分步电离
提示:二元弱碱的电离也是分步电离
该溶液中的微粒的物质的量分数
 随
随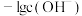 变化的关系如图所示。下列叙述错误的是
变化的关系如图所示。下列叙述错误的是
A.据A点可求: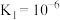 |
B.D点溶液的 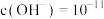 |
C.若C点为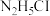 溶液,则存在: 溶液,则存在: |
D.在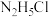 水溶液中, 水溶液中, |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】常温下,在新制氯水中滴加少量烧碱溶液,溶液中含氯粒子的物质的量分数与pH关系如图所示。
下列说法错误的是

下列说法错误的是
| A.pH=2时,c(Cl)>c(Cl2)>c(Cl3)>c(HClO)>c(ClO) |
| B.pH=5左右时,溶液中c(HClO)最大,漂白效率最高 |
| C.常温下,HClO的电离常数(Ka)数量级为107 |
| D.pH=7时,溶液中存在:c(Na)=c(ClO)+c(Cl3)+c(Cl) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】常温下,用pH传感器进行数字化实验,分别向两个盛50mL 0.100mol/L 盐酸的烧杯中匀速滴加50mL 去离子水、50mL 0.100mol/L 醋酸铵溶液,滴加过程进行磁力搅拌,测得溶液pH随时间变化如下图所示。已知常温下醋酸铵溶液pH=7,下列说法错误的是


| A.曲线X表示盐酸中加水稀释的pH变化 |
| B.曲线Y的pH变化主要是因为CH3COO-与H+结合成了弱电解质 |
| C.a点对应的溶液中c(Cl-)+c(CH3COO-)+c(CH3COOH)-c(NH4+)=0.01mol/L |
| D.b点对应的溶液中水电离的c(H+)=10-12.86mol/L |
您最近一年使用:0次

 和
和 存在的水溶液中有如下平衡:
存在的水溶液中有如下平衡: 。向某浓度的硫酸铜溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的
。向某浓度的硫酸铜溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的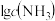 关系如图所示。下列说法正确的是
关系如图所示。下列说法正确的是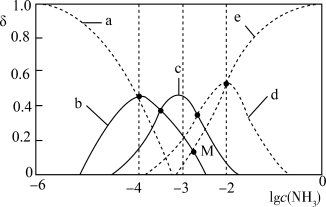

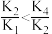
 时,
时,