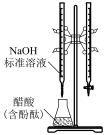
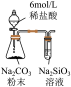
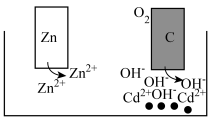
下列实验方案不能达到相应目的的是
| 目的 | A.验证Fe是否被氧化 | B.研究浓度对FeCl3水解平衡的影响 |
| 实验方案 | 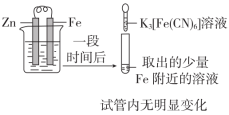 |  |
| 目的 | C.比较CH3COOH和H3BO3(硼酸,一元弱酸)酸性的强弱 | D.比较AgCl和AgI溶解度的大小 |
| 实验方案 |  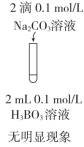 | 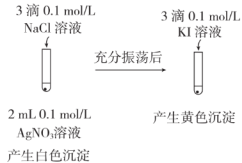 |
| A.A | B.B | C.C | D.D |
22-23高二上·北京西城·期中 查看更多[2]
更新时间:2022-11-19 17:52:36
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 可用饱和 溶液浸泡生锈的青铜器 溶液浸泡生锈的青铜器 |  不稳定,易分解 不稳定,易分解 |
| B | 向蛋白质溶液中加入几滴醋酸铅溶液,有固体析出 | 蛋白质发生了盐析 |
| C | 向 溶液中滴加1滴 溶液中滴加1滴 溶液,再加入稀 溶液,再加入稀 溶液,溶液颜色变浅色 溶液,溶液颜色变浅色 | 其他条件不变,增大产物浓度,平衡向逆反应方向移动 |
| D | 向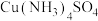 溶液中加入乙醇,析出蓝色晶体[ 溶液中加入乙醇,析出蓝色晶体[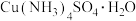 ] ] | 乙醇的极性比水的极性弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验室配制碘水时,通常将I2溶于KI溶液:I2(aq)+I-(aq) I
I (aq)。关于该溶液,下列说法正确的是
(aq)。关于该溶液,下列说法正确的是
 I
I (aq)。关于该溶液,下列说法正确的是
(aq)。关于该溶液,下列说法正确的是| A.滴入淀粉溶液,不变蓝 | B.KI增大了I2的溶解度 |
| C.加少量AgNO3固体平衡正向移动 | D.加水稀释,平衡正向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】等物质的量浓度的下列五种溶液:①CH3COONa,②NH4Cl,③NaHSO4,④Na2CO3,⑤Ba(OH)2,溶液的pH由小到大正确的是
| A.②③①④⑤ | B.③②①④⑤ | C.③①②④⑤ | D.③②④①⑤ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列实验操作、现象和结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 用铂丝蘸取某未知溶液放到无色火焰上灼烧,并透过蓝色钴玻璃观察 | 火焰呈紫色 | 该未知溶液中一定有钾盐 |
| B | 向淀粉溶液中加入稀硫酸,水浴加热后,加入新制氢氧化铜,加热 | 得到蓝色溶液 | 淀粉没有水解 |
| C | 将NaHCO3溶液与NaAlO2溶液混合 | 产生白色沉淀 | 结合H+的能力:CO <AlO <AlO |
| D | 将HI溶液加入Fe(NO3)3溶液中,充分反应后再加入 CCl4混合振荡,静置 | 溶液分层,下层液体显紫红色 | 氧化性:Fe3+>I2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知H2A为二元弱酸,25℃时,用Na2A溶液吸收H2A,且最终吸收H2A的量小于原溶液中Na2A的物质的量,其吸收液pH随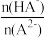 变化的关系如图所示,以下说法不正确的是
变化的关系如图所示,以下说法不正确的是

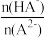 变化的关系如图所示,以下说法不正确的是
变化的关系如图所示,以下说法不正确的是
| A.NaHA溶液中:c(H+)>c(OH-) | B.Na2A溶液中:c(A2-)>c(HA-) |
| C.H2A的第二步电离常数为10-7.2 | D.当吸收液呈中性时:c(Na+)=c(A2-)+c(HA-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列实验操作与实验目的均正确的是
| 选项 | 实验操作 | 实验目的 |
| A | 将5mL0.1mol•L-1Na2S2O3溶液和5mL0.1mol•L-1H2SO4溶液混合后,均分至两支试管,一支放入冷水中,另一支放入热水中,观察现象 | 探究温度对反应速率的影响 |
| B | 向两支分别盛有等浓度的醋酸和硼酸溶液的试管中滴加等浓度的NaHCO3溶液,观察是否产生气泡 | 探究醋酸、碳酸、硼酸的酸性强弱 |
| C | 向盛有5mL0.1mol•L-1AgNO3溶液的试管中先滴加10滴0.1mol•L-1NaCl溶液,再滴加10滴0.1mol•L-1KI溶液,观察是否产生黄色沉淀 | 证明溶解度:AgCl>AgI |
| D | 向5mLFeCl3溶液中加入5滴同浓度的KI溶液,再加入几滴KSCN溶液,溶液显红色 | 证明FeCl3与KI的反应是可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论不正确 的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 探究Fe和S反应特点 | 将适量硫粉和铁粉混合堆成条状。用灼热的玻璃棒触及一端,当混合物呈红热状态时,移开玻璃棒。 | 混合物继续保持红热并持续扩散,粉末呈黑色 | 该反应为放热反应 |
| B | 比较沉淀的Ksp大小 | 向相同浓度和体积的浓氨水中,分别加入等量AgCl和AgI固体,充分搅拌 | 氯化银溶解,碘化银无变化 | Ksp:AgCl>AgI |
| C | 判断平衡移动的方向 | 将装有NO2气体的注射器的活塞缓慢向外拉 | 红棕色逐渐变浅 | 可逆反应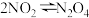 平衡正向移动 平衡正向移动 |
| D | 检验Na2S2O3样品是否含有Na2SO4杂质 | 取少量样品溶于水,先加入过量稀盐酸,过滤,向滤液中滴加少量BaCl2溶液 | 滤液中出现浑浊 | 该样品中含有Na2SO4杂质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】乙醇燃料电池广泛应用于微型电源、能源汽车、家用电源、国防等领域,工作原理如图所示,电池总反应为: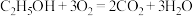 ,下列说法错误的是
,下列说法错误的是

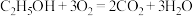 ,下列说法错误的是
,下列说法错误的是
A. 和 和 通入的一极为负极 通入的一极为负极 |
B.正极反应式为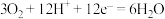 |
C.负极反应式为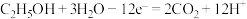 |
D. 从正极经传导质子的固体膜移向负极 从正极经传导质子的固体膜移向负极 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】银锌纽扣电池的电池反应式为:Zn+Ag2O+H2O=Zn(OH)2+2Ag。下列说法不正确的是
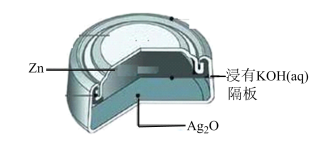

| A.锌作负极,失去电子 |
| B.正极为Ag2O,发生还原反应 |
| C.电池工作时,电子从Ag2O经导线流向Zn |
| D.正极的电极方程式为:Ag2O+2e-+H2O=2Ag+2OH- |
您最近一年使用:0次