全国农村应当在“绿色生态・美丽多彩・低碳节能・循环发展”的理念引导下,更快更好地发展“中国绿色村庄”,参与“亚太国际低碳农庄”建设。试回答下列问题:
(1)碳的单质及其部分化合物是人类生产生活的主要能源物质。
①有机物M经过太阳光光照可转化成N,转化过程如图
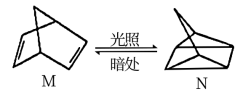
△H=+886kJ/mol,则M、N相比,较稳定的是___ 。
②将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s),△H=-1176kJ/mol,则反应过程中,每转移1mol电子放出的热量为___ 。
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g)⇌Fe(s)+CO2(g),△H>0。已知在1100℃时,该反应的平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值__ (填“增大”、“减小”或“不变”)。
②1100℃时测得高炉中,c(CO2)=0.025mol/L,c(CO)=0.1mol/L,则在这种情况下,该反应是否处于化学平衡状态?___ 。(填“是”或“否”),其判断依据是___ 。
(3)目前工业上可用CO2来生产燃料甲醇,有关反应为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),△H=-50.0kJ/mol。现向容积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
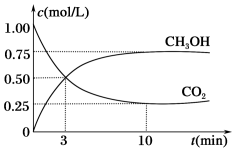
①该反应到达平衡后,H2的转化率α(H2)=____ 。
②下列措施能使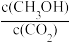 增大的是(填字母)
增大的是(填字母)___ 。
A.升高温度
B.再充入H2
C.再充入CO2
D.将H2O(g)从体系中分离
E.充入He(g),使体系压强增大
③下列各项能作为判断该反应达到化学平衡状态依据的是___ (填字母)。
A.v正(CH3OH)=3v逆(H2)
B.平衡混合物中各组分的含量不再变化
C.CO2和H2的浓度比为1:2
D.混合气体的密度不再变化
(1)碳的单质及其部分化合物是人类生产生活的主要能源物质。
①有机物M经过太阳光光照可转化成N,转化过程如图

△H=+886kJ/mol,则M、N相比,较稳定的是
②将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s),△H=-1176kJ/mol,则反应过程中,每转移1mol电子放出的热量为
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g)⇌Fe(s)+CO2(g),△H>0。已知在1100℃时,该反应的平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值
②1100℃时测得高炉中,c(CO2)=0.025mol/L,c(CO)=0.1mol/L,则在这种情况下,该反应是否处于化学平衡状态?
(3)目前工业上可用CO2来生产燃料甲醇,有关反应为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),△H=-50.0kJ/mol。现向容积为1L的密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。

①该反应到达平衡后,H2的转化率α(H2)=
②下列措施能使
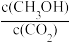 增大的是(填字母)
增大的是(填字母)A.升高温度
B.再充入H2
C.再充入CO2
D.将H2O(g)从体系中分离
E.充入He(g),使体系压强增大
③下列各项能作为判断该反应达到化学平衡状态依据的是
A.v正(CH3OH)=3v逆(H2)
B.平衡混合物中各组分的含量不再变化
C.CO2和H2的浓度比为1:2
D.混合气体的密度不再变化
更新时间:2019-12-20 13:00:44
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】I.基于新材料及3D打印技术,科学家研制出一种微胶囊吸收剂能将工厂排放的CO2以更加安全、廉价和高效的方式处理掉,球形微胶囊内部充入Na2CO3溶液,其原理如图所示。
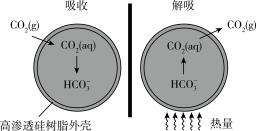
(1)这种微胶囊吸收CO2的原理是_____ (写离子方程式),此过程是_____ (填“吸收”或“放出”)能量的过程。
(2)在吸收过程中关于胶囊内溶液下列说法正确的是_____ 。
(3)将解吸后的CO2催化加氢可制取乙烯。
已知:C2H4(g)+3O2(g)=2CO2(g)+2H2O(g) ΔH=-1323kJ/mol
2H2(g)+O2(g)=2H2O(g) ΔH=-484kJ/mol
写出CO2催化加氢制取乙烯的热化学方程式_____ 。
II.常温下,向20.00mL0.1000mol•L-1H2C2O4溶液中逐滴滴加0.1000mol•L-1NaOH溶液,所得溶液中的H2C2O4、 、
、 的物质的量分数(δ)与pH的关系如图所示(示例:δ(
的物质的量分数(δ)与pH的关系如图所示(示例:δ( )=
)=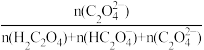 )。
)。
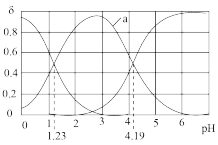
(4)曲线a代表的微粒是_____ (填化学式)。
(5)当滴入NaOH溶液体积为20.00mL时,发生的离子反应方程式为_____ 。
(6)pH=4.19时,3c( )-c(Na+)=
)-c(Na+)=_____ (用计算式表达)。
(7)请用具体数据说明NaHC2O4溶液显酸性的原因:_____ 。

(1)这种微胶囊吸收CO2的原理是
(2)在吸收过程中关于胶囊内溶液下列说法正确的是
A.吸收前溶液中c(Na+)>c( )>c( )>c( )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
B.吸收过程中,体系中的含碳微粒有 、 、 、H2CO3、CO2 、H2CO3、CO2 |
C.当n(CO2)∶n(Na2CO3)=1∶3时,溶液中c( )<c( )<c( ) ) |
D.溶液中始终有c(Na+)+c(H+)=2c( )+c( )+c( )+c(OH-) )+c(OH-) |
已知:C2H4(g)+3O2(g)=2CO2(g)+2H2O(g) ΔH=-1323kJ/mol
2H2(g)+O2(g)=2H2O(g) ΔH=-484kJ/mol
写出CO2催化加氢制取乙烯的热化学方程式
II.常温下,向20.00mL0.1000mol•L-1H2C2O4溶液中逐滴滴加0.1000mol•L-1NaOH溶液,所得溶液中的H2C2O4、
 、
、 的物质的量分数(δ)与pH的关系如图所示(示例:δ(
的物质的量分数(δ)与pH的关系如图所示(示例:δ( )=
)=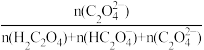 )。
)。
(4)曲线a代表的微粒是
(5)当滴入NaOH溶液体积为20.00mL时,发生的离子反应方程式为
(6)pH=4.19时,3c(
 )-c(Na+)=
)-c(Na+)=(7)请用具体数据说明NaHC2O4溶液显酸性的原因:
您最近一年使用:0次
【推荐2】“加大力度保护自然,实现可持续发展”是第五届联合国环境大会会议主题。工业生产产生的含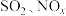 的烟气对环境和人体健康有极大的危害,必须经过处理才可排放。
的烟气对环境和人体健康有极大的危害,必须经过处理才可排放。
(1)在一定条件下,肼( )与
)与 反应能生成
反应能生成 和
和 。
。
已知:①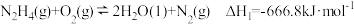 ;
;
②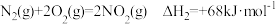 ;
;
③ ;
;
则反应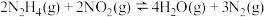 的
的
_______  。
。
(2)在一恒容密闭容器中发生反应: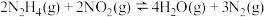 。当温度高于250℃时,正、逆反应速率分别为
。当温度高于250℃时,正、逆反应速率分别为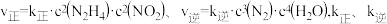 分别为正、逆反应速率常数,
分别为正、逆反应速率常数, 、
、 与该反应的平衡常数
与该反应的平衡常数 之间的关系为
之间的关系为_______ 。速率常数 随温度的升高而增大,则达到平衡后,仅升高温度,
随温度的升高而增大,则达到平衡后,仅升高温度, 增大的倍数
增大的倍数_______ (填“>”、“<”或“=”) 增大的倍数。
增大的倍数。
(3)在一定条件下,利用催化净化技术,CO可将NO2转化为无毒物质反应为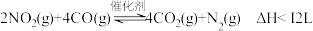 。向两个容积均为2L的恒容密闭容器中均分别充入
。向两个容积均为2L的恒容密闭容器中均分别充入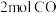 和
和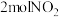 ,分别在220℃和300℃下发生反应。测得两容器中CO或CO2的物质的量随时间的变化关系如图所示,曲线I代表的体系平衡后气体的总压强为
,分别在220℃和300℃下发生反应。测得两容器中CO或CO2的物质的量随时间的变化关系如图所示,曲线I代表的体系平衡后气体的总压强为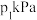 ,曲线II代表的体系平衡后气体的总压强为
,曲线II代表的体系平衡后气体的总压强为 。
。
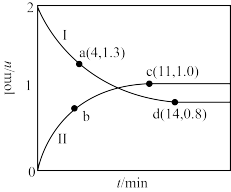
①代表220℃条件下的变化曲线为___ (填“I”或“II”);ad段 的平均反应速率为
的平均反应速率为__  。
。
②下列有关曲线II条件下的反应的说法正确的是_______ (填标号)。
A.当体系中 与
与 的物质的量之比不随时间变化时,反应达到平衡状态
的物质的量之比不随时间变化时,反应达到平衡状态
B.当混合气体的密度不随时间变化时,该反应达到平衡状态
C.体系达到平衡后,升高温度,混合气体的平均相对分子质量增大
D.使用高效催化剂可提高 的转化率
的转化率
③图中a、c、d三点对应的逆反应速率由大到小的顺序为_______ (用a、c、d表示);在曲线II代表的温度下,该反应的平衡常数Kp=_______  (Kp为用平衡分压代替平衡浓度表示的化学平衡常数,分压=总压×物质的量分数)。
(Kp为用平衡分压代替平衡浓度表示的化学平衡常数,分压=总压×物质的量分数)。
 的烟气对环境和人体健康有极大的危害,必须经过处理才可排放。
的烟气对环境和人体健康有极大的危害,必须经过处理才可排放。(1)在一定条件下,肼(
 )与
)与 反应能生成
反应能生成 和
和 。
。已知:①
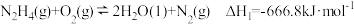 ;
;②
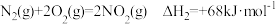 ;
;③
 ;
;则反应
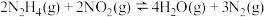 的
的
 。
。(2)在一恒容密闭容器中发生反应:
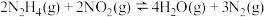 。当温度高于250℃时,正、逆反应速率分别为
。当温度高于250℃时,正、逆反应速率分别为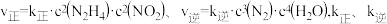 分别为正、逆反应速率常数,
分别为正、逆反应速率常数, 、
、 与该反应的平衡常数
与该反应的平衡常数 之间的关系为
之间的关系为 随温度的升高而增大,则达到平衡后,仅升高温度,
随温度的升高而增大,则达到平衡后,仅升高温度, 增大的倍数
增大的倍数 增大的倍数。
增大的倍数。(3)在一定条件下,利用催化净化技术,CO可将NO2转化为无毒物质反应为
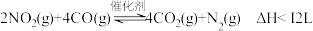 。向两个容积均为2L的恒容密闭容器中均分别充入
。向两个容积均为2L的恒容密闭容器中均分别充入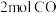 和
和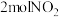 ,分别在220℃和300℃下发生反应。测得两容器中CO或CO2的物质的量随时间的变化关系如图所示,曲线I代表的体系平衡后气体的总压强为
,分别在220℃和300℃下发生反应。测得两容器中CO或CO2的物质的量随时间的变化关系如图所示,曲线I代表的体系平衡后气体的总压强为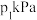 ,曲线II代表的体系平衡后气体的总压强为
,曲线II代表的体系平衡后气体的总压强为 。
。
①代表220℃条件下的变化曲线为
 的平均反应速率为
的平均反应速率为 。
。②下列有关曲线II条件下的反应的说法正确的是
A.当体系中
 与
与 的物质的量之比不随时间变化时,反应达到平衡状态
的物质的量之比不随时间变化时,反应达到平衡状态B.当混合气体的密度不随时间变化时,该反应达到平衡状态
C.体系达到平衡后,升高温度,混合气体的平均相对分子质量增大
D.使用高效催化剂可提高
 的转化率
的转化率③图中a、c、d三点对应的逆反应速率由大到小的顺序为
 (Kp为用平衡分压代替平衡浓度表示的化学平衡常数,分压=总压×物质的量分数)。
(Kp为用平衡分压代替平衡浓度表示的化学平衡常数,分压=总压×物质的量分数)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】CO、NH3、NO2、SO2处理不当易造成环境污染,如果对这些气体加以利用就可以变废为宝。回答下列问题:
(1)硝酸厂常用催化还原法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:I.CH4(g)+ 2O2(g)=CO2(g) +2H2O(l) ΔH1=-890.3kJ·mol-1;
II.N2(g)+ 2O2(g)=2NO2(g) ΔH2= +67.7 kJ·mol-1
则CH4(g) +2NO2(g)=CO2(g) +N2(g)+ 2H2O(l) ΔH=_______ 。
(2)工业上利用NH3生产氢氰酸(HCN)的反应为CH4(g)+NH3(g) ⇌HCN(g)+3H2(g) ΔH>0。
①该反应在_______ (填“较高”或“较低”)温度下能自发进行。
②一定温度下,向2L恒容密闭容器中充入2 mol CH4(g)和2 mol NH3(g),发生上述反应,10 min末达到平衡状态,测得NH3的体积分数为30%。则0~10 min内,用HCN的浓度变化表示的平均反应速率为_______ ;CH4的平衡转化率为_______ ;该温度下,该反应的平衡常数K=_______ ( mol/L)2
(3)在催化剂作用下,CO还原NO2进行汽车尾气处理:2NO2(g) + 4CO(g) ⇌4CO2(g)+ N2(g) ΔH<0。
①相同条件下,选用A、B、C三种催化剂进行反应,生成N2的物质的量随时间的变化如图1所示。活化能最小的是_______ [填“E(A)” “E(B)”或“E(C)”]。
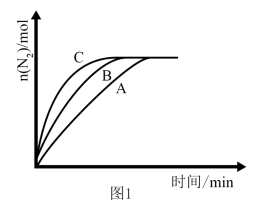
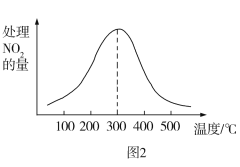
②在催化剂B作用下,测得相同时间内,处理NO2的量与温度的关系如图2所示。温度高于300℃,处理NO2的量随温度升高而减小的原因为(假设该温度范围内催化效率相同)_______ 。
(4)煤燃烧产生的SO2可用足量NaOH溶液吸收生成Na2SO3,Na2SO3溶液中各离子浓度由大到小的顺序为_______ 。
(1)硝酸厂常用催化还原法处理尾气。CH4在催化条件下可以将NO2还原为N2。
已知:I.CH4(g)+ 2O2(g)=CO2(g) +2H2O(l) ΔH1=-890.3kJ·mol-1;
II.N2(g)+ 2O2(g)=2NO2(g) ΔH2= +67.7 kJ·mol-1
则CH4(g) +2NO2(g)=CO2(g) +N2(g)+ 2H2O(l) ΔH=
(2)工业上利用NH3生产氢氰酸(HCN)的反应为CH4(g)+NH3(g) ⇌HCN(g)+3H2(g) ΔH>0。
①该反应在
②一定温度下,向2L恒容密闭容器中充入2 mol CH4(g)和2 mol NH3(g),发生上述反应,10 min末达到平衡状态,测得NH3的体积分数为30%。则0~10 min内,用HCN的浓度变化表示的平均反应速率为
(3)在催化剂作用下,CO还原NO2进行汽车尾气处理:2NO2(g) + 4CO(g) ⇌4CO2(g)+ N2(g) ΔH<0。
①相同条件下,选用A、B、C三种催化剂进行反应,生成N2的物质的量随时间的变化如图1所示。活化能最小的是

②在催化剂B作用下,测得相同时间内,处理NO2的量与温度的关系如图2所示。温度高于300℃,处理NO2的量随温度升高而减小的原因为(假设该温度范围内催化效率相同)

(4)煤燃烧产生的SO2可用足量NaOH溶液吸收生成Na2SO3,Na2SO3溶液中各离子浓度由大到小的顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】催化还原CO2是解决温室效应及能源问题的重要手段之一。研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO。反应的热化学方程式如下:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1 I
CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1 I
CO2(g)+H2(g) CO(g)+H2O(g) ΔH2 II
CO(g)+H2O(g) ΔH2 II
某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l)=H2O(g) ΔH3=44.0kJ·mol-1
请回答(不考虑温度对ΔH的影响):
(1)反应I的平衡常数表达式K=___ ;
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有___ 。
A.使用催化剂Cat.1
B.使用催化剂Cat.2
C.降低反应温度
D.投料比不变,增加反应物的浓度
E.增大CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是___ 。
(4)在图中分别画出反应I在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程~能量”示意图 ___ 。

CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1 I
CH3OH(g)+H2O(g) ΔH1=-53.7kJ·mol-1 ICO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2 II
CO(g)+H2O(g) ΔH2 II某实验室控制CO2和H2初始投料比为1:2.2,在相同压强下,经过相同反应时间测得如下实验数据:
| T(K) | 催化剂 | CO2转化率(%) | 甲醇选择性(%) |
| 543 | Cat.1 | 12.3 | 42.3 |
| 543 | Cat.2 | 10.9 | 72.7 |
| 553 | Cat.1 | 15.3 | 39.1 |
| 553 | Cat.2 | 12.0 | 71.6 |
【备注】Cat.1:Cu/ZnO纳米棒;Cat.2:Cu/ZnO纳米片;甲醇选择性:转化的CO2中生成甲醇的百分比
已知:①CO和H2的标准燃烧热分别为-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l)=H2O(g) ΔH3=44.0kJ·mol-1
请回答(不考虑温度对ΔH的影响):
(1)反应I的平衡常数表达式K=
(2)有利于提高CO2转化为CH3OH平衡转化率的措施有
A.使用催化剂Cat.1
B.使用催化剂Cat.2
C.降低反应温度
D.投料比不变,增加反应物的浓度
E.增大CO2和H2的初始投料比
(3)表中实验数据表明,在相同温度下不同的催化剂对CO2转化成CH3OH的选择性有显著的影响,其原因是
(4)在图中分别画出反应I在无催化剂、有Cat.1和有Cat.2三种情况下“反应过程~能量”

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】以钛铁矿(主要成分 ,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如下,其中钛铁矿与浓硫酸发生反应的化学方程式为:
,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如下,其中钛铁矿与浓硫酸发生反应的化学方程式为: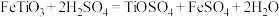 。
。
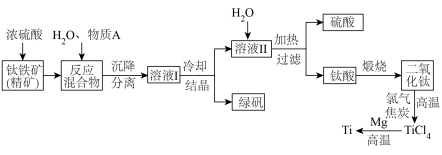
回答下列问题:
(1)钛铁矿和浓硫酸反应属于___________ (选填“氧化还原反应”或“非氧化还原反应”)。
(2)上述生产流程中加入物质A的目的是防止 被氧化,物质A是
被氧化,物质A是___________ ,上述制备 的过程中,所得到的副产物和可回收利用的物质分别是
的过程中,所得到的副产物和可回收利用的物质分别是___________ 、___________ 。
(3)反应 在Ar气氛中进行的理由是
在Ar气氛中进行的理由是___________ 。
(4)由二氧化钛制取四氯化钛所涉及的反应有:
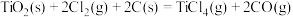
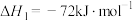

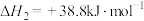

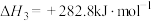
反应 的
的
___________ 。
 ,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如下,其中钛铁矿与浓硫酸发生反应的化学方程式为:
,钛酸亚铁)为主要原料冶炼金属钛,生产的工艺流程图如下,其中钛铁矿与浓硫酸发生反应的化学方程式为: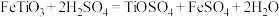 。
。
回答下列问题:
(1)钛铁矿和浓硫酸反应属于
(2)上述生产流程中加入物质A的目的是防止
 被氧化,物质A是
被氧化,物质A是 的过程中,所得到的副产物和可回收利用的物质分别是
的过程中,所得到的副产物和可回收利用的物质分别是(3)反应
 在Ar气氛中进行的理由是
在Ar气氛中进行的理由是(4)由二氧化钛制取四氯化钛所涉及的反应有:
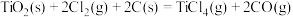
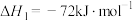

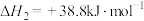

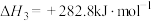
反应
 的
的
您最近一年使用:0次
【推荐3】以NOx为主要成分的雾霾的综合治理是当前重要的研究课题。
(1)已知: 2C(s) + O2(g) = 2CO(g) ∆H1= a kJ/mol
N2(g) + O2(g) = 2NO(g) ∆H2= b kJ/mol
2NO(g) + 2CO(g) =2CO2(g) + N2(g) ∆H3= c kJ/mol
则 2NO(g) + C(s) = CO2(g) + N2(g) ∆H=_______ kJ/mol
(2)NO和CO均为汽车尾气的成分,在催化转换器中二者可发生反应减少尾气污染。
已知2NO(g)+2CO(g) N2(g)+2CO2(g) ∆H<0。
N2(g)+2CO2(g) ∆H<0。
①在500℃时,向恒容密闭体系中通入1mol的NO和1mol的CO进行反应时,下列描述能说明反应达到平衡状态的是_______ 。
A. (CO)正 = 2
(CO)正 = 2 (N2)逆
(N2)逆
B.体系中混合气体密度不变
C.混合气体的平均相对分子质量不变
D.体系中NO、CO的浓度相等
E.单位时间内消耗nmol的NO同时消耗nmol的N2
②向1L密闭容器中通入1mol的NO和1mol的CO气体,在不同温度下反应达到平衡时,NO的平衡转化率随压强变化曲线如图所示:

T1_______ T2(填“>”、“<”),理由是_______ 。M点时混合气体中CO的体积分数为_______ 。
③一定温度下,向恒容容器中通入等物质的量的NO和CO气体,测得容器中压强随时间的变化关系如表所示:
该反应条件下的平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数),该反应中的 正=k正·p2(NO)p2(CO),
正=k正·p2(NO)p2(CO), 逆=k逆·p(N2)p2(CO2),则该反应达到平衡时,k正
逆=k逆·p(N2)p2(CO2),则该反应达到平衡时,k正_______ k逆(填“>”、“<”或“=”)。
(1)已知: 2C(s) + O2(g) = 2CO(g) ∆H1= a kJ/mol
N2(g) + O2(g) = 2NO(g) ∆H2= b kJ/mol
2NO(g) + 2CO(g) =2CO2(g) + N2(g) ∆H3= c kJ/mol
则 2NO(g) + C(s) = CO2(g) + N2(g) ∆H=
(2)NO和CO均为汽车尾气的成分,在催化转换器中二者可发生反应减少尾气污染。
已知2NO(g)+2CO(g)
 N2(g)+2CO2(g) ∆H<0。
N2(g)+2CO2(g) ∆H<0。①在500℃时,向恒容密闭体系中通入1mol的NO和1mol的CO进行反应时,下列描述能说明反应达到平衡状态的是
A.
 (CO)正 = 2
(CO)正 = 2 (N2)逆
(N2)逆 B.体系中混合气体密度不变
C.混合气体的平均相对分子质量不变
D.体系中NO、CO的浓度相等
E.单位时间内消耗nmol的NO同时消耗nmol的N2
②向1L密闭容器中通入1mol的NO和1mol的CO气体,在不同温度下反应达到平衡时,NO的平衡转化率随压强变化曲线如图所示:

T1
③一定温度下,向恒容容器中通入等物质的量的NO和CO气体,测得容器中压强随时间的变化关系如表所示:
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| p/kPa | 200 | 185 | 173 | 165 | 160 | 160 |
 正=k正·p2(NO)p2(CO),
正=k正·p2(NO)p2(CO), 逆=k逆·p(N2)p2(CO2),则该反应达到平衡时,k正
逆=k逆·p(N2)p2(CO2),则该反应达到平衡时,k正
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】 是大气污染物之一,主要来源于工业烟气及汽车尾气等。除去
是大气污染物之一,主要来源于工业烟气及汽车尾气等。除去 的方法统称为脱硝,一般有干法脱硝[选择性催化剂法(SCR)]、湿法脱硝等。
的方法统称为脱硝,一般有干法脱硝[选择性催化剂法(SCR)]、湿法脱硝等。
请完成下列问题:
(1)汽车发动机工作时会引发反应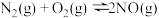 。2000K时,向固定容积的密闭容器中充入等物质的量的
。2000K时,向固定容积的密闭容器中充入等物质的量的 、
、 发生上述反应,各组分体积分数
发生上述反应,各组分体积分数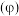 的变化如图1所示。
的变化如图1所示。 的平衡转化率为
的平衡转化率为___________ 。
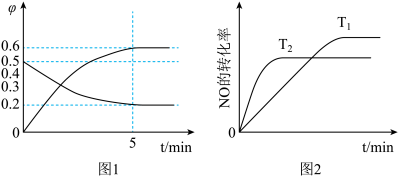
(2)在密闭、固定容积的容器中,一定量NO发生分解的过程中,NO的转化率随时间变化关系如图2所示。
①反应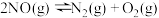
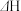
___________ 0(填“>”或“<”)。
②一定温度下,能说明反应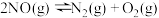 已达到化学平衡的
已达到化学平衡的___________ (填序号)。
a.容器内的压强不发生变化 b.混合气体的密度不发生变化
c.NO、 、
、 的浓度保持不变 d.
的浓度保持不变 d.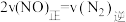
(3)干法脱硝:SCR(选择性催化剂法)技术可有效降低柴油发动机在空气过量条件下的NO排放。其工作原理如下:
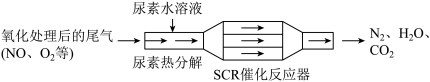
①尿素 水溶液热分解为
水溶液热分解为 和
和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
②加热条件下,反应器中 还原NO的化学方程式为
还原NO的化学方程式为___________ 。
(4)湿法脱硝:采用 溶液作为吸收剂可对烟气进行脱硝。323K下,向足量碱性
溶液作为吸收剂可对烟气进行脱硝。323K下,向足量碱性 溶液中通入含NO的烟气,充分反应后,溶液中离子浓度的分析结果如下表:
溶液中通入含NO的烟气,充分反应后,溶液中离子浓度的分析结果如下表:
① 中心原子的杂化轨道类型为
中心原子的杂化轨道类型为___________ , 的空间构型为
的空间构型为___________ 。 溶液显碱性,用离子方程式解释原因
溶液显碱性,用离子方程式解释原因___________ 。
②依据表中数据,写出 溶液脱硝过程中发生总反应的离子方程式
溶液脱硝过程中发生总反应的离子方程式___________ 。
 是大气污染物之一,主要来源于工业烟气及汽车尾气等。除去
是大气污染物之一,主要来源于工业烟气及汽车尾气等。除去 的方法统称为脱硝,一般有干法脱硝[选择性催化剂法(SCR)]、湿法脱硝等。
的方法统称为脱硝,一般有干法脱硝[选择性催化剂法(SCR)]、湿法脱硝等。请完成下列问题:
(1)汽车发动机工作时会引发反应
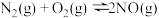 。2000K时,向固定容积的密闭容器中充入等物质的量的
。2000K时,向固定容积的密闭容器中充入等物质的量的 、
、 发生上述反应,各组分体积分数
发生上述反应,各组分体积分数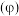 的变化如图1所示。
的变化如图1所示。 的平衡转化率为
的平衡转化率为
(2)在密闭、固定容积的容器中,一定量NO发生分解的过程中,NO的转化率随时间变化关系如图2所示。
①反应
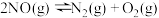
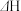
②一定温度下,能说明反应
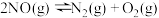 已达到化学平衡的
已达到化学平衡的a.容器内的压强不发生变化 b.混合气体的密度不发生变化
c.NO、
 、
、 的浓度保持不变 d.
的浓度保持不变 d.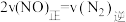
(3)干法脱硝:SCR(选择性催化剂法)技术可有效降低柴油发动机在空气过量条件下的NO排放。其工作原理如下:

①尿素
 水溶液热分解为
水溶液热分解为 和
和 ,该反应的化学方程式为
,该反应的化学方程式为②加热条件下,反应器中
 还原NO的化学方程式为
还原NO的化学方程式为(4)湿法脱硝:采用
 溶液作为吸收剂可对烟气进行脱硝。323K下,向足量碱性
溶液作为吸收剂可对烟气进行脱硝。323K下,向足量碱性 溶液中通入含NO的烟气,充分反应后,溶液中离子浓度的分析结果如下表:
溶液中通入含NO的烟气,充分反应后,溶液中离子浓度的分析结果如下表:| 离子 |  |  |  |
 | 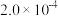 |  | 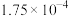 |
①
 中心原子的杂化轨道类型为
中心原子的杂化轨道类型为 的空间构型为
的空间构型为 溶液显碱性,用离子方程式解释原因
溶液显碱性,用离子方程式解释原因②依据表中数据,写出
 溶液脱硝过程中发生总反应的离子方程式
溶液脱硝过程中发生总反应的离子方程式
您最近一年使用:0次
【推荐2】本题为《化学反应原理(选修4)》选做题。
(l)T℃时,在1L密闭容器中A气体与B气体反应生成C气体。反应过程中A、B、C的浓度随时间t的变化如图所示。

该反应的化学方程式为____________
(2)一定条件下,上述反应达到化学平衡状态的标志是_____ (填字母代号)。
A.v(正)=v(逆)=0
B.各物质的浓度不再变化
C.单位时间内消耗1molA,同时生成3molB
(3)若该反应放出热量,升高温度时,化学反应速率______ (填“增大”或“减小”),平衡向______ (填“正”或“逆”)反应方向移动。
(4)下图是电解NaCl溶液的示意图。请回答下列问题:
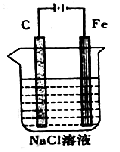
① 石墨电极上的反应式为_____________ ;
② 电解一段时间后,溶液的pH______ (填“增大”“减小”或“不变”)。
(5)水溶液中的离子平衡是化学反应原理的重要内容。请回答下列问题:
① 常温下,0.1mol/LNH4Cl溶液呈______ (填“酸”“碱”或“中”)性,溶液中c(NH4+)____ c(Cl-)(填“>”“< ”或“=”);
② 已知:20℃时,Ksp(AgCl)=1.1×10-10, Ksp(AgBr)=2.0×10-13。在浓度均为0.01mol/L的NaCl和NaBr混合溶液中,逐滴加入AgNO3溶液,先产生的沉淀是_____ (填“AgCl”或“AgBr ”)。
(l)T℃时,在1L密闭容器中A气体与B气体反应生成C气体。反应过程中A、B、C的浓度随时间t的变化如图所示。

该反应的化学方程式为
(2)一定条件下,上述反应达到化学平衡状态的标志是
A.v(正)=v(逆)=0
B.各物质的浓度不再变化
C.单位时间内消耗1molA,同时生成3molB
(3)若该反应放出热量,升高温度时,化学反应速率
(4)下图是电解NaCl溶液的示意图。请回答下列问题:

① 石墨电极上的反应式为
② 电解一段时间后,溶液的pH
(5)水溶液中的离子平衡是化学反应原理的重要内容。请回答下列问题:
① 常温下,0.1mol/LNH4Cl溶液呈
② 已知:20℃时,Ksp(AgCl)=1.1×10-10, Ksp(AgBr)=2.0×10-13。在浓度均为0.01mol/L的NaCl和NaBr混合溶液中,逐滴加入AgNO3溶液,先产生的沉淀是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】汽车尾气中排放的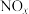 和CO污染环境,在汽车尾气系统装置中安装催化转化器,可有效降低
和CO污染环境,在汽车尾气系统装置中安装催化转化器,可有效降低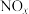 和CO的排放。
和CO的排放。
I.实验室为了模拟反应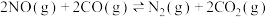 在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用现代传感技术测得不同时间NO和CO的浓度如下表:
在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用现代传感技术测得不同时间NO和CO的浓度如下表:
(1)前2s的平均反应速率
_______ ;
(2)能说明上述反应达到平衡状态的是_______ (填字母)。
a.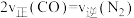 b.
b. c.容器内压强不变
c.容器内压强不变
d.混合气体密度不变 e.混合气体的平均相对分子质量不变
II.某硝酸厂处理尾气中NO的方法:催化剂存在时用 将NO还原为N2。已知:
将NO还原为N2。已知:
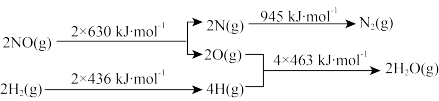
(3)则1mol 和2mol水蒸气反应生成氢气和一氧化氮的过程
和2mol水蒸气反应生成氢气和一氧化氮的过程_______ (填“吸收”或“释放”)_______ kJ能量。
III.燃料电池是一种高效、安全环保的供电装置,以CO作燃料的电池,如下图所示:
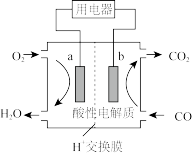
(4)负极反应物是_______ , 从
从_______ (填“a”或“b”,下同)极移动到_______ 极。
(5)正极反应式为_______ 。
 和CO污染环境,在汽车尾气系统装置中安装催化转化器,可有效降低
和CO污染环境,在汽车尾气系统装置中安装催化转化器,可有效降低 和CO的排放。
和CO的排放。I.实验室为了模拟反应
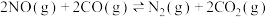 在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用现代传感技术测得不同时间NO和CO的浓度如下表:
在催化转化器内的工作情况,控制一定条件,让反应在恒容密闭容器中进行,用现代传感技术测得不同时间NO和CO的浓度如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
 | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
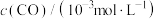 | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
(1)前2s的平均反应速率

(2)能说明上述反应达到平衡状态的是
a.
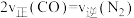 b.
b. c.容器内压强不变
c.容器内压强不变 d.混合气体密度不变 e.混合气体的平均相对分子质量不变
II.某硝酸厂处理尾气中NO的方法:催化剂存在时用
 将NO还原为N2。已知:
将NO还原为N2。已知: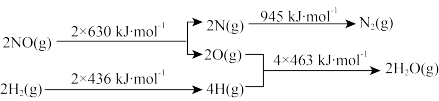
(3)则1mol
 和2mol水蒸气反应生成氢气和一氧化氮的过程
和2mol水蒸气反应生成氢气和一氧化氮的过程III.燃料电池是一种高效、安全环保的供电装置,以CO作燃料的电池,如下图所示:

(4)负极反应物是
 从
从(5)正极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】为探究原电池和电解池的工作原理,某研究性学习小组分别用如图所示装置进行实验。
Ⅰ.用图1甲装置进行第一组实验:
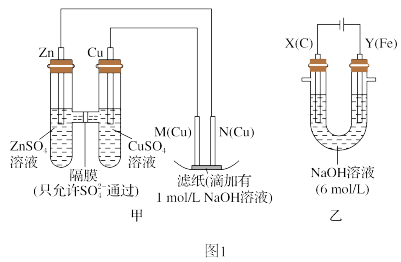
(1)实验过程中,
_______ (填“从左向右”、“从右向左”或“不”)移动。
(2)电极M处滤纸上可观察到的现象是_______ 。
(3)该小组同学用图1乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子( )在溶液中呈紫红色。
)在溶液中呈紫红色。
①电解过程中,Y极发生的电极反应为 和
和_______ 。
②电解一段时间后,若在X极收集到672mL气体,Y电极(铁电极)质量减小0.28g,则在Y极收集到的气体体积为_______ mL(气体均为标准状况下的体积)。
Ⅱ.某同学设计如图2所示燃料电池探究氯碱工业原理和粗铜的精炼原理:
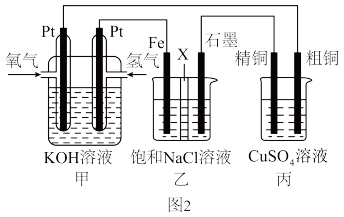
(4)下列说法正确的是_______(填字母)。
(5)如果粗铜中含有锌,银等杂质,丙装置中反应一段时间后,硫酸铜溶液浓度将_______ (填“增大”、“减小”或“不变”)。若在标准状况下,有224mL氧气参加反应,则丙装置中阴极析出铜的质量为_______ g。
Ⅲ.以铬酸钾( )为原料,用电化学法制备重铬酸钾的实验装置如图3所示(已知
)为原料,用电化学法制备重铬酸钾的实验装置如图3所示(已知
 ):
):
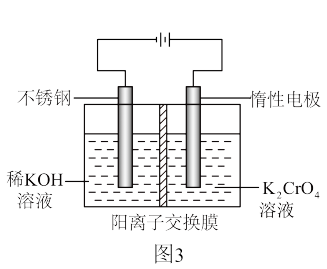
(6)分析阳极区能得到重铬酸钾溶液的原因_______ 。
(7)电解一段时间后,测得阳极区溶液中 物质的量由a mol变为b mol,则此时铬酸钾的转化率为
物质的量由a mol变为b mol,则此时铬酸钾的转化率为_______ 。
Ⅰ.用图1甲装置进行第一组实验:

(1)实验过程中,

(2)电极M处滤纸上可观察到的现象是
(3)该小组同学用图1乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子(
 )在溶液中呈紫红色。
)在溶液中呈紫红色。①电解过程中,Y极发生的电极反应为
 和
和②电解一段时间后,若在X极收集到672mL气体,Y电极(铁电极)质量减小0.28g,则在Y极收集到的气体体积为
Ⅱ.某同学设计如图2所示燃料电池探究氯碱工业原理和粗铜的精炼原理:

(4)下列说法正确的是_______(填字母)。
| A.装置甲中通入氢气的电极为正极,装置乙中石墨电极为阳极 |
B.装置甲中负极的电极反应式为 |
| C.反应一段时间后,在乙装置中滴入酚酞溶液,铁极区的溶液先变红 |
| D.若用隔膜法电解饱和食盐水生成NaClO,则X应为阳离子交换膜 |
Ⅲ.以铬酸钾(
 )为原料,用电化学法制备重铬酸钾的实验装置如图3所示(已知
)为原料,用电化学法制备重铬酸钾的实验装置如图3所示(已知
 ):
):
(6)分析阳极区能得到重铬酸钾溶液的原因
(7)电解一段时间后,测得阳极区溶液中
 物质的量由a mol变为b mol,则此时铬酸钾的转化率为
物质的量由a mol变为b mol,则此时铬酸钾的转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】二氧化碳是用途非常广泛的化工基础原料,回答下列问题:
(1)工业上可以用CO2来生产燃料甲醇。已知:
CO2(g) + 3H2(g) CH3OH(l) + H2O(l) ΔH1 = -131.0 kJ·mol−1
CH3OH(l) + H2O(l) ΔH1 = -131.0 kJ·mol−1
H2(g) + O2(g) = H2O(l) ΔH2 = -285.8 kJ·mol−1
O2(g) = H2O(l) ΔH2 = -285.8 kJ·mol−1
则CH3OH的燃烧热ΔH =________________ 。
(2)在催化剂作用下,CO2和CH4可以直接转化为乙酸:CO2(g) + CH4(g) CH3COOH(g) ΔH = +36.0 kJ·mol−1
CH3COOH(g) ΔH = +36.0 kJ·mol−1
欲使乙酸的平衡产率提高,应采取的措施是__________ (填标号)。
A.升高温度 B.降低温度 C.增大压强 D.降低压强
(3)高温下,CO2与足量的碳在密闭容器中实现反应:C(s) + CO2(g) 2CO(g)。
2CO(g)。
① 该反应的平衡常数表达式K =_____________ 。
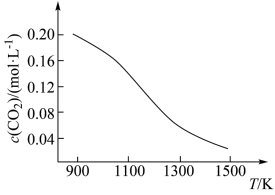
② 向容积为1 L的恒容容器中加入足量的碳和0.2 mol CO2,在不同温度下达到平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示。则该反应为__________ (填“放热”或“吸热”)反应。某温度下,若向该平衡体系中再通入0.2 mol CO2,达到新平衡后,体系中CO的百分含量______________ (填“变大”或“变小”或“不变”,下同),平衡常数__________ 。
(1)工业上可以用CO2来生产燃料甲醇。已知:
CO2(g) + 3H2(g)
 CH3OH(l) + H2O(l) ΔH1 = -131.0 kJ·mol−1
CH3OH(l) + H2O(l) ΔH1 = -131.0 kJ·mol−1H2(g) +
 O2(g) = H2O(l) ΔH2 = -285.8 kJ·mol−1
O2(g) = H2O(l) ΔH2 = -285.8 kJ·mol−1则CH3OH的燃烧热ΔH =
(2)在催化剂作用下,CO2和CH4可以直接转化为乙酸:CO2(g) + CH4(g)
 CH3COOH(g) ΔH = +36.0 kJ·mol−1
CH3COOH(g) ΔH = +36.0 kJ·mol−1欲使乙酸的平衡产率提高,应采取的措施是
A.升高温度 B.降低温度 C.增大压强 D.降低压强
(3)高温下,CO2与足量的碳在密闭容器中实现反应:C(s) + CO2(g)
 2CO(g)。
2CO(g)。① 该反应的平衡常数表达式K =
② 向容积为1 L的恒容容器中加入足量的碳和0.2 mol CO2,在不同温度下达到平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示。则该反应为

您最近一年使用:0次
【推荐3】羰基硫(COS)广泛存在于煤、石油和天然气为原料的化工生产中,不经处理直接排放会引起大气污染,石油化工中产生的羰基硫可通过以下方法脱除。
Ⅰ.干法脱除:在催化剂存在下,COS和H2可发生两个平行反应:
i. COS(g)+H2(g) H2S(g)+CO(g)△H1=-17kJ/mol
H2S(g)+CO(g)△H1=-17kJ/mol
ii. COS(g)+4H2(g) H2S(g)+CH4(g)+H2O(g) △H2
H2S(g)+CH4(g)+H2O(g) △H2
(1)已知:CH4(g)+H2O(g) CO(g)+3H2(g)△H=+206kJ/mol,则△H2=
CO(g)+3H2(g)△H=+206kJ/mol,则△H2=______________ 。
(2)T1℃时,向10L恒容密闭容器中充人1molCOS和4molH2,发生反应i和ii。5min时达到平衡,测得体系压强减少了20%,CO的体积分数为10%且其平衡分压为P1。
①0-5min内,v(COS)=______________ 。
②反应i的平衡常数K=______________ 。
③若在起始温度为T1℃的绝热容器中重复上述实验,H2的平衡分压P2______________ P1(填“>”“=”或“<”),理由为______________ 。
Ⅱ.湿法脱除:原理为COS+4OH-=S2-+CO32-+2H2O。温度为293K时,将COS以固定流速匀速通入一定浓度的NaOH溶液中,测得体系内c(S2-)随时间(t)的变化如图所示:
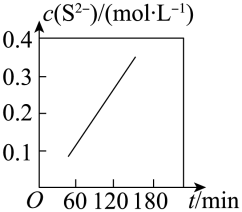
(3)由图可知,增大NaOH溶液的初始浓度,COS的吸收速率______________ (填“增大”“减小”或“不变”),判断依据为______________ 。
(4)在上述反应体系中同时加入少量溴水,也能吸收COS并得到澄清溶液,发生反应的化学方程式为______________ 。
Ⅰ.干法脱除:在催化剂存在下,COS和H2可发生两个平行反应:
i. COS(g)+H2(g)
 H2S(g)+CO(g)△H1=-17kJ/mol
H2S(g)+CO(g)△H1=-17kJ/molii. COS(g)+4H2(g)
 H2S(g)+CH4(g)+H2O(g) △H2
H2S(g)+CH4(g)+H2O(g) △H2(1)已知:CH4(g)+H2O(g)
 CO(g)+3H2(g)△H=+206kJ/mol,则△H2=
CO(g)+3H2(g)△H=+206kJ/mol,则△H2=(2)T1℃时,向10L恒容密闭容器中充人1molCOS和4molH2,发生反应i和ii。5min时达到平衡,测得体系压强减少了20%,CO的体积分数为10%且其平衡分压为P1。
①0-5min内,v(COS)=
②反应i的平衡常数K=
③若在起始温度为T1℃的绝热容器中重复上述实验,H2的平衡分压P2
Ⅱ.湿法脱除:原理为COS+4OH-=S2-+CO32-+2H2O。温度为293K时,将COS以固定流速匀速通入一定浓度的NaOH溶液中,测得体系内c(S2-)随时间(t)的变化如图所示:

(3)由图可知,增大NaOH溶液的初始浓度,COS的吸收速率
(4)在上述反应体系中同时加入少量溴水,也能吸收COS并得到澄清溶液,发生反应的化学方程式为
您最近一年使用:0次



