我国力争于2030年前实现碳达峰,2060年前实现碳中和,在这种背景下,CO2的利用和转化成为研究重点。回答下列问题:
(1)2021年9月,我国科学家在《科学》杂志发表了二氧化碳人工合成淀粉的研究成果。合成淀粉的重要反应包括二氧化碳制备甲醇的反应: ,该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态):
,该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态):

使用催化剂的曲线是___________ (填“甲”或“乙”),催化剂可使反应历程中决速步骤的活化能降低___________ eV,达到化学平衡后再降低温度,平衡___________ (填“正向”“逆向”或“不”)移动。
(2)一定条件下,向某密闭容器中通入x mol CO2,y mol H2,在催化剂存在下发生反应: 。
。
①恒压条件下,当x:y=___________ 时,平衡体系中CH3OH的体积分数最大。
②恒容条件下,当x=2,y=6,温度为T1K时,反应起始压强为8MPa,经10min,反应达到平衡状态,CO2的平衡转化率为50%。则T1K时平衡常数Kp=___________ 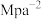 (Kp为以分压表示的平衡常数,分压=总压×物质的量分数),0~10 min内,v(H2)=
(Kp为以分压表示的平衡常数,分压=总压×物质的量分数),0~10 min内,v(H2)=___________  。
。
(1)2021年9月,我国科学家在《科学》杂志发表了二氧化碳人工合成淀粉的研究成果。合成淀粉的重要反应包括二氧化碳制备甲醇的反应:
 ,该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态):
,该反应在有催化剂和无催化剂作用下的反应机理如图所示(其中标有*的为吸附在催化剂表面上的物种,TS为过渡态):
使用催化剂的曲线是
(2)一定条件下,向某密闭容器中通入x mol CO2,y mol H2,在催化剂存在下发生反应:
 。
。①恒压条件下,当x:y=
②恒容条件下,当x=2,y=6,温度为T1K时,反应起始压强为8MPa,经10min,反应达到平衡状态,CO2的平衡转化率为50%。则T1K时平衡常数Kp=
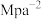 (Kp为以分压表示的平衡常数,分压=总压×物质的量分数),0~10 min内,v(H2)=
(Kp为以分压表示的平衡常数,分压=总压×物质的量分数),0~10 min内,v(H2)= 。
。
更新时间:2023-08-11 23:46:57
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】化学家一直致力于对化学反应进行的方向、限度和速率进行研究,寻找合适理论对其进行解释。
I.为了治理汽车尾气污染(含有NO、CO、烃类等),科学家设计在汽车排气管上装上催化剂发生如下反应:2NO(g)+2CO(g) N2(g)+2CO2(g)。某温度下,向体积为1L的密闭容器中充入NO、CO各0.1mol,平衡时NO的转化率为60%,计算该反应的平衡常数K=
N2(g)+2CO2(g)。某温度下,向体积为1L的密闭容器中充入NO、CO各0.1mol,平衡时NO的转化率为60%,计算该反应的平衡常数K=______________ ;此反应常温下能够自发进行的原因是_______________________ 。
Ⅱ.右图是高锰酸钾酸性溶液与草酸发生反应的有关图象,溶液体积为500mL。
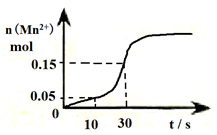
(1)该反应在10-30s的化学反应速率v(Mn2+)=________________________ 。
(2)请写出该反应的离子方程式____________________________________________________ 。
(3)观察图象说明在一定温度下反应速率起始缓慢然后加快的原因______________________ 。
Ⅲ.难溶电解质FeS在水溶液中存在着溶解平衡:FeS(s) Fe2+(aq) + S2-(aq),在一定温度下,Ksp=c(Fe2+)·c(S2-)=6.25×10-18;在该温度下,氢硫酸饱和溶液中存在c2(H+)·c(S2-)=1.0×10-22。将适量FeCl2投入氢硫酸饱和溶液中,欲使溶液中c(Fe2+)=1.0 mol·L-1,应调节溶液的c(H+)=
Fe2+(aq) + S2-(aq),在一定温度下,Ksp=c(Fe2+)·c(S2-)=6.25×10-18;在该温度下,氢硫酸饱和溶液中存在c2(H+)·c(S2-)=1.0×10-22。将适量FeCl2投入氢硫酸饱和溶液中,欲使溶液中c(Fe2+)=1.0 mol·L-1,应调节溶液的c(H+)=_______ 。
IV.氢硫酸中H2S是分步电离的,H2S H++ HS-K1=1.3×10-7,HS-
H++ HS-K1=1.3×10-7,HS- H++ S2-K2=7.1×10-15欲使溶液中c(S2-)浓度增大,应采取的措施有
H++ S2-K2=7.1×10-15欲使溶液中c(S2-)浓度增大,应采取的措施有_____________ 。
A.加入NaOH B.加入CuSO4C.适当降低温度D.通入过量SO2E.加入Na2CO3(H2CO3电离常数K1=4.4×10-7,K2=4.7×10-11)
I.为了治理汽车尾气污染(含有NO、CO、烃类等),科学家设计在汽车排气管上装上催化剂发生如下反应:2NO(g)+2CO(g)
 N2(g)+2CO2(g)。某温度下,向体积为1L的密闭容器中充入NO、CO各0.1mol,平衡时NO的转化率为60%,计算该反应的平衡常数K=
N2(g)+2CO2(g)。某温度下,向体积为1L的密闭容器中充入NO、CO各0.1mol,平衡时NO的转化率为60%,计算该反应的平衡常数K=Ⅱ.右图是高锰酸钾酸性溶液与草酸发生反应的有关图象,溶液体积为500mL。

(1)该反应在10-30s的化学反应速率v(Mn2+)=
(2)请写出该反应的离子方程式
(3)观察图象说明在一定温度下反应速率起始缓慢然后加快的原因
Ⅲ.难溶电解质FeS在水溶液中存在着溶解平衡:FeS(s)
 Fe2+(aq) + S2-(aq),在一定温度下,Ksp=c(Fe2+)·c(S2-)=6.25×10-18;在该温度下,氢硫酸饱和溶液中存在c2(H+)·c(S2-)=1.0×10-22。将适量FeCl2投入氢硫酸饱和溶液中,欲使溶液中c(Fe2+)=1.0 mol·L-1,应调节溶液的c(H+)=
Fe2+(aq) + S2-(aq),在一定温度下,Ksp=c(Fe2+)·c(S2-)=6.25×10-18;在该温度下,氢硫酸饱和溶液中存在c2(H+)·c(S2-)=1.0×10-22。将适量FeCl2投入氢硫酸饱和溶液中,欲使溶液中c(Fe2+)=1.0 mol·L-1,应调节溶液的c(H+)=IV.氢硫酸中H2S是分步电离的,H2S
 H++ HS-K1=1.3×10-7,HS-
H++ HS-K1=1.3×10-7,HS- H++ S2-K2=7.1×10-15欲使溶液中c(S2-)浓度增大,应采取的措施有
H++ S2-K2=7.1×10-15欲使溶液中c(S2-)浓度增大,应采取的措施有A.加入NaOH B.加入CuSO4C.适当降低温度D.通入过量SO2E.加入Na2CO3(H2CO3电离常数K1=4.4×10-7,K2=4.7×10-11)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】甲醇是21世纪的新型燃料,而据统计,我国没经处理便排放的焦炉煤气超250亿立方米,这是能源的浪费。为解决这一问题,我国在2004年起利用焦炉煤气制取甲醇。
(1)已知 中的
中的 与
与 之间为三键连接,且合成甲醇的主要反应原理为
之间为三键连接,且合成甲醇的主要反应原理为 。表中所列为常见化学键的键能数据:
。表中所列为常见化学键的键能数据:
则该反应的
___________  。
。
(2)以 和
和 为原料也可合成甲醇,反应的能量变化如图所示。
为原料也可合成甲醇,反应的能量变化如图所示。

图中 处应填入
处应填入___________ 。
(3)工业上可以用 和
和 为原料,先制备
为原料,先制备 和
和 气体,再制备甲醇。现将
气体,再制备甲醇。现将
 和
和 通入容积为
通入容积为 的反应室,在一定条件下发生反应:
的反应室,在一定条件下发生反应: 的平衡转化率与温度、压强的关系如图:
的平衡转化率与温度、压强的关系如图:

①已知 ,压强为
,压强为 时,达到平衡需时
时,达到平衡需时 ,则用
,则用 表示的平均反应速率为
表示的平均反应速率为___________ 。
②其它条件不变,升高温度,化学平衡常数将___________ (填“增大”“减小”或“不变”)。
③图2中的
_______  (填“<”、“>”或“=”),在
(填“<”、“>”或“=”),在 ,压强为
,压强为 时平衡常数为
时平衡常数为___________ 。
④保持反应体系 ,压强为
,压强为 后再向容器中充入
后再向容器中充入 各
各 ,化学平衡将
,化学平衡将___________ 移动(填“向左”“向右”或“不”)。
(1)已知
 中的
中的 与
与 之间为三键连接,且合成甲醇的主要反应原理为
之间为三键连接,且合成甲醇的主要反应原理为 。表中所列为常见化学键的键能数据:
。表中所列为常见化学键的键能数据:| 化学键 |  |  |  |  |  |  |
键能 | 348 | 414 | 436 | 326.8 | 1032 | 464 |

 。
。(2)以
 和
和 为原料也可合成甲醇,反应的能量变化如图所示。
为原料也可合成甲醇,反应的能量变化如图所示。
图中
 处应填入
处应填入(3)工业上可以用
 和
和 为原料,先制备
为原料,先制备 和
和 气体,再制备甲醇。现将
气体,再制备甲醇。现将
 和
和 通入容积为
通入容积为 的反应室,在一定条件下发生反应:
的反应室,在一定条件下发生反应: 的平衡转化率与温度、压强的关系如图:
的平衡转化率与温度、压强的关系如图:
①已知
 ,压强为
,压强为 时,达到平衡需时
时,达到平衡需时 ,则用
,则用 表示的平均反应速率为
表示的平均反应速率为②其它条件不变,升高温度,化学平衡常数将
③图2中的

 (填“<”、“>”或“=”),在
(填“<”、“>”或“=”),在 ,压强为
,压强为 时平衡常数为
时平衡常数为④保持反应体系
 ,压强为
,压强为 后再向容器中充入
后再向容器中充入 各
各 ,化学平衡将
,化学平衡将
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】燃煤会产生CO2、CO、SO2等大气污染物。燃煤脱硫的相关反应的热化学方程式如下:
Ⅰ.
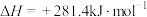
Ⅱ.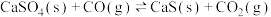
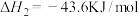
(1)一定温度下,向某恒容密闭容器中加入CaSO4(s)和1molCO,若只发生反应Ⅰ,下列能说明该反应已达到平衡状态的是________ (填字母)。
a.容器内的压强不发生变化 b.
c.容器内气体的密度不发生变化 d.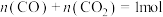
(2)一定温度下,体积为1L的容器中加入CaSO4(s)和1molCO,若只发生反应Ⅱ,测得CO2的物质的量随时间变化如图中曲线A所示:
________ 。
②曲线B表示过程与曲线A相比,改变的反应条件可能为________ (答出一条即可)。
③若要提高反应体系中CO2的体积分数,可采取的措施为________ 。
(3)以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.

Ⅱ.

Ⅲ.

回答下列问题:

________ kJmol-1。
Ⅰ.

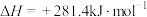
Ⅱ.
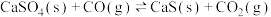
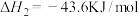
(1)一定温度下,向某恒容密闭容器中加入CaSO4(s)和1molCO,若只发生反应Ⅰ,下列能说明该反应已达到平衡状态的是
a.容器内的压强不发生变化 b.

c.容器内气体的密度不发生变化 d.
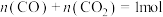
(2)一定温度下,体积为1L的容器中加入CaSO4(s)和1molCO,若只发生反应Ⅱ,测得CO2的物质的量随时间变化如图中曲线A所示:
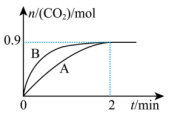

②曲线B表示过程与曲线A相比,改变的反应条件可能为
③若要提高反应体系中CO2的体积分数,可采取的措施为
(3)以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.


Ⅱ.


Ⅲ.


回答下列问题:

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】资源化利用二氧化硫,一方面能保护环境,另一方面能提高经济效益,具有深远意义。钠碱法的启动吸收剂为 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。
(1)常温下进行“钠碱法”的模拟实验。用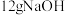 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为___________ L(折算成标准状况)。若实验时只吸收了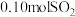 ,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为
,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为___________ 。
(2)当钠碱法的吸收液 达到4~6时,混合液中含较多量
达到4~6时,混合液中含较多量 。加热该溶液可回收得到较高纯度的
。加热该溶液可回收得到较高纯度的 ,剩余溶液可循环使用,进一步吸收
,剩余溶液可循环使用,进一步吸收 ,剩余溶液的主要溶质是
,剩余溶液的主要溶质是___________ (填写化学式)。
(3)将 通入
通入 溶液时,得到一组
溶液时,得到一组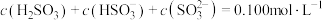 的混合溶液,溶液中部分微粒的物质的量浓度随
的混合溶液,溶液中部分微粒的物质的量浓度随 的关系曲线如下图所示。
的关系曲线如下图所示。
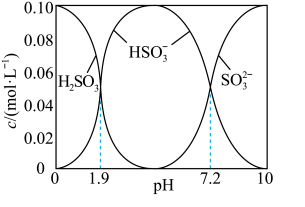
若溶液的 ,溶液中
,溶液中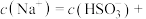
___________ 此时溶液中
___________  。(选填“>”、“<”或“=”)
。(选填“>”、“<”或“=”)
(4)亚硫酸为二元弱酸, 时,其电离常数
时,其电离常数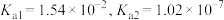 。请说明
。请说明 溶液呈酸性的理由。
溶液呈酸性的理由。___________ 。
(5)工业中可用含 的冶炼烟气为原料生产硫酸,在如图装置中完成“
的冶炼烟气为原料生产硫酸,在如图装置中完成“ 转化”工序。使用该装置实现了
转化”工序。使用该装置实现了___________ (选填编号)。
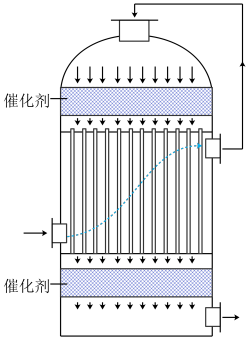
a.充分利用热能 b.防止形成酸雾 c.加速转化 d.获取纯净
d.获取纯净
 溶液,捕捉
溶液,捕捉 后生成
后生成 和
和 的混合液。
的混合液。(1)常温下进行“钠碱法”的模拟实验。用
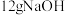 固体配成一定浓度的溶液,这些
固体配成一定浓度的溶液,这些 理论上最多可吸收
理论上最多可吸收 的体积约为
的体积约为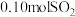 ,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为
,则反应后的吸收液中,所含负离子的浓度由大到小的顺序为(2)当钠碱法的吸收液
 达到4~6时,混合液中含较多量
达到4~6时,混合液中含较多量 。加热该溶液可回收得到较高纯度的
。加热该溶液可回收得到较高纯度的 ,剩余溶液可循环使用,进一步吸收
,剩余溶液可循环使用,进一步吸收 ,剩余溶液的主要溶质是
,剩余溶液的主要溶质是(3)将
 通入
通入 溶液时,得到一组
溶液时,得到一组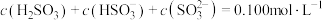 的混合溶液,溶液中部分微粒的物质的量浓度随
的混合溶液,溶液中部分微粒的物质的量浓度随 的关系曲线如下图所示。
的关系曲线如下图所示。
若溶液的
 ,溶液中
,溶液中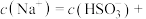

 。(选填“>”、“<”或“=”)
。(选填“>”、“<”或“=”)(4)亚硫酸为二元弱酸,
 时,其电离常数
时,其电离常数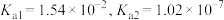 。请说明
。请说明 溶液呈酸性的理由。
溶液呈酸性的理由。(5)工业中可用含
 的冶炼烟气为原料生产硫酸,在如图装置中完成“
的冶炼烟气为原料生产硫酸,在如图装置中完成“ 转化”工序。使用该装置实现了
转化”工序。使用该装置实现了
a.充分利用热能 b.防止形成酸雾 c.加速转化
 d.获取纯净
d.获取纯净
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
为了探究浓度对反应速率的影响,小组成员设计了三组平行实验,实验时,溶液迅速混合并开始计时通过溶液褪色所需时间来判断反应快慢。(控制反应过程中溶液温度为室温)
【实验原理】
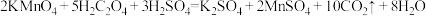
【实验内容及记录】
请回答下列问题:
(1)第三组实验中,所加蒸馏水的体积为x=___________ mL
(2)利用实验2中数据计算,
___________ 。
(3)根据上表中的实验数据,可以得到的结论是___________ 。
(4)该化学小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。

①该小组同学提出的假设是___________ 。
②请你帮助该小组同学完成实验方案,并填写表中空白。
实验4中向试管中加入少量固体___________ 。
③若该小组同学提出的假设成立,室温下溶液颜色褪至无色所需时间___________ (填大于、等于或小于)4 min。
为了探究浓度对反应速率的影响,小组成员设计了三组平行实验,实验时,溶液迅速混合并开始计时通过溶液褪色所需时间来判断反应快慢。(控制反应过程中溶液温度为室温)
【实验原理】
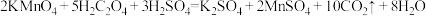
【实验内容及记录】
| 编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | 调控溶液温度 | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/LKMnO4溶液 | 3 mol/L稀硫酸 | |||
| 1 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 | 298K |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.0 | 298K |
| 3 | 3.0 | x | 1.0 | 2.0 | 6.4 | 298K |
(1)第三组实验中,所加蒸馏水的体积为x=
(2)利用实验2中数据计算,

(3)根据上表中的实验数据,可以得到的结论是
(4)该化学小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。

①该小组同学提出的假设是
②请你帮助该小组同学完成实验方案,并填写表中空白。
| 编号 | 室温下,试管中所加试剂及其用量/mL | 再向试管中加入少量固体 | 室温下溶液颜色褪至无色所需时间/min | |||
| 0.6 mol/L H2C2O4溶液 | H2O | 0.2 mol/LKMnO4溶液 |  稀硫酸 稀硫酸 | |||
| 4 | 3.0 | 2.0 | 3.0 | 2.0 | ___________ | ___________ |
③若该小组同学提出的假设成立,室温下溶液颜色褪至无色所需时间
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某研究性学习小组利用H2C2O4与酸性KMnO4溶液的反应,探究“外界条件对化学反应速率的影响”,实验记录如下表所示:
查阅资料:KMnO4溶液中滴加过量的H2C2O4,振荡后溶液由紫色变为无色,反应的离子方程式为:5H2C2O4+2MnO +6H+=2Mn2++10CO2↑+8H2O。
+6H+=2Mn2++10CO2↑+8H2O。
回答下列问题:
(1)T1=___________ 。
(2)V1=___________ ,理由是___________ 。
(3)若探究温度对化学反应速率的影响,可选择实验________ (填组别),根据实验数据,可以得出的结论是___________ 。
(4)甲同学依据经验绘制出A组实验中V(CO2)随时间t的变化如图1所示,乙同学查阅资料发现实验过程中V(CO2)随时间t的变化趋势如图2所示。
小组同学针对这一现象,设计实验进一步探究影响因素,具体情况见下表。

①补全方案1中的实验操作:_____ ;②方案2中的假设为_____ 。
| 实验组别 | 实验温度/K | 参加反应的物质 | 溶液褪色所需时间/s | ||||
KMnO4溶液(含硫酸) | H2C2O4溶液 | H2O | |||||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | |||
A | 293 | 3 | 0.2 | 7 | 1 | 0 | 60 |
B | T1 | 3 | 0.2 | 5 | 1 | V1 | 80 |
C | 313 | 3 | 0.2 | V2 | 1 | 2 | t1 |
 +6H+=2Mn2++10CO2↑+8H2O。
+6H+=2Mn2++10CO2↑+8H2O。回答下列问题:
(1)T1=
(2)V1=
(3)若探究温度对化学反应速率的影响,可选择实验
(4)甲同学依据经验绘制出A组实验中V(CO2)随时间t的变化如图1所示,乙同学查阅资料发现实验过程中V(CO2)随时间t的变化趋势如图2所示。
小组同学针对这一现象,设计实验进一步探究影响因素,具体情况见下表。

方案 | 假设 | 实验操作 |
1 | 该反应放热,使溶液温度升高,化学反应速率提高 | 向烧杯中加入3 mL 0.2 mol·L-1 KMnO4溶液和7 mL 1 mol·L-1 H2C2O4溶液,____。 |
2 | _____ | 取3 mL 0.2 mol·L-1 KMnO4溶液加入烧杯中,向其中加入少量硫酸锰固体,再加入7 mL 1 mol·L-1 H2C2O4溶液 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】合成氨工业对国民经济和社会发展具有重要的意义。
(1) 在不同温度、压强和相同催化剂条件下,初始
在不同温度、压强和相同催化剂条件下,初始 、
、 分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(
分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数( )如图所示。
)如图所示。
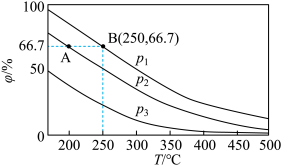
①其中,
___________  (填“>”或“<”),其原因是
(填“>”或“<”),其原因是___________ 。
②A、B两点的反应速率: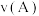
___________ 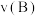 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③若在250℃、 条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
___________  (保留一位小数)。
(保留一位小数)。
(2)工业合成氨生产流程示意图如下:
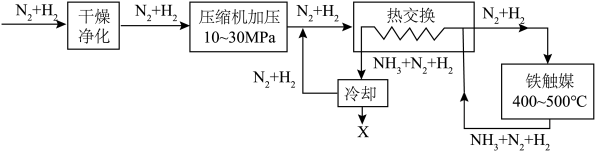
①X为___________ 。
②上述流程中,有利于提高原料利用率的措施是___________ (填标号)。
A.“净化干燥” B.“压缩机加压” C.“铁触媒400~500℃” D.原料气循环利用
③“干燥净化”中采用铜氨溶液除去CO:
 如何处理吸收CO后的铜氨溶液,请提出你的建议
如何处理吸收CO后的铜氨溶液,请提出你的建议___________ 。
(1)
 在不同温度、压强和相同催化剂条件下,初始
在不同温度、压强和相同催化剂条件下,初始 、
、 分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(
分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数( )如图所示。
)如图所示。
①其中,

 (填“>”或“<”),其原因是
(填“>”或“<”),其原因是②A、B两点的反应速率:
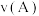
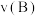 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③若在250℃、
 条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
条件下,反应达到平衡时容器的体积为0.06L,则该条件下合成氨的平衡常数
 (保留一位小数)。
(保留一位小数)。(2)工业合成氨生产流程示意图如下:

①X为
②上述流程中,有利于提高原料利用率的措施是
A.“净化干燥” B.“压缩机加压” C.“铁触媒400~500℃” D.原料气循环利用
③“干燥净化”中采用铜氨溶液除去CO:

 如何处理吸收CO后的铜氨溶液,请提出你的建议
如何处理吸收CO后的铜氨溶液,请提出你的建议
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氮的化合物应用广泛,但氮氧化物是主要的空气污染物,应降低其排放量。
(1) 用CO2和NH3可合成氮肥尿素[CO(NH2)2]。
已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5 kJ·mol-1;
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5 kJ·mol-1;
③H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1。
用CO2和NH3合成尿素(副产物是液态水)的热化学方程式为_______ 。
(2)工业上常用如下反应消除氮氧化物的污染:CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)ΔH在温度为T1和T2时,分别将0.40 mol CH4和1.0 mol NO2充入体积为1 L的密闭容器中,n(CH4)随反应时间的变化如图所示:
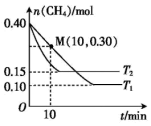
①据图判断该反应的ΔH_______ (填“>”“<”“=”)0,理由是 _______ 。
②温度为T1时,0~10 min内,NO2的平均反应速率v(NO2)=_______ 。
③该反应达到平衡后,为提高反应速率同时提高NO2的转化率,可采取的措施有_______ (填字母)。
A.改用高效催化剂 B.升高温度 C.缩小容器的体积 D.增大CH4的浓度
(3) 利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3=7N2+12H2O,电解质溶液为NaOH溶液。工作一段时间后,该电池正极附近溶液的pH_______ (填“增大” “减小”或“不变”),负极的电极反应式为_______ 。
(4)氮的一种氢化物为HN3,其水溶液酸性强弱与醋酸相似,25℃时,将a mol·L-1HN3与b mol·L-1Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(N ),则该混合溶液呈
),则该混合溶液呈_______ (填“酸”“碱”或“中”)性,溶液中c(HN3)=_______ mol·L-1。此温度下Ka(HN3)=_______ (用a.b表示)
(1) 用CO2和NH3可合成氮肥尿素[CO(NH2)2]。
已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH=-159.5 kJ·mol-1;
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH=+116.5 kJ·mol-1;
③H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1。
用CO2和NH3合成尿素(副产物是液态水)的热化学方程式为
(2)工业上常用如下反应消除氮氧化物的污染:CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)ΔH在温度为T1和T2时,分别将0.40 mol CH4和1.0 mol NO2充入体积为1 L的密闭容器中,n(CH4)随反应时间的变化如图所示:

①据图判断该反应的ΔH
②温度为T1时,0~10 min内,NO2的平均反应速率v(NO2)=
③该反应达到平衡后,为提高反应速率同时提高NO2的转化率,可采取的措施有
A.改用高效催化剂 B.升高温度 C.缩小容器的体积 D.增大CH4的浓度
(3) 利用原电池反应可实现NO2的无害化,总反应为6NO2+8NH3=7N2+12H2O,电解质溶液为NaOH溶液。工作一段时间后,该电池正极附近溶液的pH
(4)氮的一种氢化物为HN3,其水溶液酸性强弱与醋酸相似,25℃时,将a mol·L-1HN3与b mol·L-1Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(N
 ),则该混合溶液呈
),则该混合溶液呈
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】将CH4和CO2两种引发温室效应气体转化为合成气(H2和CO),可以实现能量综合利用,对环境保护具有十分重要的意义。
(1)利用CH4、CO2在一定条件下重整的技术可得到富含CO的气体,此技术在能源和环境上具有双重重大意义。重整过程中的催化转化原理如图所示。

已知:i.CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH1=+206kJ·mol-1
ii.CH4(g)+2H2O(g)⇌CO2(g)+4H2(g) ΔH2=+165kJ·mol-1
①过程I反应的化学方程式为___________ 。
②该技术总反应的热化学方程式为___________ 。
③反应i甲烷含量随温度变化如图1,图中a、b、c、d四条曲线中的两条代表压强分别为1MPa、2MPa时甲烷含量曲线,其中表示2MPa的是___________ 。
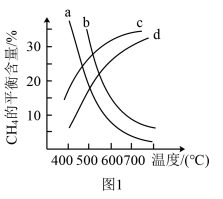
(2)甲烷的水蒸气重整涉及以下反应
I.CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH1=+206kJ·mol-1
II.CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH2=-41kJ·mol-1
在一密闭体积可变容器中,通入1molCH4和3molH2O(g)发生甲烷的水蒸气重整反应。
①反应II平衡常数K(500℃)___________ K(700℃)(填“>”“<”或“=”)。
②压强为P0kPa时,分别在加CaO和不加CaO时,平衡体系H2的物质的量随温度变化如图2所示。温度低于700℃时,加入CaO可明显提高混合气中H2的量,原因是___________ 。
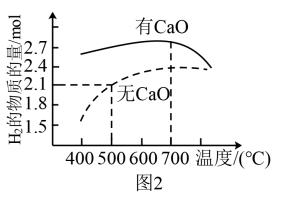
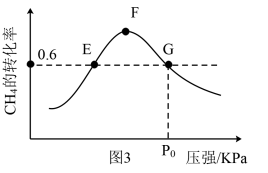
③500℃时,反应相同时间后测得CH4的转化率随压强的变化如图3所示。则图2中E点和G点CH4的浓度大小关系为c(G)___________ c(E)((填“>”“<”或“=”);结合的图2、图3,计算500℃、P0kPa下反应II的分压平衡常数Kp(用分压代替浓度,分压等于总压×物质的量分数)为___________ 。
(1)利用CH4、CO2在一定条件下重整的技术可得到富含CO的气体,此技术在能源和环境上具有双重重大意义。重整过程中的催化转化原理如图所示。

已知:i.CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH1=+206kJ·mol-1
ii.CH4(g)+2H2O(g)⇌CO2(g)+4H2(g) ΔH2=+165kJ·mol-1
①过程I反应的化学方程式为
②该技术总反应的热化学方程式为
③反应i甲烷含量随温度变化如图1,图中a、b、c、d四条曲线中的两条代表压强分别为1MPa、2MPa时甲烷含量曲线,其中表示2MPa的是

(2)甲烷的水蒸气重整涉及以下反应
I.CH4(g)+H2O(g)⇌CO(g)+3H2(g) ΔH1=+206kJ·mol-1
II.CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH2=-41kJ·mol-1
在一密闭体积可变容器中,通入1molCH4和3molH2O(g)发生甲烷的水蒸气重整反应。
①反应II平衡常数K(500℃)
②压强为P0kPa时,分别在加CaO和不加CaO时,平衡体系H2的物质的量随温度变化如图2所示。温度低于700℃时,加入CaO可明显提高混合气中H2的量,原因是

③500℃时,反应相同时间后测得CH4的转化率随压强的变化如图3所示。则图2中E点和G点CH4的浓度大小关系为c(G)

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)已知CH3OH(l)的燃烧热△H=-238.6 kJ/mol,CH3OH(l)+ O2(g)=CO2(g)+2H2O(g) △H=-a kJ/mol,则a
O2(g)=CO2(g)+2H2O(g) △H=-a kJ/mol,则a__ 238.6(填“>”“<”或“=”)。
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:__ 。
(3)mA(g)+nB(g) pC(g)+qD(g)在反应过程中的能量变化如图所示,回答下列问题。
pC(g)+qD(g)在反应过程中的能量变化如图所示,回答下列问题。

该反应△H=_____ (用E1、E2表示)kJ•mol-1;在反应体系中加入催化剂,E1将____ (填“增大”“减小”或“不变”,下同),△H将______ 。
(4)已知CO(g)+H2O(g) H2(g)+CO2(g)的平衡常数K随温度的变化如表:
H2(g)+CO2(g)的平衡常数K随温度的变化如表:
回答下列问题:
①该反应的△H_____ 0(填“>”“<”或“=”)。
②已知在一定温度下,C(s)+CO2(g) 2CO(g)的平衡常数为K1,C(s)+H2O(g)
2CO(g)的平衡常数为K1,C(s)+H2O(g) CO(g)+H2(g)的平衡常数为K2,则K、K1、K2之间的关系是
CO(g)+H2(g)的平衡常数为K2,则K、K1、K2之间的关系是___ 。
③500℃时,若起始时c(CO)=2 mol•L-1,c(H2O)=2 mol•L-1,则平衡时CO的转化率为____ 。
 O2(g)=CO2(g)+2H2O(g) △H=-a kJ/mol,则a
O2(g)=CO2(g)+2H2O(g) △H=-a kJ/mol,则a(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:
(3)mA(g)+nB(g)
 pC(g)+qD(g)在反应过程中的能量变化如图所示,回答下列问题。
pC(g)+qD(g)在反应过程中的能量变化如图所示,回答下列问题。
该反应△H=
(4)已知CO(g)+H2O(g)
 H2(g)+CO2(g)的平衡常数K随温度的变化如表:
H2(g)+CO2(g)的平衡常数K随温度的变化如表:| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
①该反应的△H
②已知在一定温度下,C(s)+CO2(g)
 2CO(g)的平衡常数为K1,C(s)+H2O(g)
2CO(g)的平衡常数为K1,C(s)+H2O(g) CO(g)+H2(g)的平衡常数为K2,则K、K1、K2之间的关系是
CO(g)+H2(g)的平衡常数为K2,则K、K1、K2之间的关系是③500℃时,若起始时c(CO)=2 mol•L-1,c(H2O)=2 mol•L-1,则平衡时CO的转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g) CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:
CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ•mol-1
②CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ•mol-1
总反应的ΔH=___________ kJ•mol-1;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是 ___________ (填标号)。
A.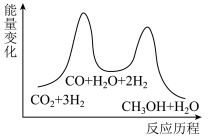 B.
B. 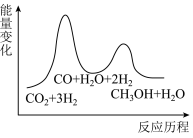
C.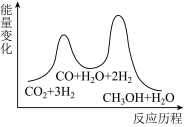 D.
D. 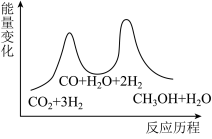
(2)合成总反应在起始物 3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下,x(CH3OH)与压强的关系(x(CH3OH)~p)和在p=5×105Pa下,x(CH3OH)与温度的关系(x(CH3OH)~t)分别如图所示,请回答下列问题:
3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下,x(CH3OH)与压强的关系(x(CH3OH)~p)和在p=5×105Pa下,x(CH3OH)与温度的关系(x(CH3OH)~t)分别如图所示,请回答下列问题:
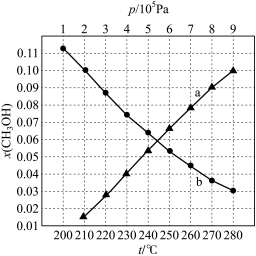
①图中对应等压过程的曲线是___________ ,判断的理由是 ___________ 。
②当x(CH3OH)=0.10时,CO2的平衡转化率α=___________ (保留两位有效数字),反应条件可能为 ___________ 。
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:
CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:①CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ•mol-1
②CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ•mol-1
总反应的ΔH=
A.
 B.
B. 
C.
 D.
D. 
(2)合成总反应在起始物
 3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下,x(CH3OH)与压强的关系(x(CH3OH)~p)和在p=5×105Pa下,x(CH3OH)与温度的关系(x(CH3OH)~t)分别如图所示,请回答下列问题:
3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下,x(CH3OH)与压强的关系(x(CH3OH)~p)和在p=5×105Pa下,x(CH3OH)与温度的关系(x(CH3OH)~t)分别如图所示,请回答下列问题:
①图中对应等压过程的曲线是
②当x(CH3OH)=0.10时,CO2的平衡转化率α=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】铁及其化合物在日常生活生产中应用广泛,研究铁及其化合物的应用意义重大。回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g)=Fe(s)+CO2(g) △H1
Fe2O3(s)+ CO(g)=
CO(g)= Fe3O4(s)+
Fe3O4(s)+ CO2(g) △H2
CO2(g) △H2
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) △H3
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H4
则△H4的表达式为△H4=__ (用含△H1、△H2、△H3中一个或多个的代数式表示)。
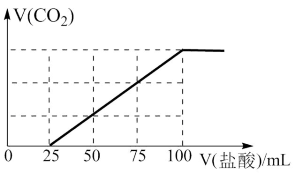
(2)把高炉出来的气体经过处理后通入NaOH溶液中完全吸收,再用0.01 mol•L-1的盐酸溶液进行滴定,所得气体与滴入的盐酸体积的关系如图,则滴定前溶液中的溶质为:__ ,该溶液中离子浓度由大到小的顺序为:__ 。
(3)①铁等金属可用作CO与氢气反应的催化剂。已知某种催化剂可用来催化CO(g)+3H2(g) CH4(g)+H2O(g) △H<0。在T℃、10 6Pa时将1 mol CO和3 mol H2加入容积不变的密闭容器中,实验测得CO的体积分数φ(CO)如表:
CH4(g)+H2O(g) △H<0。在T℃、10 6Pa时将1 mol CO和3 mol H2加入容积不变的密闭容器中,实验测得CO的体积分数φ(CO)如表:
达到平衡时CO的转化率为__ 。
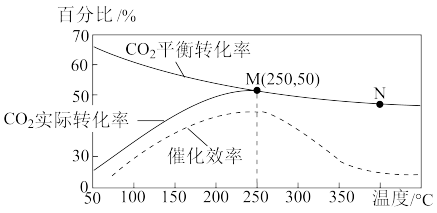
②某种含铁催化剂可以催化合成乙烯:6H2(g)+2CO2(g) CH2=CH2(g)+4H2O(g)。已知温度对CO2的平衡转化率、实际催化率和催化剂催化效率的影响如图所示,结合图象分析温度低于250℃时CO2实际转化率变化的原因:
CH2=CH2(g)+4H2O(g)。已知温度对CO2的平衡转化率、实际催化率和催化剂催化效率的影响如图所示,结合图象分析温度低于250℃时CO2实际转化率变化的原因:__ 。
(4)炉渣中的Fe2O3可制备还原铁粉。还原铁粉纯度可通过下列方法测定:称取0.2800 g样品,溶于过量稀硫酸,添加二苯胺磺酸钠作指示剂(可被氧化为紫红色物质),平行三次用标准K2Cr2O7溶液滴定所得溶液中的Fe2+,平均消耗0.0300 mol•L-1的K2Cr2O7溶液25.10 mL(测定过程中杂质不参与反应)。
①滴定终点的现象为__ 。
②计算还原铁粉的纯度(保留4位有效数字)__ 。
(1)已知高炉炼铁过程中会发生如下反应:
FeO(s)+CO(g)=Fe(s)+CO2(g) △H1
Fe2O3(s)+
 CO(g)=
CO(g)= Fe3O4(s)+
Fe3O4(s)+ CO2(g) △H2
CO2(g) △H2Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) △H3
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H4
则△H4的表达式为△H4=
(2)把高炉出来的气体经过处理后通入NaOH溶液中完全吸收,再用0.01 mol•L-1的盐酸溶液进行滴定,所得气体与滴入的盐酸体积的关系如图,则滴定前溶液中的溶质为:

(3)①铁等金属可用作CO与氢气反应的催化剂。已知某种催化剂可用来催化CO(g)+3H2(g)
 CH4(g)+H2O(g) △H<0。在T℃、10 6Pa时将1 mol CO和3 mol H2加入容积不变的密闭容器中,实验测得CO的体积分数φ(CO)如表:
CH4(g)+H2O(g) △H<0。在T℃、10 6Pa时将1 mol CO和3 mol H2加入容积不变的密闭容器中,实验测得CO的体积分数φ(CO)如表:| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| φ(CO) | 0.25 | 0.23 | 0.214 | 0.202 | 0.200 | 0.200 |
达到平衡时CO的转化率为
②某种含铁催化剂可以催化合成乙烯:6H2(g)+2CO2(g)
 CH2=CH2(g)+4H2O(g)。已知温度对CO2的平衡转化率、实际催化率和催化剂催化效率的影响如图所示,结合图象分析温度低于250℃时CO2实际转化率变化的原因:
CH2=CH2(g)+4H2O(g)。已知温度对CO2的平衡转化率、实际催化率和催化剂催化效率的影响如图所示,结合图象分析温度低于250℃时CO2实际转化率变化的原因:
(4)炉渣中的Fe2O3可制备还原铁粉。还原铁粉纯度可通过下列方法测定:称取0.2800 g样品,溶于过量稀硫酸,添加二苯胺磺酸钠作指示剂(可被氧化为紫红色物质),平行三次用标准K2Cr2O7溶液滴定所得溶液中的Fe2+,平均消耗0.0300 mol•L-1的K2Cr2O7溶液25.10 mL(测定过程中杂质不参与反应)。
①滴定终点的现象为
②计算还原铁粉的纯度(保留4位有效数字)
您最近一年使用:0次



