在恒温恒容的密闭容器中发生 △H<0,T℃时,平衡常数为K,下列说法正确的是
△H<0,T℃时,平衡常数为K,下列说法正确的是
 △H<0,T℃时,平衡常数为K,下列说法正确的是
△H<0,T℃时,平衡常数为K,下列说法正确的是| A.该反应在任何温度下都可自发进行 |
B.T℃时,若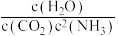 <K时,则V正<V逆 <K时,则V正<V逆 |
| C.若容器内气体压强保持不变,该可逆反应达到化学平衡状态 |
| D.选择高效催化剂可以提高活化分子百分数,提高CO(NH2)2平衡产率 |
更新时间:2023-08-14 18:21:17
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】在一定条件下,一定浓度的甲酸溶液在密闭容器中发生分解反应(分解产物均溶于水):
Ⅰ.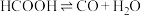 Ⅱ.
Ⅱ.
反应过程中含碳微粒(忽略碳元素的其他存在形式)的占比随时间的变化及反应Ⅰ的反应历程如图所示:
Ⅰ.
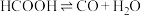 Ⅱ.
Ⅱ.
反应过程中含碳微粒(忽略碳元素的其他存在形式)的占比随时间的变化及反应Ⅰ的反应历程如图所示:
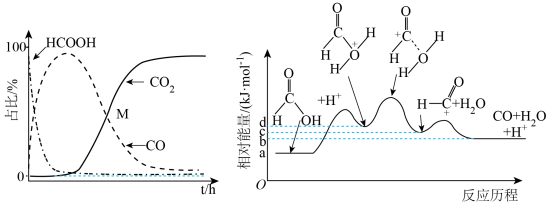
A.反应Ⅰ中 是该反应的催化剂,平衡前适当提高 是该反应的催化剂,平衡前适当提高 浓度有利于加快反应Ⅰ的速率 浓度有利于加快反应Ⅰ的速率 |
B.反应Ⅰ的热化学方程式可表示为: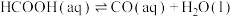 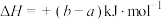 |
C.适当升高温度可降低平衡时CO和 的比例 的比例 |
| D.在反应Ⅰ的反应历程中,存在3种中间产物 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
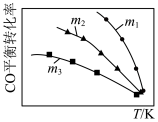
【推荐2】利用反应2NO(g)+2CO(g) 2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比
2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
 2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比
2CO2(g)+N2(g),可实现汽车尾气无害化处理。一定条件下进行该反应,测得CO的平衡转化率与温度、起始投料比 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
| A.若m=2,反应达平衡时,NO的转化率为40%,则N2的体积分数为15.4% |
B.该反应的 |
C.投料比: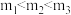 |
| D.汽车排气管中的催化剂可提高NO的平衡转化率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】温度为T时,向 恒容密闭容器中充入
恒容密闭容器中充入 :
: ,反应经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
,反应经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
下列说法正确的是
 恒容密闭容器中充入
恒容密闭容器中充入 :
: ,反应经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
,反应经过一段时间后达到平衡。反应过程中测定的部分数据见下表: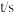 | 0 | 50 | 150 | 250 | 350 |
 | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.温度为T时平衡常数 |
B.保持其他条件不变,升高温度再次平衡时 |
C. 后向该容器中再充入 后向该容器中再充入 、 、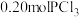 和 和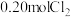 ,反应达到平衡前v(正)<v(逆) ,反应达到平衡前v(正)<v(逆) |
D.相同温度下,起始时向容器中充入 和 和 ,达到平衡时, ,达到平衡时, 的转化率小于80% 的转化率小于80% |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】以CO2和NH3为原料,通过反应:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(l)合成尿素。该反应的平衡常数和温度的关系如表;在一定温度和压强下,原料气中NH3和CO2的物质的量之比(氨碳比)与CO2平衡转化率(α)的关系如图所示。下列说法正确的是( )
CO(NH2)2(l)+H2O(l)合成尿素。该反应的平衡常数和温度的关系如表;在一定温度和压强下,原料气中NH3和CO2的物质的量之比(氨碳比)与CO2平衡转化率(α)的关系如图所示。下列说法正确的是( )

 CO(NH2)2(l)+H2O(l)合成尿素。该反应的平衡常数和温度的关系如表;在一定温度和压强下,原料气中NH3和CO2的物质的量之比(氨碳比)与CO2平衡转化率(α)的关系如图所示。下列说法正确的是( )
CO(NH2)2(l)+H2O(l)合成尿素。该反应的平衡常数和温度的关系如表;在一定温度和压强下,原料气中NH3和CO2的物质的量之比(氨碳比)与CO2平衡转化率(α)的关系如图所示。下列说法正确的是( )| t/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |

| A.图中B点处NH3的平衡转化率为32% |
B.该反应平衡常数的表达式为 |
| C.该反应中反应物的总键能大于生成物的总键能 |
| D.氨碳比越高,合成CO(NH2)2时NH3的转化率越高 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】温度为T1时,在三个容积均为1 L的恒容密闭容器中仅发生反应 2NO2(g)⇌2NO(g)+O2(g) ΔH>0。实验测得:υ正=υ(NO2)消耗=k正c2(NO2),υ逆=υ(NO)消耗=2υ(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法正确的是
| 容器编号 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度(mol·L-1) | ||
| c(NO2) | c(NO) | c(O2) | c(O2) | |
| Ⅰ | 0.6 | 0 | 0 | 0.2 |
| Ⅱ | 0.3 | 0.5 | 0.2 | |
| Ⅲ | 0 | 0.5 | 0.35 | |
| A.反应达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为1∶1 |
B.反应达平衡时,容器Ⅱ中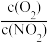 比容器Ⅰ中的大 比容器Ⅰ中的大 |
| C.反应达平衡时,容器Ⅲ中NO的体积分数大于50% |
| D.当温度改变为T2时,若k正=k逆,则T2>T1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在一个绝热的固定容积的密闭容器中,发生可逆反应mA(g)+nB(g)  pC(g)+qD(s),当m+n=p时,一定可以作为反应达到平衡状态标志的是
pC(g)+qD(s),当m+n=p时,一定可以作为反应达到平衡状态标志的是
①体系的压强不再改变 ②体系的温度不再改变 ③体系的密度不再改变 ④各组分质量分数不再改变
 pC(g)+qD(s),当m+n=p时,一定可以作为反应达到平衡状态标志的是
pC(g)+qD(s),当m+n=p时,一定可以作为反应达到平衡状态标志的是①体系的压强不再改变 ②体系的温度不再改变 ③体系的密度不再改变 ④各组分质量分数不再改变
| A.①②③ | B.①②③④ | C.②③④ | D.③④ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】对于反应2SO2+O2 2SO3,下列判断正确的是
2SO3,下列判断正确的是
 2SO3,下列判断正确的是
2SO3,下列判断正确的是| A.2 mol SO2和5 mol O2充分反应可生成2 mol SO3 |
| B.2 mol SO2和1mol O2达到化学平衡时SO2、O2、SO3的分子数之比一定为2∶1∶2 |
| C.达到化学平衡时SO2的消耗速率必定等于O2的生成速率的2倍 |
| D.三种物质的浓度相等时,说明反应达到了化学平衡。 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】在甲、乙、丙三个恒温恒容的密闭容器中,分别加入足量活性炭和一定量的 NO,进行反应C(s)+2NO(g)  N2(g)+CO2(g), 测得各容器中 c(NO)随反应时间 t 的变化情况如下表所示,下列说法正确的是( )
N2(g)+CO2(g), 测得各容器中 c(NO)随反应时间 t 的变化情况如下表所示,下列说法正确的是( )

 N2(g)+CO2(g), 测得各容器中 c(NO)随反应时间 t 的变化情况如下表所示,下列说法正确的是( )
N2(g)+CO2(g), 测得各容器中 c(NO)随反应时间 t 的变化情况如下表所示,下列说法正确的是( )
| A.达到平衡状态时,2v 正(NO)= v 逆(N2) |
| B.活性炭的质量不再改变不能说明反应已达平衡状态 |
| C.丙容器中,从反应开始到建立平衡时的平均反应速率为 v (NO) >0.01125mol·L-1·min-1 |
| D.由表格数据可知:T<400℃ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列有关说法正确的是( )
| A.常温下,将pH =10的氨水稀释,溶液中所有离子浓度都减小 |
| B.常温下,反应2A (s)+B (g)=2C (g)+D (g)不能自发进行,则该反应△H一定大于0 |
| C.在酸碱中和滴定实验中,锥形瓶未用待测液润洗会对实验结果造成影响 |
| D.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列说法正确的是
| A.Na与H2O的反应是熵增的放热反应,该反应能自发进行 |
B.常温下,NH4Cl溶液加水稀释, 增大 增大 |
| C.0.1 mol·L-1NaCN溶液中含 HCN和CN-总数目为0.1×6.02×1023 |
| D.FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】 在电子、光学和催化剂领域有广泛应用,设计通过
在电子、光学和催化剂领域有广泛应用,设计通过 制备
制备 和
和 制备
制备 的反应原理分别如下:I.
的反应原理分别如下:I.

Ⅱ.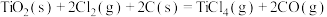
 。
。
下列说法错误的是
 在电子、光学和催化剂领域有广泛应用,设计通过
在电子、光学和催化剂领域有广泛应用,设计通过 制备
制备 和
和 制备
制备 的反应原理分别如下:I.
的反应原理分别如下:I.

Ⅱ.
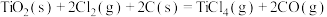
 。
。下列说法错误的是
| A.反应I能自发进行主要是焓减驱动 |
| B.反应I的体系中加入碳粉,可改变反应进行的方向 |
| C.反应Ⅱ正反应的活化能比逆反应的活化能大 |
D.减小压强和降低温度,会降低反应Ⅱ的速率,但可提高 的平衡转化率 的平衡转化率 |
您最近一年使用:0次

 转化为高附加值产品
转化为高附加值产品 的催化反应历程,该历程示意如下。则下列说法不正确的是
的催化反应历程,该历程示意如下。则下列说法不正确的是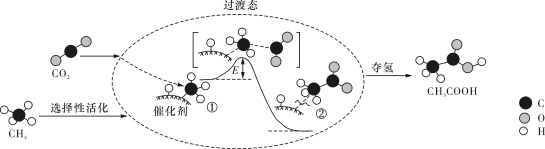
 过程中,形成的键只有非极性共价键
过程中,形成的键只有非极性共价键 键
键

