中国旅美教授JingjieWu及其学生利用石墨烯量子点为催化剂,将CO2转化为燃料甲烷,空间站基于该反应将宇航员呼出的CO2转化为火箭燃料。将5molCO2和20molH2通入某恒压(压强为P0)密闭容器中,发生如下反应:
Ⅰ.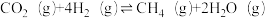 △H=-165kJ·mol-1(主反应)
△H=-165kJ·mol-1(主反应)
Ⅱ.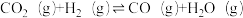 △H=+41kJ·mol-1(副反应)
△H=+41kJ·mol-1(副反应)
平衡时容器中含碳元素物质的物质的量[n(X)]随温度(T)的变化如图甲、乙、丙曲线所示。
Ⅰ.
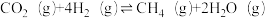 △H=-165kJ·mol-1(主反应)
△H=-165kJ·mol-1(主反应)Ⅱ.
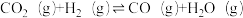 △H=+41kJ·mol-1(副反应)
△H=+41kJ·mol-1(副反应)平衡时容器中含碳元素物质的物质的量[n(X)]随温度(T)的变化如图甲、乙、丙曲线所示。

| A.曲线甲、乙、丙分别表示CO2、CO、CH4 |
| B.空间站中使CO2转化为燃料CH4的反应不能采用高温 |
| C.1050K时,曲线丙逐渐下降的原因是以反应Ⅱ为主 |
D.800K时反应Ⅰ的压强平衡常数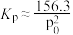 |
23-24高三上·湖南·开学考试 查看更多[4]
湖南省部分学校2023-2024学年高三8月开学考试化学试题湖南省邵阳市武冈市2023-2024学年高三上学期期中考试化学试题湖南省张家界市慈利县第一中学2023-2024学年高三上学期第二次月考化学试卷(已下线)提升练05 化学平衡常数的计算-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
更新时间:2023-08-31 08:41:46
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】工业上用乙苯与 生产苯乙烯,主要反应:
生产苯乙烯,主要反应: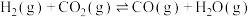
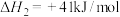
在一定压强和催化剂作用下,向恒容容器中充入等物质的量的乙苯和 。达到平衡时,各物质的体积分数随温度的变化如图所示。
。达到平衡时,各物质的体积分数随温度的变化如图所示。不正确 的是
 生产苯乙烯,主要反应:
生产苯乙烯,主要反应:① (g)
(g)
 (g)+H2(g)
(g)+H2(g)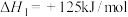
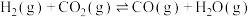
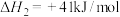
在一定压强和催化剂作用下,向恒容容器中充入等物质的量的乙苯和
 。达到平衡时,各物质的体积分数随温度的变化如图所示。
。达到平衡时,各物质的体积分数随温度的变化如图所示。
| A.当反应混合气体的平均相对分子质量不再变化时,反应达到化学平衡状态 |
B.苯乙烯和 的体积分数变化差异的主要原因是 的体积分数变化差异的主要原因是 消耗 消耗 |
| C.乙苯的平衡转化率随温度升高而升高,宜采用700℃获得更多的苯乙烯 |
| D.温度越高,乙苯脱氢生成苯乙烯的反应的K越大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】T℃时,在1L密闭容器中A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图I所示;若保持其他条件不变,温度分别为Tl和T2时,B的体积百分含量与时间的关系如图Ⅱ所示。则下列结论正确的是
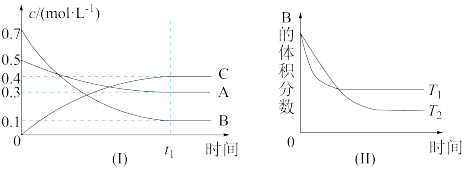

| A.在达平衡后,保持其他条件不变,增大压强,平衡向逆反应方向移动 |
| B.在达平衡后,保持压强不变,通入稀有气体,平衡向正反应方向移动 |
| C.保持其他条件不变,若反应开始时A、B、C的浓度分别为0.4mol·L-1、0.5 mol·L-1和0.2 mol·L—1,则达到平衡后,C的浓度大于0.4 mol·L-1 |
| D.保持其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】苯乙烯是制备高分子的原料.乙苯脱氢制苯乙烯的反应如下:
反应I:
制备过程中会发生如下两个副反应:
反应Ⅱ:
反应Ⅲ:
在 下,将质量比为
下,将质量比为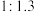 的水蒸气和乙苯在催化剂作用下反应,测得乙苯的转化率、苯乙烯、苯、甲苯的选择性与时间的关系如下图所示.
的水蒸气和乙苯在催化剂作用下反应,测得乙苯的转化率、苯乙烯、苯、甲苯的选择性与时间的关系如下图所示.
苯乙烯的选择性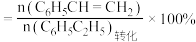
苯的选择性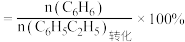
甲苯的选择性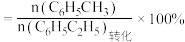
下列说法不正确 的是
反应I:

制备过程中会发生如下两个副反应:
反应Ⅱ:

反应Ⅲ:

在
 下,将质量比为
下,将质量比为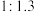 的水蒸气和乙苯在催化剂作用下反应,测得乙苯的转化率、苯乙烯、苯、甲苯的选择性与时间的关系如下图所示.
的水蒸气和乙苯在催化剂作用下反应,测得乙苯的转化率、苯乙烯、苯、甲苯的选择性与时间的关系如下图所示.苯乙烯的选择性
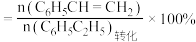
苯的选择性
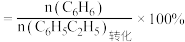
甲苯的选择性
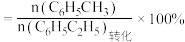
下列说法

| A.曲线a表示乙苯的转化率 |
B. 时,所得 时,所得 的物质的量逐渐减少 的物质的量逐渐减少 |
| C.其他条件不变,增大水蒸气与乙苯的质量比,可以提高乙苯的平衡转化率 |
D. 时,苯乙烯选择性下降的原因之一是反应I生成的 时,苯乙烯选择性下降的原因之一是反应I生成的 促进了反应Ⅲ的进行 促进了反应Ⅲ的进行 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】二氧化碳催化加氢可合成乙烯:
 。当原料初始组成
。当原料初始组成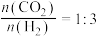 ,体系压强为
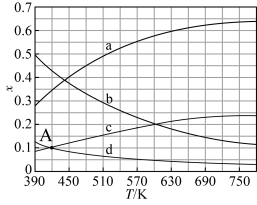
,体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图所示。下列说法正确的是
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图所示。下列说法正确的是

 。当原料初始组成
。当原料初始组成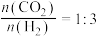 ,体系压强为
,体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图所示。下列说法正确的是
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如题图所示。下列说法正确的是
A.该反应的 |
B.表示 、 、 变化的曲线分别为c、d 变化的曲线分别为c、d |
C.A点对应温度为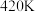 ,此时 ,此时 的转化率为66.7% 的转化率为66.7% |
| D.选择合适的催化剂可提高反应速率和乙烯的平衡产率 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】 和
和 在一定条件下合成甲醇的反应为;
在一定条件下合成甲醇的反应为; 。现在容积均为
。现在容积均为 的a、b、c、d、e五个密闭容器中分别充入
的a、b、c、d、e五个密闭容器中分别充入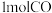 和
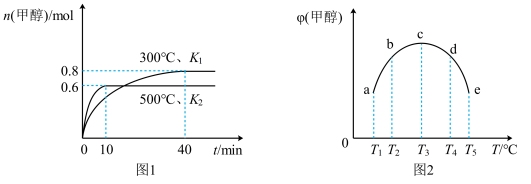
和 的混合气体,控制温度,进行实验,测得相关数据如图(图1:温度分别为300℃、500℃的密闭容器中,甲醇的物质的量:图2:温度分别为
的混合气体,控制温度,进行实验,测得相关数据如图(图1:温度分别为300℃、500℃的密闭容器中,甲醇的物质的量:图2:温度分别为 的密闭容器中,反应均进行到
的密闭容器中,反应均进行到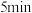 时甲醇的体积分数)。下列叙述正确的是
时甲醇的体积分数)。下列叙述正确的是
 和
和 在一定条件下合成甲醇的反应为;
在一定条件下合成甲醇的反应为; 。现在容积均为
。现在容积均为 的a、b、c、d、e五个密闭容器中分别充入
的a、b、c、d、e五个密闭容器中分别充入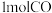 和
和 的混合气体,控制温度,进行实验,测得相关数据如图(图1:温度分别为300℃、500℃的密闭容器中,甲醇的物质的量:图2:温度分别为
的混合气体,控制温度,进行实验,测得相关数据如图(图1:温度分别为300℃、500℃的密闭容器中,甲醇的物质的量:图2:温度分别为 的密闭容器中,反应均进行到
的密闭容器中,反应均进行到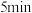 时甲醇的体积分数)。下列叙述正确的是
时甲醇的体积分数)。下列叙述正确的是
A.该反应的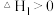 ,且 ,且 |
B.将容器c中的平衡状态转变到容器 中的平衡状态,可采取的措施有升温或加压 中的平衡状态,可采取的措施有升温或加压 |
C.300℃时,向平衡后的容器中再充入 , ,  ,平衡正向移动 ,平衡正向移动 |
D.500℃时,向平衡后的容器中再充入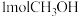 ,重新平衡后, ,重新平衡后, 的百分含量增大 的百分含量增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】向体积为 的某恒容密闭容器中充入
的某恒容密闭容器中充入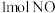 和
和 ,发生反应:
,发生反应:
 。已知反应体系的平衡温度与起始温度相同,体系总压强
。已知反应体系的平衡温度与起始温度相同,体系总压强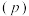 与时间
与时间 的关系如图中曲线I所示,曲线II为只改变某一条件体系总压强随时间的变化曲线。下列说法正确的是。
的关系如图中曲线I所示,曲线II为只改变某一条件体系总压强随时间的变化曲线。下列说法正确的是。
 的某恒容密闭容器中充入
的某恒容密闭容器中充入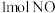 和
和 ,发生反应:
,发生反应:
 。已知反应体系的平衡温度与起始温度相同,体系总压强
。已知反应体系的平衡温度与起始温度相同,体系总压强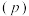 与时间
与时间 的关系如图中曲线I所示,曲线II为只改变某一条件体系总压强随时间的变化曲线。下列说法正确的是。
的关系如图中曲线I所示,曲线II为只改变某一条件体系总压强随时间的变化曲线。下列说法正确的是。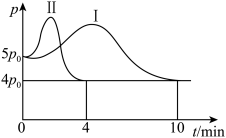
A. ,曲线II改变的条件可能是加入了催化剂 ,曲线II改变的条件可能是加入了催化剂 |
B. 内,曲线I对应的 内,曲线I对应的 |
C.4 时曲线I、II对应的 时曲线I、II对应的 的转化率均为80% 的转化率均为80% |
D.曲线I条件下,反应达平衡时,向平衡体系中同时充入 和 和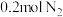 ,此时v(正)>v(逆) ,此时v(正)>v(逆) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】恒压密闭容器中充入H2S和CH4且n(H2S):n(CH4)=2:1,发生反应2H2S(g)+CH4(g) CS2(g)+4H2(g) ΔH。0.11MPa时,温度变化对平衡时各物质的物质的量分数的影响如图所示。下列说法正确的是
CS2(g)+4H2(g) ΔH。0.11MPa时,温度变化对平衡时各物质的物质的量分数的影响如图所示。下列说法正确的是
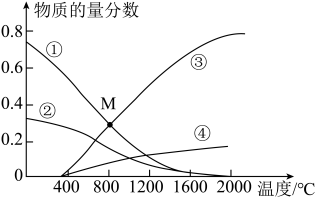
 CS2(g)+4H2(g) ΔH。0.11MPa时,温度变化对平衡时各物质的物质的量分数的影响如图所示。下列说法正确的是
CS2(g)+4H2(g) ΔH。0.11MPa时,温度变化对平衡时各物质的物质的量分数的影响如图所示。下列说法正确的是 
| A.ΔH<0 |
| B.将CS2液化或提高H2S与CH4物质的量的比例均可提高H2S的平衡转化率 |
| C.若向容器中充入Ar(g),反应速率不变,平衡不移动 |
| D.M点的Kp=8×10-4(MPa)2(Kp为以分压表示的平衡常数) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】C(s)+2H2(g) CH4(g) ΔH。在1 L密闭容器中投入1mol碳,并充入2mol H2,测得相关数据如图所示。
CH4(g) ΔH。在1 L密闭容器中投入1mol碳,并充入2mol H2,测得相关数据如图所示。
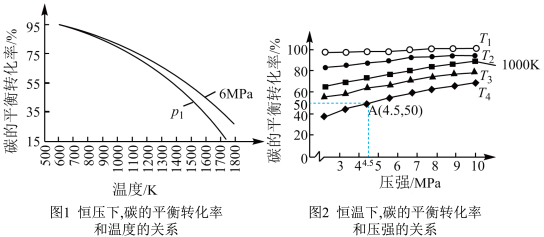
(已知:可用平衡分压代替平衡浓度算出平衡常数Kp,分压=总压×物质的量分数 )下列有关说法错误的
 CH4(g) ΔH。在1 L密闭容器中投入1mol碳,并充入2mol H2,测得相关数据如图所示。
CH4(g) ΔH。在1 L密闭容器中投入1mol碳,并充入2mol H2,测得相关数据如图所示。
(已知:可用平衡分压代替平衡浓度算出平衡常数Kp,分压=总压×物质的量分数 )下列有关说法错误的
| A.ΔH<0 | B.p1<6MPa | C.T1<1 000 K | D.A点的平衡常数Kp=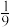 |
您最近一年使用:0次





