某二元酸(化学式用 表示)在水中的电离方程式是
表示)在水中的电离方程式是 ;
; 。下列说法正确的是
。下列说法正确的是
 表示)在水中的电离方程式是
表示)在水中的电离方程式是 ;
; 。下列说法正确的是
。下列说法正确的是A.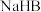 溶液呈碱性 溶液呈碱性 |
B.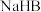 溶液中: 溶液中: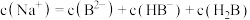 |
C.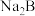 溶液中: 溶液中: |
D.常温下,某 的 的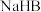 与 与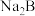 混合液中: 混合液中: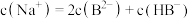 |
更新时间:2023-12-14 09:10:09
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,将HCl气体通入0.1mol/L氨水中,混合溶液中pH与微粒浓度的对数值(lgc)和反应物物质的量之比X[X= ]的关系如图所示(忽略溶液体积的变化),下列说法正确的是
]的关系如图所示(忽略溶液体积的变化),下列说法正确的是
 ]的关系如图所示(忽略溶液体积的变化),下列说法正确的是
]的关系如图所示(忽略溶液体积的变化),下列说法正确的是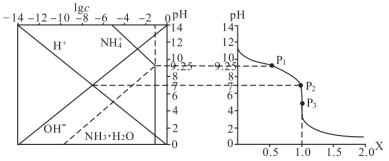
| A.NH3·H2O的电离平衡常数为10-9.25 |
| B.P2点由水电离出的c(H+)=1.0×10-7mol/L |
C.P3为恰好完全反应点,c(Cl-)+c(NH )=0.2mol/L )=0.2mol/L |
| D.P3之后,水的电离程度一直减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】将等物质的量浓度的NaOH(甲)、NH3·H2O(乙)水溶液加水稀释,下列图示能正确表示水电离出的c水(H+)与加入水的体积V的关系的是
A. | B. |
C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下图是0.01mol·L-1甲溶液滴定0.0lmol·L-1乙溶液的导电能力变化曲线,其中曲线③表示盐酸滴定CH3COONa溶液,其他曲线是醋酸溶液滴定NaOH溶液或者NaOH溶液滴定盐酸。下列判断正确的是
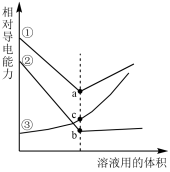

| A.由图可知条件相同时离子导电能力为H+>OH->CH3COO- |
| B.曲线②是NaOH溶液滴定盐酸导电能力变化曲线 |
| C.随着甲溶液体积增大,曲线①始终保持最高导电能力 |
| D.a、b、c三个点不都是反应终点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25℃,浓度均为 、体积为
、体积为 的HX、HY榕液,分别加水稀释至体积V,pH随
的HX、HY榕液,分别加水稀释至体积V,pH随 的变化关系如图所示,下列叙述错误的是
的变化关系如图所示,下列叙述错误的是

 、体积为
、体积为 的HX、HY榕液,分别加水稀释至体积V,pH随
的HX、HY榕液,分别加水稀释至体积V,pH随 的变化关系如图所示,下列叙述错误的是
的变化关系如图所示,下列叙述错误的是
A.相同温度下,电离常数 |
B.HX或HY的电离度: |
C.中和a、b两点溶液,消耗 物质的量相同 物质的量相同 |
D.a点溶液升高温度, 增大 增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知:常温下, 碳酸的电离平衡常数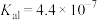 ,
,  。常温下, 向
。常温下, 向  溶液中缓慢滴加
溶液中缓慢滴加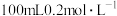 盐酸, 溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸, 溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。
未画出)。

下列说法不正确的是
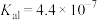 ,
,  。常温下, 向
。常温下, 向  溶液中缓慢滴加
溶液中缓慢滴加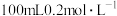 盐酸, 溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示(
盐酸, 溶液中各离子的物质的量随加入盐酸的物质的量的变化如图所示( 和
和 未画出)。
未画出)。
下列说法不正确的是
| A.A点到B点,水的电离程度逐渐减小 |
B.滴加至B点时, |
C.滴加至C点时, |
D.滴加至D点时,溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法正确的是
A.常温下,将0.1mol·L-1NH4Cl溶液与0.05mol·L-1NaOH溶液等体积混合,(pH=9.25):c(Cl-)>c(Na+)>c( )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
B.pH相等的①NH4Cl②(NH4)2SO4③NH4HSO4溶液:c( )大小顺序为①>②>③ )大小顺序为①>②>③ |
| C.常温下,0.1mol·L-1NaHA溶液的pH=8,则溶液中:c(HA-)>c(OH-)>c(H2A)>c(A2-) |
| D.常温下,NaB溶液的pH=8,c(Na+)-c(B-)=9.9×10-9mol·L-1 |
您最近一年使用:0次

 的数目一定小于0.1 NA
的数目一定小于0.1 NA

