河北省石家庄市第十五中学2023-2024学年高二上学期期中考试化学试题
河北
高二
期中
2023-11-29
182次
整体难度:
适中
考查范围:
化学反应原理、认识化学科学、常见无机物及其应用、化学实验基础
河北省石家庄市第十五中学2023-2024学年高二上学期期中考试化学试题
河北
高二
期中
2023-11-29
182次
整体难度:
适中
考查范围:
化学反应原理、认识化学科学、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
1. 下列物质间的转化属于化学变化且能量变化符合图示变化的是
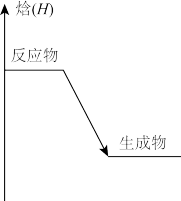

| A.2Cl→Cl2 | B.NaOH(s)溶解 | C.水煤气燃烧 | D.煅烧石灰石 |
您最近一年使用:0次
2022-10-12更新
|
257次组卷
|
6卷引用:河北省故城县高级中学2022-2023学年高二上学期第一次月考化学试题
单选题
|
适中(0.65)
名校
2. 反应 在四种不同情况下的反应速率最快的是
在四种不同情况下的反应速率最快的是
 在四种不同情况下的反应速率最快的是
在四种不同情况下的反应速率最快的是A. | B. |
C. | D.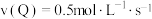 |
您最近一年使用:0次
单选题
|
较易(0.85)
名校
3. 化学反应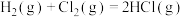
 的能量变化如图所示。下列说法正确的是
的能量变化如图所示。下列说法正确的是

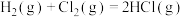
 的能量变化如图所示。下列说法正确的是
的能量变化如图所示。下列说法正确的是
A.升高反应温度, 减小 减小 |
| B.反应物的总能量小于生成物的 |
C.断裂1 mol  键时需要吸收y kJ的能量 键时需要吸收y kJ的能量 |
D.  kJ⋅mol kJ⋅mol |
您最近一年使用:0次
2023-10-28更新
|
185次组卷
|
2卷引用:河北省石家庄市第十五中学2023-2024学年高二上学期期中考试化学试题
单选题
|
适中(0.65)
名校
4. 常温下,有关 和
和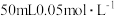 的
的 的说法正确的是
的说法正确的是
 和
和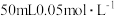 的
的 的说法正确的是
的说法正确的是| A.两者都促进了水的电离 |
B.两溶液中由水电离出的 相等 相等 |
C. 的 的 溶液中: 溶液中: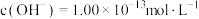 |
D.加入等体积的水稀释后溶液的 |
【知识点】 影响水电离的因素解读 浓度对电离平衡的影响解读
您最近一年使用:0次
2023-11-24更新
|
94次组卷
|
2卷引用:河北省石家庄市第十五中学2023-2024学年高二上学期期中考试化学试题
5. 已知一定条件下:
①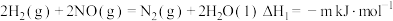 ;
;
② ;
;
③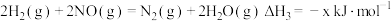 ﹔
﹔
④
下列关系式中正确的是
①
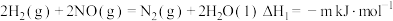 ;
;②
 ;
;③
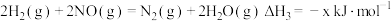 ﹔
﹔④

下列关系式中正确的是
A.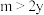 | B.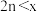 | C.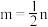 | D. |
您最近一年使用:0次
2023-11-24更新
|
63次组卷
|
3卷引用:河北省故城县高级中学2022-2023学年高二上学期第一次月考化学试题
单选题
|
适中(0.65)
名校
6. 常温下。下列各组离子一定能在指定溶液中大量共存的是
A. 的溶液: 的溶液: |
B.滴加酚酞变红的溶液: |
C.有 存在的强酸性溶液: 存在的强酸性溶液: |
D.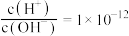 的溶液: 的溶液: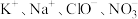 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
7. 已知反应: 。一定条件下,将
。一定条件下,将 和
和 通入
通入 的恒容密闭容器中。反应进行
的恒容密闭容器中。反应进行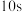 时,测得生成
时,测得生成 。下列说法正确的是
。下列说法正确的是
 。一定条件下,将
。一定条件下,将 和
和 通入
通入 的恒容密闭容器中。反应进行
的恒容密闭容器中。反应进行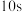 时,测得生成
时,测得生成 。下列说法正确的是
。下列说法正确的是A. 内, 内, |
B.第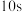 时, 时, |
C.第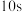 时,NO的浓度为 时,NO的浓度为 |
D. 内, 内, 与 与 反应放出的热量为 反应放出的热量为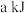 |
【知识点】 化学反应速率的定量表示方法解读 化学反应速率计算解读
您最近一年使用:0次
2023-11-24更新
|
175次组卷
|
4卷引用:河北省石家庄市第十五中学2023-2024学年高二上学期期中考试化学试题
河北省石家庄市第十五中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业02 化学反应速率-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)河北省沧州市部分学校2023-2024学年高二上学期11月期中考试化学试题江西省上饶市广信二中2023-2024学年高二上学期期中考试化学试卷
单选题
|
较易(0.85)
名校
8. NA为阿伏加德罗常数的值。室温下,下列关于1L0.01mol•L-1NaF溶液的说法正确的是
| A.该溶液中F-的数目为0.01NA | B.该溶液中:c(H+)+c(HF)=c(OH-) |
| C.通入HCl至溶液pH=7:c(Na+)=c(F-) | D.加入少量KF固体后,水电离出的c(OH-)减小 |
您最近一年使用:0次
2023-05-11更新
|
194次组卷
|
8卷引用:江苏省响水中学2022-2023学年高二下学期期中考试化学试题
9. 在一定体积的密闭容器中,进行反应
 ,K为化学平衡常数,其中K和温度的关系如下表所示:
,K为化学平衡常数,其中K和温度的关系如下表所示:
根据以上信息推断下列说法错误的是

 ,K为化学平衡常数,其中K和温度的关系如下表所示:
,K为化学平衡常数,其中K和温度的关系如下表所示:T/℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
A.该反应的 |
| B.压强保持不变时,反应达到平衡状态 |
| C.反应达到1000℃时的反应速率比700℃时大 |
| D.K数值越大,反应物的转化率越高 |
您最近一年使用:0次
2023-05-24更新
|
184次组卷
|
9卷引用:河北省承德市重点高中2022-2023学年高一下学期5月月考化学试题
河北省承德市重点高中2022-2023学年高一下学期5月月考化学试题辽宁省鞍山市岫岩满族自治县高级中学2022-2023学年高二上学期10月期中考试化学试题(已下线)选择题6-10河北省石家庄市第十五中学2023-2024学年高二上学期期中考试化学试题安徽省阜阳市城郊中学2023-2024学年高二上学期第一次月考化学试题山西省朔州市怀仁一中2023-2024学年高二上学期12月期中考试化学试题河北省沧州市部分学校2023-2024学年高二上学期11月期中考试化学试题四川省广元市苍溪中学校2023-2024学年高二上学期12月月考化学试题辽宁省本溪市第一中学2023-2024学年高二上学期11月期中考试化学试题
单选题
|
适中(0.65)
名校
10. 实验是研究化学的重要手段。下列操作规范且能达到定量实验目的的是
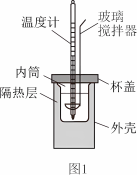
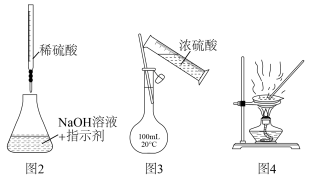


| A.用图1所示装置测定中和反应反应热 |
| B.用图2所示装置测定稀硫酸溶液的浓度 |
C.用图3所示装置配制 一定物质的量浓度的稀硫酸溶液 一定物质的量浓度的稀硫酸溶液 |
D.用图4所示装置加热海水得到 等固体物质 等固体物质 |
您最近一年使用:0次
2023-11-24更新
|
132次组卷
|
3卷引用:河北省石家庄市第十五中学2023-2024学年高二上学期期中考试化学试题
单选题
|
适中(0.65)
名校
11. 下列有关说法正确的是
A. 的 的 溶液中: 溶液中: |
B.用蒸馏水稀释 的醋酸溶液至原溶液体积的10倍其 的醋酸溶液至原溶液体积的10倍其 变为3 变为3 |
C.25℃时,用稀盐酸滴定稀氨水。达到滴定终点时 为7 为7 |
D.等物质的量浓度的 溶液, 溶液, 溶液中水的电离程度; 溶液中水的电离程度; |
您最近一年使用:0次
2023-11-24更新
|
153次组卷
|
2卷引用:河北省石家庄市第十五中学2023-2024学年高二上学期期中考试化学试题
单选题
|
适中(0.65)
名校
解题方法
12. 一定温度下,向容积为 的密闭容器中通入两种气体发生化学反应(已如生成物也为气体),反应中各物质的物质的量变化如图所示,下列对反应的推断正确的是
的密闭容器中通入两种气体发生化学反应(已如生成物也为气体),反应中各物质的物质的量变化如图所示,下列对反应的推断正确的是

 的密闭容器中通入两种气体发生化学反应(已如生成物也为气体),反应中各物质的物质的量变化如图所示,下列对反应的推断正确的是
的密闭容器中通入两种气体发生化学反应(已如生成物也为气体),反应中各物质的物质的量变化如图所示,下列对反应的推断正确的是
A.该反应的化学方程式为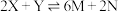 |
B.反应进行到 时, 时, |
C.反应进行到 时,M的平均反应速率为 时,M的平均反应速率为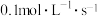 |
D. 时,反应达到平衡,各物质的反应速率相等 时,反应达到平衡,各物质的反应速率相等 |
您最近一年使用:0次
2023-05-24更新
|
109次组卷
|
4卷引用:河北省承德市重点高中2022-2023学年高一下学期5月月考化学试题
单选题
|
适中(0.65)
名校
解题方法
13. 某二元酸(化学式用 表示)在水中的电离方程式是
表示)在水中的电离方程式是 ;
; 。下列说法正确的是
。下列说法正确的是
 表示)在水中的电离方程式是
表示)在水中的电离方程式是 ;
; 。下列说法正确的是
。下列说法正确的是A.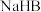 溶液呈碱性 溶液呈碱性 |
B.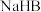 溶液中: 溶液中: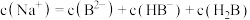 |
C.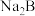 溶液中: 溶液中: |
D.常温下,某 的 的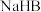 与 与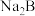 混合液中: 混合液中: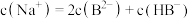 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
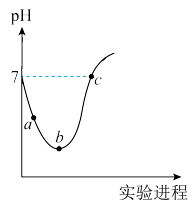
14. 常温下,首先将 缓慢通入水中至饱和,然后向所得饱和氯水中滴加
缓慢通入水中至饱和,然后向所得饱和氯水中滴加 的KOH溶液,整个实验进程中溶液的
的KOH溶液,整个实验进程中溶液的 变化曲线如图所示。下列叙述正确的是
变化曲线如图所示。下列叙述正确的是
 缓慢通入水中至饱和,然后向所得饱和氯水中滴加
缓慢通入水中至饱和,然后向所得饱和氯水中滴加 的KOH溶液,整个实验进程中溶液的
的KOH溶液,整个实验进程中溶液的 变化曲线如图所示。下列叙述正确的是
变化曲线如图所示。下列叙述正确的是
A.用 试纸测a点 试纸测a点 约为b点 约为b点 2倍 2倍 |
B.向a点所示溶液中通入 ﹐溶液的酸性增强 ﹐溶液的酸性增强 |
C.b点溶液中: |
D.c点所示溶液中: |
您最近一年使用:0次
2023-11-24更新
|
209次组卷
|
2卷引用:河北省石家庄市第十五中学2023-2024学年高二上学期期中考试化学试题
二、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
解题方法
15. 电离是电解质在水溶液中的主要行为之一,回答下列问题:
(1)室温下。现有a.盐酸,b.硫酸,c.醋酸三种酸。
①当这三种酸体积相同。物质的量浓度相同时,使其恰好完全反应所需 的物质的量由大到小的顺序是
的物质的量由大到小的顺序是___________ (用a,b,c表示。下同)。
②当这三种酸中的 均为
均为 且体积相同时,分别放入足量的锌。相同状况下产生
且体积相同时,分别放入足量的锌。相同状况下产生 的体积由大到小的顺序是
的体积由大到小的顺序是___________ 。
(2)现用中和滴定法测定某 溶液的浓度。有关数据记录如表:
溶液的浓度。有关数据记录如表:
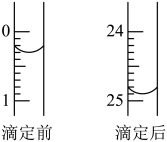
①用___________ 式滴定管盛装 盐酸标准液。如图表示第3次滴定前后
盐酸标准液。如图表示第3次滴定前后 滴定管中液面的位置。该次滴定所用标准盐酸体积为
滴定管中液面的位置。该次滴定所用标准盐酸体积为___________ mL。
②实验室中有石蕊和酚酞两种指示剂,该实验应选用___________ 作指示剂。
③根据实验1、2所给数据计算,该 试样的物质的量浓度为
试样的物质的量浓度为___________
④若操作过程中滴加盐酸速度过快。未充分振荡。刚看到溶液变色,就立刻停止滴定,则会造成测定结果___________ (填“偏低”“偏高”或“无影响”)。
(1)室温下。现有a.盐酸,b.硫酸,c.醋酸三种酸。
①当这三种酸体积相同。物质的量浓度相同时,使其恰好完全反应所需
 的物质的量由大到小的顺序是
的物质的量由大到小的顺序是②当这三种酸中的
 均为
均为 且体积相同时,分别放入足量的锌。相同状况下产生
且体积相同时,分别放入足量的锌。相同状况下产生 的体积由大到小的顺序是
的体积由大到小的顺序是(2)现用中和滴定法测定某
 溶液的浓度。有关数据记录如表:
溶液的浓度。有关数据记录如表:| 实验序号 | 待测液体积/ mL | 所消耗盐酸标准液的体积/mL | ||
| 滴定前读数 | 滴定后读数 | 消耗的体积 | ||
| 1 | 20.00 | 0.50 | 26.80 | 26.30 |
| 2 | 20.00 | 5.00 | 31.34 | 26.34 |
| 3 | 20.00 | —— | —— | —— |
 盐酸标准液。如图表示第3次滴定前后
盐酸标准液。如图表示第3次滴定前后 滴定管中液面的位置。该次滴定所用标准盐酸体积为
滴定管中液面的位置。该次滴定所用标准盐酸体积为
②实验室中有石蕊和酚酞两种指示剂,该实验应选用
③根据实验1、2所给数据计算,该
 试样的物质的量浓度为
试样的物质的量浓度为④若操作过程中滴加盐酸速度过快。未充分振荡。刚看到溶液变色,就立刻停止滴定,则会造成测定结果
您最近一年使用:0次
三、解答题 添加题型下试题
解答题-原理综合题
|
适中(0.65)
名校
解题方法
16. 甲烷是重要的气体燃料和化工原料,由 制取合成气(CO、
制取合成气(CO、 )的反应原理为
)的反应原理为 。回答下列问题:
。回答下列问题:
(1)若生成 ,吸收热量
,吸收热量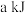 ,相关化学键的键能(断裂
,相关化学键的键能(断裂 化学键所吸收的能量),如表所示。
化学键所吸收的能量),如表所示。
①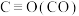 的键能为
的键能为___________ (用含a的式子表示)
②当体系温度等于 时
时 。温度大于T时
。温度大于T时
___________ (填“>”“<”或“=”)0。
③在一定温度下,恒容密闭容器中发生上述反应,下列状态表示反应一定达到平衡状态的有___________ (填标号)。
A. B.气体压强不再变化
B.气体压强不再变化
C.单位时间每消耗 同时产生
同时产生 D.
D. 与
与 的物质的量之比为1:3
的物质的量之比为1:3
(2)在体积为 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,在不同条件下发生反应
,在不同条件下发生反应 ,测得平衡时
,测得平衡时 的体积分数与温度,压强的关系如图所示。
的体积分数与温度,压强的关系如图所示。

①X表示___________ (填“温度”或“压强”),该反应的平衡常数表达式
___________ 。
②m、n、q点的平衡常数由大到小的顺序为___________
③若q点对应的纵坐标为30。此时甲烷的转化率为___________ ,该条件下平衡常数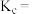
___________ (保留两位有效数字)。
 制取合成气(CO、
制取合成气(CO、 )的反应原理为
)的反应原理为 。回答下列问题:
。回答下列问题:(1)若生成
 ,吸收热量
,吸收热量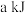 ,相关化学键的键能(断裂
,相关化学键的键能(断裂 化学键所吸收的能量),如表所示。
化学键所吸收的能量),如表所示。| 化学键 | C-H | H-H | H-O |
键能/ | 414 | 436 | 467 |
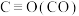 的键能为
的键能为
②当体系温度等于
 时
时 。温度大于T时
。温度大于T时
③在一定温度下,恒容密闭容器中发生上述反应,下列状态表示反应一定达到平衡状态的有
A.
 B.气体压强不再变化
B.气体压强不再变化C.单位时间每消耗
 同时产生
同时产生 D.
D. 与
与 的物质的量之比为1:3
的物质的量之比为1:3(2)在体积为
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,在不同条件下发生反应
,在不同条件下发生反应 ,测得平衡时
,测得平衡时 的体积分数与温度,压强的关系如图所示。
的体积分数与温度,压强的关系如图所示。
①X表示

②m、n、q点的平衡常数由大到小的顺序为
③若q点对应的纵坐标为30。此时甲烷的转化率为
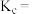
您最近一年使用:0次
2023-11-24更新
|
139次组卷
|
7卷引用:河北省石家庄市第十五中学2023-2024学年高二上学期期中考试化学试题
四、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
17. 氰化钠( )是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。回答下列问题:
)是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。回答下列问题:
(1)氰化钠与硫代硫酸钠的反应为 。已知:
。已知: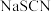 中S为-2价。则
中S为-2价。则 的电子式为
的电子式为___________
(2) 中C元素显+2价,N元素显-3价。说明非金属性
中C元素显+2价,N元素显-3价。说明非金属性 。请设计实验证明:
。请设计实验证明:___________
(3)HCN能与水互溶,造成水污染。已知部分弱酸的电离平衡常数如下表所示:
①25℃时, 的HCN溶液的
的HCN溶液的 约为
约为___________ (结果保留一位小数,已知 )。
)。
②向 溶液中通入少量
溶液中通入少量 ,发生反应的离子方程式为
,发生反应的离子方程式为___________
③等体积、等物质的量浓度的 和
和 溶液中所含离子总数:
溶液中所含离子总数:
___________ (填“>”“<”或“=”) 。
。
(4)常温下,用 的
的 溶液分别滴定
溶液分别滴定 浓度均为
浓度均为 的
的 溶液和HCN溶液,所得滴定曲线如图所示。
溶液和HCN溶液,所得滴定曲线如图所示。

①常温时 的电离常数为
的电离常数为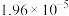 ,
, 的
的 溶液中
溶液中
___________ 
②在a点所示的溶液中溶质为___________ (填化学式)。
③在a点和b点所示溶液中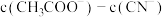
___________  。(填“>”“<”或“=”)
。(填“>”“<”或“=”)
 )是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。回答下列问题:
)是一种白色结晶颗粒,剧毒,易溶于水,水溶液呈碱性,易水解生成氰化氢。回答下列问题:(1)氰化钠与硫代硫酸钠的反应为
 。已知:
。已知: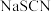 中S为-2价。则
中S为-2价。则 的电子式为
的电子式为(2)
 中C元素显+2价,N元素显-3价。说明非金属性
中C元素显+2价,N元素显-3价。说明非金属性 。请设计实验证明:
。请设计实验证明:(3)HCN能与水互溶,造成水污染。已知部分弱酸的电离平衡常数如下表所示:
| 弱酸 |  | HCN |  |
| 电离平衡常数(25℃) | 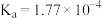 | 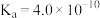 | 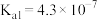 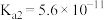 |
 的HCN溶液的
的HCN溶液的 约为
约为 )。
)。②向
 溶液中通入少量
溶液中通入少量 ,发生反应的离子方程式为
,发生反应的离子方程式为③等体积、等物质的量浓度的
 和
和 溶液中所含离子总数:
溶液中所含离子总数:
 。
。(4)常温下,用
 的
的 溶液分别滴定
溶液分别滴定 浓度均为
浓度均为 的
的 溶液和HCN溶液,所得滴定曲线如图所示。
溶液和HCN溶液,所得滴定曲线如图所示。
①常温时
 的电离常数为
的电离常数为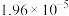 ,
, 的
的 溶液中
溶液中

②在a点所示的溶液中溶质为
③在a点和b点所示溶液中
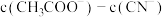
 。(填“>”“<”或“=”)
。(填“>”“<”或“=”)
【知识点】 弱电解质的电离平衡 电离平衡常数及影响因素解读
您最近一年使用:0次
填空题
|
适中(0.65)
名校
18. 水溶液中的离子反应与平衡在生产和生活中有广泛的用途、回答下列问题:
(1)相同条件下, 的氨水和
的氨水和 的氢氧化钠溶液,水的电离程度
的氢氧化钠溶液,水的电离程度___________ (填“相同”或“不同”),向氨水中滴加同浓度的 溶液,滴加过程中
溶液,滴加过程中
___________ (填“增大”“减小”或“不变”)。
(2)某同学在两个相同的特制容器中分别加入 溶液和
溶液和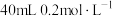
 溶液,再分别用
溶液,再分别用 的盐酸滴定。利用
的盐酸滴定。利用 计和压强传感器检测,得到如图变化曲线。
计和压强传感器检测,得到如图变化曲线。
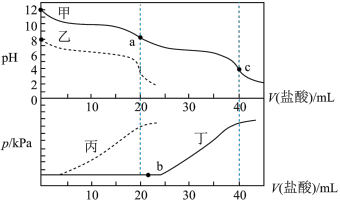
下列说法正确的是___________(填字母)。
(3)在25℃下。将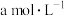 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液。中
的盐酸等体积混合,反应平衡时溶液。中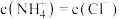 ,则溶液显
,则溶液显___________ (填“酸”“碱”或“中”)性;用含a的代数式表示 的电离常数
的电离常数
___________
(4)在一定温度下,用 溶液将
溶液将 转化为
转化为 溶液,实验测得
溶液,实验测得 溶液中
溶液中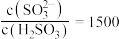 ,则该溶液的
,则该溶液的 为
为___________ (已知:该温度下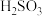 的
的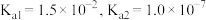 )。
)。
(5)关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下:
①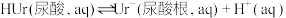 ;
;
② 。
。
37℃时某人尿液试样中: ,其中
,其中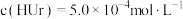 (37℃时,
(37℃时,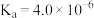 ),则该尿液试样中
),则该尿液试样中 为
为___________ (结果保留两位有效数字)。
(1)相同条件下,
 的氨水和
的氨水和 的氢氧化钠溶液,水的电离程度
的氢氧化钠溶液,水的电离程度 溶液,滴加过程中
溶液,滴加过程中
(2)某同学在两个相同的特制容器中分别加入
 溶液和
溶液和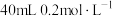
 溶液,再分别用
溶液,再分别用 的盐酸滴定。利用
的盐酸滴定。利用 计和压强传感器检测,得到如图变化曲线。
计和压强传感器检测,得到如图变化曲线。
下列说法正确的是___________(填字母)。
A. 溶液和 溶液和 溶液中微粒种类相同 溶液中微粒种类相同 |
B.图中曲线甲和丁表示向 溶液中滴加盐酸 溶液中滴加盐酸 |
C.在b点发生反应的离子方程式为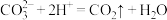 |
| D.滴定分析时,a点可用酚酞、c点可用甲基橙作指示剂指示滴定终点 |
(3)在25℃下。将
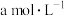 的氨水与
的氨水与 的盐酸等体积混合,反应平衡时溶液。中
的盐酸等体积混合,反应平衡时溶液。中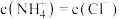 ,则溶液显
,则溶液显 的电离常数
的电离常数
(4)在一定温度下,用
 溶液将
溶液将 转化为
转化为 溶液,实验测得
溶液,实验测得 溶液中
溶液中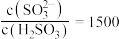 ,则该溶液的
,则该溶液的 为
为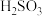 的
的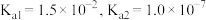 )。
)。(5)关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下:
①
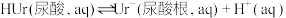 ;
;②
 。
。37℃时某人尿液试样中:
 ,其中
,其中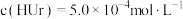 (37℃时,
(37℃时,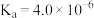 ),则该尿液试样中
),则该尿液试样中 为
为
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:化学反应原理、认识化学科学、常见无机物及其应用、化学实验基础
试卷题型(共 18题)
题型
数量
单选题
14
填空题
3
解答题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 化学反应中能量变化的原因 常见能量转化形式 吸热反应和放热反应 | |
| 2 | 0.65 | 化学反应的速率 化学反应速率计算 化学反应速率与化学计量数之间的关系 | |
| 3 | 0.85 | 化学键与化学反应中的能量关系 热化学方程式书写及正误判断 | |
| 4 | 0.65 | 影响水电离的因素 浓度对电离平衡的影响 | |
| 5 | 0.65 | 盖斯定律的应用 依据热化学方程式的计算 反应热大小比较 化学反应速率与化学计量数之间的关系 | |
| 6 | 0.65 | 限定条件下的离子共存 硝酸的强氧化性 水的离子积常数 | |
| 7 | 0.65 | 化学反应速率的定量表示方法 化学反应速率计算 | |
| 8 | 0.85 | 盐类水解规律理解及应用 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 9 | 0.85 | 化学平衡状态的判断方法 化学平衡常数的影响因素及应用 | |
| 10 | 0.65 | 中和热的测定与误差分析 酸碱中和滴定实验基本操作及步骤 配制一定物质的量浓度的溶液的步骤、操作 | |
| 11 | 0.65 | 酸碱中和滴定原理的应用 一元强酸与一元弱酸的比较 盐溶液中离子浓度大小的比较 | |
| 12 | 0.65 | 化学平衡的有关计算 化学平衡图像分析 | |
| 13 | 0.65 | 弱电解质的电离平衡 弱电解质在水溶液中的电离平衡 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 | |
| 14 | 0.65 | 氯水的性质 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 二、填空题 | |||
| 15 | 0.65 | 酸碱中和滴定的综合考查 弱电解质在水溶液中的电离平衡 | |
| 17 | 0.65 | 弱电解质的电离平衡 电离平衡常数及影响因素 | |
| 18 | 0.65 | 弱电解质在水溶液中的电离平衡 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 弱电解质的电离平衡常数 | |
| 三、解答题 | |||
| 16 | 0.65 | 根据△H=反应物的键能之和-生成物的键能之和进行计算 化学平衡状态的判断方法 化学平衡常数的有关计算 转化率的相关计算及判断 | 原理综合题 |



