制备水煤气的反应C(s)+H2O(g) H2(g)+CO(g) ΔH>0,下列说法正确的是
H2(g)+CO(g) ΔH>0,下列说法正确的是
 H2(g)+CO(g) ΔH>0,下列说法正确的是
H2(g)+CO(g) ΔH>0,下列说法正确的是| A.该反应 ΔS<0 |
| B.升高温度,反应速率增大,平衡正向移动 |
| C.恒温下,增大总压,H2O(g)的平衡转化率不变 |
| D.恒温恒压下,加入催化剂,平衡常数增大 |
更新时间:2024-01-10 12:13:50
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】工业生产硫酸的一步重要反应是SO2在400℃到500℃下的催化氧化:2SO2(g)+O2(g) 2SO3(g) △H<0,如果反应在密闭容器中进行,下列有关说法不正确的是
2SO3(g) △H<0,如果反应在密闭容器中进行,下列有关说法不正确的是
 2SO3(g) △H<0,如果反应在密闭容器中进行,下列有关说法不正确的是
2SO3(g) △H<0,如果反应在密闭容器中进行,下列有关说法不正确的是| A.实际生产中选定400℃到500℃作为操作温度,其原因是在此温度下催化剂的活性最高 |
| B.使用催化剂可加快反应速率,SO3产率不变 |
| C.增大压强可以提高SO3产率,但高压对动力和设备要求太高,会增加生产成本 |
| D.其他条件保持不变,温度越高,速率越快,生产效益越好 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】反应“
 ”的速率方程可表示
”的速率方程可表示 ,其中k为速率常数,常温下,实验测得反应的数据如下:
,其中k为速率常数,常温下,实验测得反应的数据如下:
下列说法错误的是

 ”的速率方程可表示
”的速率方程可表示 ,其中k为速率常数,常温下,实验测得反应的数据如下:
,其中k为速率常数,常温下,实验测得反应的数据如下:| 实验编号 | 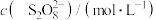 |  |  |
| ① | 1.0×10-4 |  | 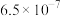 |
| ② |  |  | 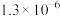 |
| ③ |  |  |  |
| ④ |  |  |  |
| A.m=1;n=3 |
B. |
| C.增大压强,该反应速率不变 |
| D.升高温度,速率常数k增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)  2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
① b<f ② 915℃、2.0 MPa时E的转化率为60% ③ 增大压强平衡左移 ④ K(1000℃)>K(810℃) 上述①~④中正确的有
 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:| 压强/Mpa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
810 | 54.0 | a | b |
915 | c | 75.0 | d |
1000 | e | f | 83.0 |
① b<f ② 915℃、2.0 MPa时E的转化率为60% ③ 增大压强平衡左移 ④ K(1000℃)>K(810℃) 上述①~④中正确的有
| A.4个 | B.3个 | C.2个 | D.1个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
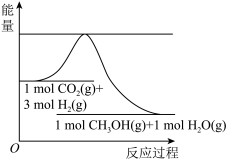
【推荐2】目前工业上有一种方法是用 生产燃料甲醇。一定条件下发生反应:
生产燃料甲醇。一定条件下发生反应:
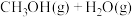 ,该反应进行过程中能量变化如图所示。下列说法正确的是
,该反应进行过程中能量变化如图所示。下列说法正确的是
 生产燃料甲醇。一定条件下发生反应:
生产燃料甲醇。一定条件下发生反应:
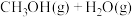 ,该反应进行过程中能量变化如图所示。下列说法正确的是
,该反应进行过程中能量变化如图所示。下列说法正确的是
A.减小压强有利于生成 |
B.升高温度有利于平衡向生成 的方向移动 的方向移动 |
C.降低温度能使平衡混合物中 增大 增大 |
D.加入催化剂能使平衡混合物中 增大 增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】某温度下进行2SO2(g)+SO2(g)⇌2SO3,该温度下甲、乙、丙三个相同的恒容密闭容器中,投入SO2(g)和O2(g)的起始浓度如下表所示。则下列判断不正确的是
| 起始浓度 | 甲 | 乙 | 丙 |
| c(SO2)/mol·L-1 | 0.10 | 0.10 | 0.20 |
| c(O2)/mol·L-1 | 0.10 | 0.20 | 0.20 |
| A.平衡时,甲中O2的转化率大于乙 |
| B.平衡时,丙中SO2的转化率大于甲 |
| C.反应初始,丙的反应速率最快,甲最慢 |
| D.平衡时,丙中c(SO2)是甲中的2倍 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在一定温度下,将一定质量的混合气体在密闭容器中发生反应aA(g)+bB(g) cC(g)+dD(g),达到平衡时测得B气体的浓度为0.6mol/l,恒温下将密闭容器的容积扩大一倍,重新达到平衡时,测得B气体的浓度为 0.4mol/l,下列叙述中正确的是( )
cC(g)+dD(g),达到平衡时测得B气体的浓度为0.6mol/l,恒温下将密闭容器的容积扩大一倍,重新达到平衡时,测得B气体的浓度为 0.4mol/l,下列叙述中正确的是( )
 cC(g)+dD(g),达到平衡时测得B气体的浓度为0.6mol/l,恒温下将密闭容器的容积扩大一倍,重新达到平衡时,测得B气体的浓度为 0.4mol/l,下列叙述中正确的是( )
cC(g)+dD(g),达到平衡时测得B气体的浓度为0.6mol/l,恒温下将密闭容器的容积扩大一倍,重新达到平衡时,测得B气体的浓度为 0.4mol/l,下列叙述中正确的是( )| A.a+b>c+d |
| B.平衡向右移动 |
| C.重新达平衡时,A气体浓度增大 |
| D.重新达平衡时,B的体积分数减小 |
您最近一年使用:0次

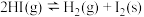 (反应放热)。若0~15s内
(反应放热)。若0~15s内 由0.1
由0.1 降到0.07
降到0.07 表示的平均反应速率为
表示的平均反应速率为
 进行过程中,当其他条件不变时,
进行过程中,当其他条件不变时, 的体积分数
的体积分数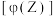 与温度
与温度 、压强
、压强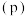 的关系如图所示。下列叙述正确的是
的关系如图所示。下列叙述正确的是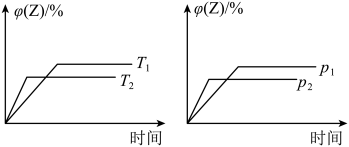
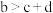
 的量,平衡向正反应方向移动
的量,平衡向正反应方向移动 pC(g)+qD(g)中,A和D都是无色气体,达到平衡后,下列叙述正确的是(
pC(g)+qD(g)中,A和D都是无色气体,达到平衡后,下列叙述正确的是(

