NA表示阿伏加德罗常数的具体数值。下列叙述正确的是
| A.18g重水(D2¹⁸O)中含有的质子数为10NA |
B.32g环状 S8分子( )中含有的S-S 键数为NA )中含有的S-S 键数为NA |
C.1LpH=4的0.1mol/LK2Cr2O7溶液中Cr2O 离子数为0.1NA 离子数为0.1NA |
| D.1L0.1mol/LCH3COOH溶液通氨气至中性, 铵根离子数为0.1NA |
更新时间:2024-01-13 09:51:37
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.常温下, 的 的 溶液中,水电离出的 溶液中,水电离出的 数为 数为 |
B.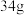 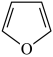 中含有的极性键数目为 中含有的极性键数目为 |
C.在反应 中,每生成 中,每生成 转移的电子数为 转移的电子数为 |
D. 时, 时, 的 的 溶液中 溶液中 数目为 数目为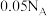 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA代表阿伏加 德罗常数的值,下列说法正确的是( )
A.0.1 mol/L Na2SO4溶液中含有Na+和 的总物质的量为0.3 mol 的总物质的量为0.3 mol |
| B.常温常压下,22.4 LO2中所含的原子数小于2NA |
| C.标准状况下, 11.2 L乙醇(CH3CH2OH)中含有0.5NA个分子 |
D.1.8 g  中含有的电子数为1.1NA 中含有的电子数为1.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温常压下,46gNO2和N2O4混合气体中所含的原子总数为3NA |
B.反应4FeS2+11O2 2Fe2O3+8SO2每生成1molFe2O3转移电子总数为44NA 2Fe2O3+8SO2每生成1molFe2O3转移电子总数为44NA |
| C.12mol/L的浓硫酸50mL与足量的Cu加热反应,得到SO2为0.3NA |
| D.密闭容器中,2molSO2和1molO2催化反应后分子总数为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是
 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是A.1mol 被还原为 被还原为 转移的电子数为3 转移的电子数为3 |
B.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.4 |
C.28g氮气和一氧化碳混合气体所含质子数为28 |
D. 和 和 混合气体中含有原子数为3 混合气体中含有原子数为3 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设NA表示阿伏加 德罗常数,下列说法正确的是( )
| A.标况下,11.2L甲醇中含有的电子数9NA |
| B.6.0g甲醛(HCHO)和醋酸的混合物中含有的原子总数为0.8NA |
| C.100mL0.1mol/L的KAl(SO4)2溶液中含有的阳离子总数小于0.02NA |
| D.分别由H2O2和KMnO4制备等量的氧气转移的电子数目相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.含有 个氢原子的氢气在标准状况下的体积约为22.4L 个氢原子的氢气在标准状况下的体积约为22.4L |
B.常温常压下,1.8g 中含电子数为 中含电子数为 |
C.将标准状况下体积为0.224L 通入水中,制成氯水,氯水中含有 通入水中,制成氯水,氯水中含有 数等于0.02 数等于0.02 |
D.1  熔融时电离产生的离子数为4 熔融时电离产生的离子数为4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】某科研小组研究臭氧脱除SO2和NO工艺,反应原理及反应热、活化能数据如下:
反应I:NO(g)+O3(g) NO2(g)+O2(g)∆H1=-200.9kJ·mol-1 Ea1=+3.2kJ·mol-1
NO2(g)+O2(g)∆H1=-200.9kJ·mol-1 Ea1=+3.2kJ·mol-1
反应II:SO2(g)+O3(g) SO3(g)+O2(g)∆H2=-241.6kJ·mol-1 Ea2=+58kJ·mol-1
SO3(g)+O2(g)∆H2=-241.6kJ·mol-1 Ea2=+58kJ·mol-1
已知该体系中臭氧发生分解反应:2O3(g) 3O2(g)。
3O2(g)。
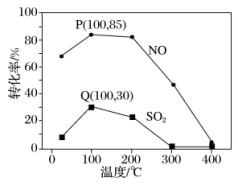
向容积一定的反应器中充入含1.0molNO、1.0mol SO2的模拟烟气和2.0mol O3,改变温度,反应相同时间t后体系中NO和SO2的转化率如图所示,下列说法正确的是
反应I:NO(g)+O3(g)
 NO2(g)+O2(g)∆H1=-200.9kJ·mol-1 Ea1=+3.2kJ·mol-1
NO2(g)+O2(g)∆H1=-200.9kJ·mol-1 Ea1=+3.2kJ·mol-1反应II:SO2(g)+O3(g)
 SO3(g)+O2(g)∆H2=-241.6kJ·mol-1 Ea2=+58kJ·mol-1
SO3(g)+O2(g)∆H2=-241.6kJ·mol-1 Ea2=+58kJ·mol-1已知该体系中臭氧发生分解反应:2O3(g)
 3O2(g)。
3O2(g)。向容积一定的反应器中充入含1.0molNO、1.0mol SO2的模拟烟气和2.0mol O3,改变温度,反应相同时间t后体系中NO和SO2的转化率如图所示,下列说法正确的是

| A.P点一定为平衡状态点 |
| B.相同温度下NO的转化率远高于SO2,主要原因是Ea1小于Ea2 |
| C.300℃后,NO和SO2的转化率随温度升高显著下降,主要是因为升温平衡逆向移动。 |
| D.其他条件不变,若缩小反应器的容积不能提高NO和SO2的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知NO2与N2O4可相互转化:2NO2(g)⇌N2O4(g) ΔH=-24.2 kJ/mol,在恒温下,将一定量NO2和N2O4的混合气体充入体积为2 L的密闭容器中,其中物质的量浓度随时间变化的关系如图所示。下列推理分析不合理的是


| A.b点所在的曲线代表NO2 |
| B.b、d两点均有v(正)=v(逆) |
| C.25 min时改变的条件可能是升高温度 |
| D.25 min时,正反应速率增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温下,下列有关溶液的叙述正确的是
| A.0.1mol·L-1CH3COONa溶液与0.05mol·L-1盐酸等体积混合后的酸性溶液中:c(CH3COO-)>c(CH3COOH)>c(Cl-)>c(H+) |
B.在0.1mol·L-1Na2C2O4溶液中: |
C.等浓度的①(NH4)2SO4②NH4HSO4③NH4Cl三种溶液中c( )大小:①>③>② )大小:①>③>② |
| D.pH=6的醋酸溶液和pH=6的NH4Cl溶液,由水电离出的c(H+)均为1×10-8mol·L-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】鸟嘌呤(G)是一种有机弱碱,可与盐酸反应生成盐酸盐(用 表示)。已知
表示)。已知 水溶液呈酸性,下列叙述正确的是
水溶液呈酸性,下列叙述正确的是
 表示)。已知
表示)。已知 水溶液呈酸性,下列叙述正确的是
水溶液呈酸性,下列叙述正确的是A.0.01mol/L 水溶液的 水溶液的 |
B. 在水中的电离方程式为: 在水中的电离方程式为: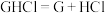 |
C.0.01mol/L 水溶液加水稀释, 水溶液加水稀释, 升高 升高 |
D.0.01mol/L 水溶液中: 水溶液中: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.1L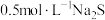 溶液中含 溶液中含 和 和 的离子总数为 的离子总数为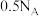 |
B.标准状况下,22.4L 中C—Cl键的数目为 中C—Cl键的数目为 |
C.一定条件下,Na与 反应生成7.8g 反应生成7.8g ,转移电子的个数为 ,转移电子的个数为 |
D.1mol 和1mol 和1mol 在密闭容器中充分反应,所得混合气体的分子数小于 在密闭容器中充分反应,所得混合气体的分子数小于 |
您最近一年使用:0次

 水解反应:
水解反应:
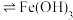 (红褐色)+3HCl的条件。
(红褐色)+3HCl的条件。 固体
固体 固体
固体



