2SO2(g)+O2(g)  2SO3(g) ΔH 的反应机理如下:
2SO3(g) ΔH 的反应机理如下:
反应I:V2O5(s)+SO2(g) V2O4(s)+SO3(g) ΔH1=+24 kJ·mol-1
V2O4(s)+SO3(g) ΔH1=+24 kJ·mol-1
反应II:2V2O4(s)+O2(g) 2V2O5(s) ΔH2=-246 kJ·mol-1
2V2O5(s) ΔH2=-246 kJ·mol-1
反应中的能量变化如图,下列说法不正确的是

 2SO3(g) ΔH 的反应机理如下:
2SO3(g) ΔH 的反应机理如下:反应I:V2O5(s)+SO2(g)
 V2O4(s)+SO3(g) ΔH1=+24 kJ·mol-1
V2O4(s)+SO3(g) ΔH1=+24 kJ·mol-1反应II:2V2O4(s)+O2(g)
 2V2O5(s) ΔH2=-246 kJ·mol-1
2V2O5(s) ΔH2=-246 kJ·mol-1反应中的能量变化如图,下列说法不正确的是

| A.ΔH=-198kJ·mol-1 | B.反应速率由反应I决定 |
| C.反应II的平衡常数K=c-1(O2) | D.通入过量空气,可提高SO2的平衡转化率 |
更新时间:2024-01-28 09:25:56
|
相似题推荐
【推荐1】如图是金属镁和卤素单质(X2)反应的能量变化示意图。下列说法正确的是( )


| A.热稳定性:MgF2 <MgCl2<MgBr2<MgI2 |
| B.22.4LF2(g)与足量的Mg充分反应,放热1124kJ |
| C.工业上可由电解MgCl2溶液冶炼金属Mg,该过程需要吸收热量 |
| D.由图可知:MgBr2(s)+Cl2(g)=MgCl2(s)+Br2(l) ∆H<-117kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用 催化还原
催化还原 ,可以消除氨氧化物的污染。例如:
,可以消除氨氧化物的污染。例如:
①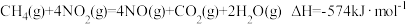
②
下列说法正确的是
 催化还原
催化还原 ,可以消除氨氧化物的污染。例如:
,可以消除氨氧化物的污染。例如:①
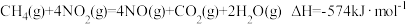
②

下列说法正确的是
A.由反应①可知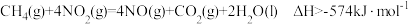 |
B.反应②中当 完全反应时,电子转移数目为 完全反应时,电子转移数目为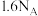 |
C.若用标准状况下 还原 还原 生成 生成 和水蒸气,放出的热量为 和水蒸气,放出的热量为 |
D.一定条件下,若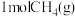 与 与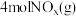 分别发生反应①和②,共放出热量为 分别发生反应①和②,共放出热量为 ,则 ,则 与 与 的体积比为 的体积比为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用钛(Ru)基催化剂催化CO2(g)和H2(g)反应生成2mol液态HCOOH放出62.4kJ热量的图示如图,下列说法正确的是
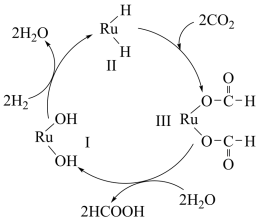

| A.图示中物质Ⅱ为该反应的催化剂 |
| B.图示中参与循环的物质只有CO2和H2 |
| C.该反应的活化能为62.4kJ•mol-1 |
| D.该反应的热化学方程式为H2(g)+CO2(g)=HCOOH(l) △H=-31.2kJ•mol-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】利用计算机技术测得在甲、乙两种催化剂作用下由正丁烷(g)制备1-丁烯(g)的反应历程如下,其中甲、乙催化剂表面的物种均用*号标注,过渡态均用TS表示,下列说法中正确的是
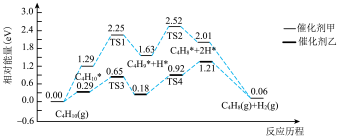

A.选用催化剂甲时的最高能垒(活化能 )为 )为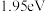 |
B.选用催化剂乙时,相对能量从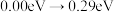 的过程为正丁烷的吸附过程 的过程为正丁烷的吸附过程 |
C.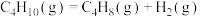 为放热反应 为放热反应 |
| D.若只从平均反应速率快慢角度考虑,生产中适宜选用催化剂甲 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知反应:2NO(g) + Br2(g) 2NOBr(g) ΔH = -a kJ·mol-1(a﹥0),其反应机理如下:
2NOBr(g) ΔH = -a kJ·mol-1(a﹥0),其反应机理如下:
① NO(g) + Br2(g) NOBr2(g) 快
NOBr2(g) 快
② NO(g) + NOBr2(g) 2NOBr(g) 慢
2NOBr(g) 慢
下列有关该反应的说法不正确 的是
 2NOBr(g) ΔH = -a kJ·mol-1(a﹥0),其反应机理如下:
2NOBr(g) ΔH = -a kJ·mol-1(a﹥0),其反应机理如下:① NO(g) + Br2(g)
 NOBr2(g) 快
NOBr2(g) 快 ② NO(g) + NOBr2(g)
 2NOBr(g) 慢
2NOBr(g) 慢下列有关该反应的说法
| A.该反应的速率主要取决于②的快慢 |
| B.NOBr2是该反应的中间产物 |
| C.正反应的活化能比逆反应的活化能小a kJ·mol-1 |
| D.增大Br2(g)的浓度能增大活化分子百分数,加快反应速率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列事实不能用平衡移动原理解释的是
| A.红棕色的NO2,加压后颜色先变深后变浅,但比原来要深 |
| B.高压比常压有利于SO2合成SO3的反应 |
| C.500 ℃时比室温更利于合成氨 |
| D.氯水在光照条件下颜色变浅,最终变为无色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】用如图所示实验装置进行相应实验,不能达到实验目的的是
| A | B | C | D |
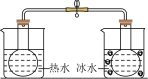 | 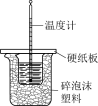 | 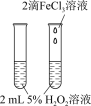 | 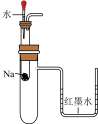 |
探究温度对反应 平衡的影响 平衡的影响 | 测定酸碱中和反应的反应热 | 验证 对 对 分解反应有催化作用 分解反应有催化作用 | 验证 与水反应为放热反应 与水反应为放热反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】一种从含砷废水[砷主要以亚砷酸(H3AsO3)形式存在]中回收砷的工艺流程如图:
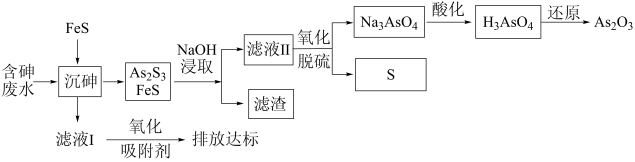
已知:
I.As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
II.As2S3(s)+3S2-(aq) 2AsS
2AsS (aq)
(aq)
III.砷酸(H3AsO4)在酸性条件下有强氧化性,能被氢碘酸等还原
下列说法错误的是

已知:
I.As2S3+6NaOH=Na3AsO3+Na3AsS3+3H2O
II.As2S3(s)+3S2-(aq)
 2AsS
2AsS (aq)
(aq)III.砷酸(H3AsO4)在酸性条件下有强氧化性,能被氢碘酸等还原
下列说法错误的是
| A.As2S3中砷元素的化合价为+3价 |
| B.“沉砷”过程中FeS可以用过量的Na2S代替 |
C.用氧气进行“氧化脱硫”涉及离子方程式AsS +2O2=AsO +2O2=AsO +3S↓ +3S↓ |
| D.能用氢碘酸、淀粉溶液检验还原后溶液中是否仍存在砷酸 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在温度 和
和 时,分别将0.5mol NO和2.0mol固体活性炭充入体积为2L的密闭容器中,发生如下反应:
时,分别将0.5mol NO和2.0mol固体活性炭充入体积为2L的密闭容器中,发生如下反应: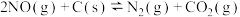 。测
。测 随时间变化数据如下表:
随时间变化数据如下表:
下列说法正确的是
 和
和 时,分别将0.5mol NO和2.0mol固体活性炭充入体积为2L的密闭容器中,发生如下反应:
时,分别将0.5mol NO和2.0mol固体活性炭充入体积为2L的密闭容器中,发生如下反应: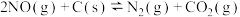 。测
。测 随时间变化数据如下表:
随时间变化数据如下表:时间/min | 0 | 10 | 20 | 40 | 50 | |
|
| 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
|
| 0.50 | 0.30 | 0.18 | …… | 0.15 |
A.温度为 时,前10min内, 时,前10min内, 的平均反应速率为 的平均反应速率为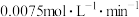 |
B.由表格数据可知,温度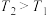 ,故该反应平衡常数 ,故该反应平衡常数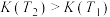 |
C.温度为 时, 时,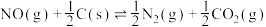 ,此反应的平衡常数约为1.17 ,此反应的平衡常数约为1.17 |
D.温度为 时,平衡后再充入0.10mol NO,再次达到平衡,NO的百分含量增大 时,平衡后再充入0.10mol NO,再次达到平衡,NO的百分含量增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
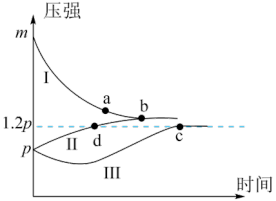
【推荐2】一定条件下,分别向体积为1L的密闭容器中充入气体,发生反应Z (g)  2X(g)+Y(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
2X(g)+Y(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
 2X(g)+Y(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
2X(g)+Y(g),测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
| 实验 | 充入气体量 | 反应过程条件 |
| ① | 2mol X+1mol Y | 恒温 |
| ② | 1molZ | 恒温 |
| ③ | 1molZ | 绝热 |
| A.曲线Ⅰ对应实验①,且3m=p | B.Z的转化率:b<c |
C.气体的总物质的量: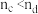 | D.b点平衡常数: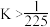 |
您最近一年使用:0次

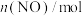
 和
和 ,其反应原理如下图所示。已知该反应在不同温度下的平衡常数如下表。下列说法正确的是
,其反应原理如下图所示。已知该反应在不同温度下的平衡常数如下表。下列说法正确的是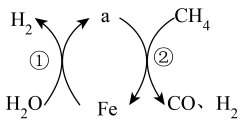
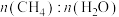 的比值,CH4的平衡转化率增大
的比值,CH4的平衡转化率增大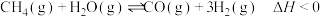

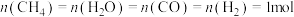 ,则
,则