已知A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。
(1)写出BA3的电子式___________ 。
(2)B基态原子中能量最高的电子,其电子云在空间有___________ 个方向,原子轨道呈___________ 形。
(3)实验室制备E的单质的离子反应方程式为___________ 。
(4)B和A中非金属性较强的是___________ (填元素的符号)。
(5)C与D的第一电离能大小为___________ 。
(6)G价电子排布图为___________ ,位于___________ 区。
(7)F元素的原子结构示意图为___________ ,前四周期中未成对电子数最多的元素在周期表中位置为___________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是:I1=738kJ/molI2=1451kJ/mol I3=7733kJ/molI4=10540kJ/mol |
| D元素简单离子半径是该周期中最小的 |
| E元素是该周期电负性最大的元素 |
| F所在族的元素种类是周期表中最多的 |
| G在周期表的第十一列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
(3)实验室制备E的单质的离子反应方程式为
(4)B和A中非金属性较强的是
(5)C与D的第一电离能大小为
(6)G价电子排布图为
(7)F元素的原子结构示意图为
更新时间:2024-02-04 18:55:38
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】短周期主族元素A、B、C、D、E原子序数依次增大。A、E同主族,E原子最外层上的电子数是D原子最外层电子数的4倍,D离子与C2-具有相同核外电子排布。
试回答下列问题:
(1)元素E在元素周期表中的位置是______ 。
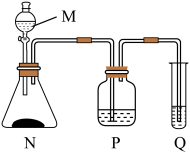
(2)A和E最高价氧化物对应的水化物,酸性较弱的为_____ 。若用图中装置验证这两种酸的酸性强弱,则在仪器P中加入的试剂为_____ ,Q中观察到的实验现象是_____ 。
(3)由以上五种元素组成的物质,其组成和结构信息如下表:
①a含有的化学键有_____ 。
②b与c反应的化学方程式为_____ 。

试回答下列问题:
(1)元素E在元素周期表中的位置是
(2)A和E最高价氧化物对应的水化物,酸性较弱的为
(3)由以上五种元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A、C、D的盐 |
| b | C、D组成的化合物,且原子数之比为1∶1 |
| c | 化学组成为AC2 |
②b与c反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A、B两元素的最外层都只有一个电子,A的原子序数等于B的原子序数的11倍,A离子的电子层结构与周期表中非金属性最强的元素的阴离子的电子层结构相同;元素C与B易形成化合物B2C,该化合物常温下呈液态,则:
(1)A的原子结构示意图为____ ,在固态时属于___ 晶体。
(2)C的单质属于___ 晶体。B与C形成化合物B2C的化学式为___ ,电子式为____ ;它是由___ 键形成的___ 分子,在固态时属于___ 晶体。
(1)A的原子结构示意图为
(2)C的单质属于
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)汞的原子结构示意图 ,写出汞在周期表中的位置
,写出汞在周期表中的位置___________ 。
(2)下列有关性质的比较能用元素周期律解释的是___________。
(3)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断错误的是___________ 。
A.硒元素的最低负化合价为-2价
B.二氧化硒(SeO2)具有还原性
C.硒的氧化物对应的水化物属于强酸
(4)某种化合物是工业洗涤剂的中间体,其结构如图所示。其中X、Y、Z、Q、W为原子序数依次增大的五种短周期元素,Q最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。回答下列问题:
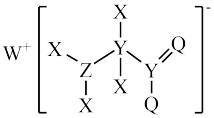
①Z单质的结构式为___________ 。
②Y、Z、Q三种元素所形成的简单气态氢化物中,稳定性最强的是___________ (填化学式);X、Y、Z、Q四种元素组成的化合物中,既含离子键又含共价键的是___________ (填化学式,一种即可)。
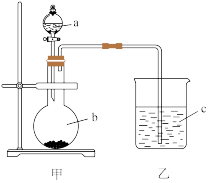
③利用如图装置可比较Y、Z两元素原子的得电子能力,b中发生反应的化学方程式为___________ 。
(1)汞的原子结构示意图
 ,写出汞在周期表中的位置
,写出汞在周期表中的位置(2)下列有关性质的比较能用元素周期律解释的是___________。
| A.酸性:HCl>H2SO3 | B.非金属性:O>S |
| C.碱性:NaOH>Mg(OH)2 | D.热稳定性:Na2CO3>NaHCO3 |
A.硒元素的最低负化合价为-2价
B.二氧化硒(SeO2)具有还原性
C.硒的氧化物对应的水化物属于强酸
(4)某种化合物是工业洗涤剂的中间体,其结构如图所示。其中X、Y、Z、Q、W为原子序数依次增大的五种短周期元素,Q最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。回答下列问题:

①Z单质的结构式为
②Y、Z、Q三种元素所形成的简单气态氢化物中,稳定性最强的是
③利用如图装置可比较Y、Z两元素原子的得电子能力,b中发生反应的化学方程式为

您最近一年使用:0次
【推荐1】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为_______ ,最高能级电子的电子云轮廓形状为_______ 。
(2)比较下列锗卤化物的熔点和沸点,分析其变化的原因_______ 。
(3)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是_______ 。
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的作用力是_______ 。
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, );C为(
);C为(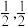 ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为_______ 。
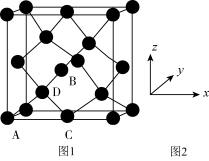
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76pm,其密度为_______ g·cm-3(列出计算式即可)。
(1)基态Ge原子的核外电子排布式为
(2)比较下列锗卤化物的熔点和沸点,分析其变化的原因
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | −49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(4)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
(5)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, );C为(
);C为(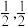 ,0)。则D原子的坐标参数为
,0)。则D原子的坐标参数为
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76pm,其密度为
您最近一年使用:0次
【推荐2】用煤炭制得的焦炭在工业上是重要的还原剂和燃料,用于许多物质的例备,如工业上用焦炭与硫酸钠反应制备硫化钠。反应方程式如下:Na2SO4+2C Na2S+CO2↑
Na2S+CO2↑
完成下列填空:
(1)上述反应的元素中,原子半径最小的元素的原子的核外电子排布式为___________ ,其最外层电子有 ___________ 种不同的能量,有 ___________ 种不同的运动状态。
(2)下列可以证明二氧化碳是非极性分子的事实是___________ (填编号)。
a.二氧化碳密度比空气大
b.二氧化碳能溶于水
c.液态二氧化碳在电场中通过不偏向
d.二氧化碳常温常压下为气态
(3)判断C、S两种元素非金属性的强弱,并写出一个能支持你的结论的实验事实___________ ,
(4)工业上利用焦炭与高温水蒸气反应制备水煤气,下面是水煤气反应的方程式:C(s)+H2O(g) CO(g)+H2(g)-Q(Q<0),写出上述反应的平衡常数表达式
CO(g)+H2(g)-Q(Q<0),写出上述反应的平衡常数表达式 ___________ ,增大该反应平衡常数的措施有 ___________ (填编号)
A.升温 B.增加水蒸气的浓度 C.减压 D.增加焦炭的量
(5)在一个2L的容器中进行该反应的实验,若混合气体的密度不变,(填“能”或“不能”)___________ 判断该反应已经达到平衡状态。若初始加入的C为16.8g,10min后为7.2g,则v(H2)=___________ 。
 Na2S+CO2↑
Na2S+CO2↑完成下列填空:
(1)上述反应的元素中,原子半径最小的元素的原子的核外电子排布式为
(2)下列可以证明二氧化碳是非极性分子的事实是
a.二氧化碳密度比空气大
b.二氧化碳能溶于水
c.液态二氧化碳在电场中通过不偏向
d.二氧化碳常温常压下为气态
(3)判断C、S两种元素非金属性的强弱,并写出一个能支持你的结论的实验事实
(4)工业上利用焦炭与高温水蒸气反应制备水煤气,下面是水煤气反应的方程式:C(s)+H2O(g)
 CO(g)+H2(g)-Q(Q<0),写出上述反应的平衡常数表达式
CO(g)+H2(g)-Q(Q<0),写出上述反应的平衡常数表达式 A.升温 B.增加水蒸气的浓度 C.减压 D.增加焦炭的量
(5)在一个2L的容器中进行该反应的实验,若混合气体的密度不变,(填“能”或“不能”)
您最近一年使用:0次
【推荐3】太阳能电池一共可分为三代,请回答下列问题:
(1)第一代太阳能电池为硅基太阳能电池,其中单晶硅太阳能电池的转化效率最高,技术最为成熟,应用最为广泛。
①在基态Si原子中,电子占据的最高电子层符号为_______ ,电子占据的最高能级的电子云轮廓图为_______ 。
②根据对角线规则,Si的一些化学性质与_______ (填短周期元素名称)相似。
(2)第二代太阳能电池是薄膜太阳能电池,如砷化镓电池。
①原子半径:Ga_______ (填“大于”或“小于”,下同)As,第一电离能:Ga_______ As。
②As的最高价氧化物的化学式为_______ 。
③Ga、F、Cl的电负性由大到小的顺序为_______ 。
(1)第一代太阳能电池为硅基太阳能电池,其中单晶硅太阳能电池的转化效率最高,技术最为成熟,应用最为广泛。
①在基态Si原子中,电子占据的最高电子层符号为
②根据对角线规则,Si的一些化学性质与
(2)第二代太阳能电池是薄膜太阳能电池,如砷化镓电池。
①原子半径:Ga
②As的最高价氧化物的化学式为
③Ga、F、Cl的电负性由大到小的顺序为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17种元素.回答下列问题;
(1)钪(Sc)元素的原子核外电子排布式为_____________ 。钬(Ho)的基态原子电子排布式为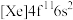 ,一个基态原子所含的未成对电子数为
,一个基态原子所含的未成对电子数为_________ 。
(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价。请根据下表中的电离能数据判断表中最有可能有+4价的元素是_____________ 。
几种稀土元素的电离能(单位:kJ/mol)
(3)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm +ICH2CH2I→SmI2+ CH2=CH2;ICH2CH2I中碳原子杂化轨道类型为________ 。
(4)离子化合物Na3[Sc(OH)6]中,存在的作用力除离子键外还有___________ 。
(5)1molCH2=CH2中含有的 键数目为:
键数目为:____________ 。
(1)钪(Sc)元素的原子核外电子排布式为
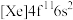 ,一个基态原子所含的未成对电子数为
,一个基态原子所含的未成对电子数为(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价。请根据下表中的电离能数据判断表中最有可能有+4价的元素是
几种稀土元素的电离能(单位:kJ/mol)
| 元素 | I1 | I2 | I3 | I1+I2+I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 4257 | 7019 |
| Y(钇) | 616 | 1181 | 1980 | 3777 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 3455 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3523 | 3547 |
(4)离子化合物Na3[Sc(OH)6]中,存在的作用力除离子键外还有
(5)1molCH2=CH2中含有的
 键数目为:
键数目为:
您最近一年使用:0次
【推荐2】下表是元素周期表前四周期的一部分,X、Y、Z、R、Q、W、J是7种元素的代号。回答下列问题时,涉及元素书写的请用相应的元素符号。

(1)J基态原子的核外电子排布式为________ 。基态Q2+中未成对电子数为________ ;R和Y的简单离子与Na+半径大小顺序为________ 。
(2)X、Y、Z三种元素电负性由大到小的排序是________ ;X与Y的第一电离能:X________ (填“>”“<”或“=”)Y,其理由是________ 。
(3)检验某溶液中是否含有Q3+的方法是_____________________________ 。
(4)已知WX3是一种引爆剂,受撞击时分解为两种单质,则其化学方程式为________________ 。

(1)J基态原子的核外电子排布式为
(2)X、Y、Z三种元素电负性由大到小的排序是
(3)检验某溶液中是否含有Q3+的方法是
(4)已知WX3是一种引爆剂,受撞击时分解为两种单质,则其化学方程式为
您最近一年使用:0次
【推荐3】前四周期元素结构信息见表,回答下列问题。
(1)A、B、C、E四种元素,第一电离能由大到小的顺序为___________ (用元素符号表示)。
(2)基态D元素的核外电子排布式为___________ 。
(3)写出B基态原子价电子的轨道式___________ 。
(4)E基态原子填有电子的轨道数为___________ 。
| 元素 | 结构信息 |
| A | 基态原子有6个原子轨道填充满电子,有3个未成对电子· |
| B | M层电子数比L层电子数少两个 |
| C | 基态原子有17个不同运动状态的电子 |
| D | 基态原子的价电子排布为3dx4s2,在常见化合物中其最高正价为+7 |
| E | 基态原子的M层全充满,N层没有成对电子,只有1个未成对电子 |
(2)基态D元素的核外电子排布式为
(3)写出B基态原子价电子的轨道式
(4)E基态原子填有电子的轨道数为
您最近一年使用:0次
【推荐1】X、Y、Z、W、R是中学化学常见的五种元素,原子序数依次增大。基态X原子s能级上的电子数等于p能级上的电子数的2倍;基态Y原子2p能级上有1个电子的自旋方向与其他电子的自旋方向相反;基态Z原子核外p能级和s能级上的电子数相等;W与Y同族;R为27号元素。
(1)上述元素位于元素周期表的p区的有___________ 种,元素X有___________ 种不同能级的电子。
(2)基态R原子的价层电子排布式为___________ , 与
与 的未成对电子数之比为
的未成对电子数之比为___________ 。
(3)X、Y、Z的电负性由大到小的顺序为___________ (用元素符号表示),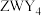 的晶体类型为
的晶体类型为___________ 。
(4)X和W形成的化合物 为一种液体溶剂,该化合物
为一种液体溶剂,该化合物___________ (填“易”或“难”)溶于水,原因为___________ 。
(1)上述元素位于元素周期表的p区的有
(2)基态R原子的价层电子排布式为
 与
与 的未成对电子数之比为
的未成对电子数之比为(3)X、Y、Z的电负性由大到小的顺序为
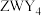 的晶体类型为
的晶体类型为(4)X和W形成的化合物
 为一种液体溶剂,该化合物
为一种液体溶剂,该化合物
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】氰化钾是一种剧毒的物质,贮存和使用时必须注意安全。已知:KCN+H2O2=KOCN+H2O,回答下列问题:
(1)OCN-中所含三种元素的第一电离能从大到小的顺序为_________ (用元素符号表示,下同),电负性从大到小的顺序为__________ ,基态氮原子价电子排布图为__________________ 。
(2)H2O2中的共价键类型为_____ (填“σ键”或“π键”),其中氧原子的杂化轨道类型为__________ ;分子中4个原子______ (填“在”或“不在”)同一条直线下。
(1)OCN-中所含三种元素的第一电离能从大到小的顺序为
(2)H2O2中的共价键类型为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】氧族元素的单质及其化合物是一类重要物质,请回答下列问题。
⑴基态硒(Se)原子的价层电子排布式为____________ 。
⑵OCN-中所含三种元素的电负性从大到小的顺序为________ (用元素符号表示,下同);第一电离能从大到小的顺序为________ 。已知等电子体具有相同的空间构型,则OCN-的空间构型为_______ 。
⑶H2O2分子中氧原子的轨道杂化类型是__________ ;H2O的沸点明显高于H2Se的沸点( 42℃),其主要原因是
42℃),其主要原因是_______________ 。
⑷硒化锌的晶胞结构如图所示,则硒化锌的化学式为_________ ,其中Zn(黑球)的配位数为______ 。

⑴基态硒(Se)原子的价层电子排布式为
⑵OCN-中所含三种元素的电负性从大到小的顺序为
⑶H2O2分子中氧原子的轨道杂化类型是
 42℃),其主要原因是
42℃),其主要原因是⑷硒化锌的晶胞结构如图所示,则硒化锌的化学式为

您最近一年使用:0次



